提供:サスメド株式会社 2024年6月期第2四半期決算説明会
【QAあり】サスメド、不眠障害治療用アプリは保険収載に向けた検討を開始、耳鳴治療用アプリの特定臨床研究も進行中
ビジョン
上野太郎氏(以下、上野):本日はお集まりいただき、ありがとうございます。サスメド株式会社代表取締役社長の上野です。それでは、弊社の第2四半期決算説明会を開催します。
弊社は「ICTの活用で『持続可能な医療』を目指す」をビジョンに掲げており、その意味である「SUStainable MEDicine」を略して、サスメドと称しています。
事業領域概要
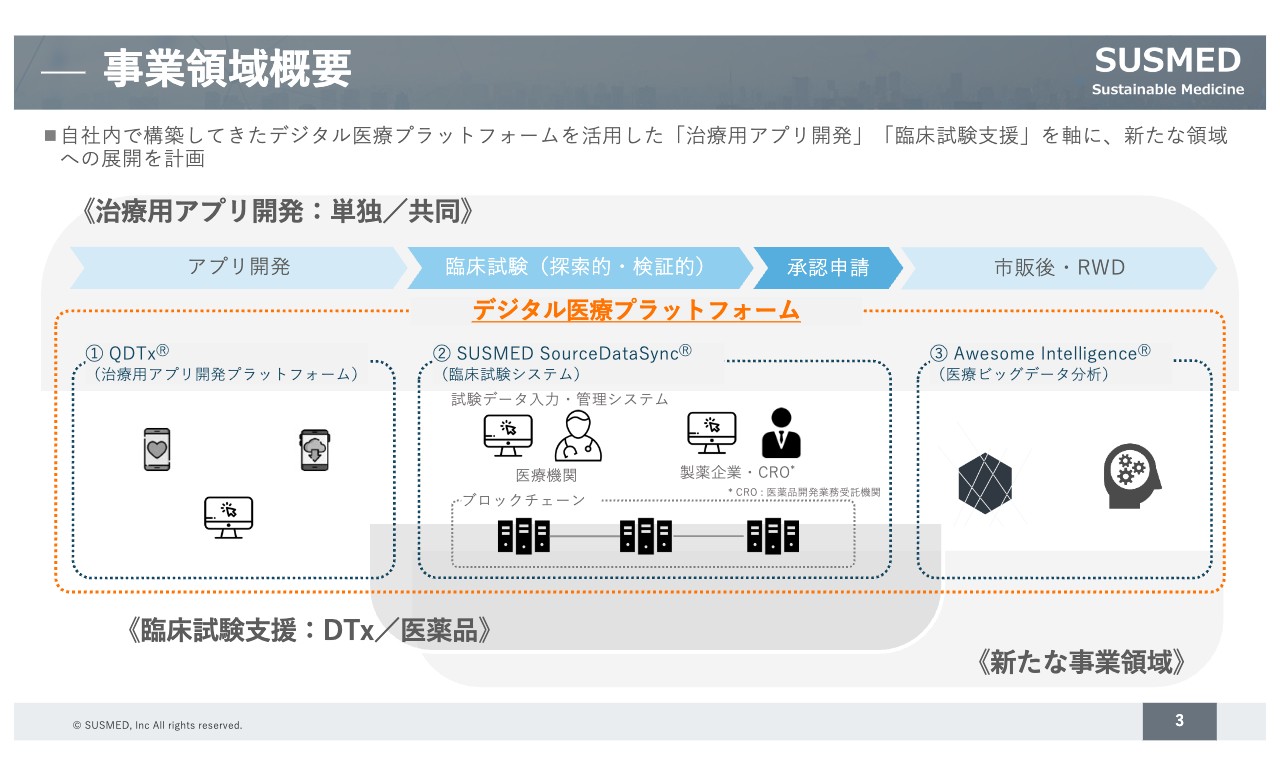
具体的な取り組みとして、事業領域の概要をご説明します。弊社は、医療プラットフォームを活用した治療用アプリの開発や臨床試験支援を軸に、事業を展開しています。
デジタル医療プラットフォームには、治療用アプリを効率よく開発するための「Q(クイック)DTx」、ブロックチェーン技術を実装した臨床試験システム「SUSMED SourceDataSync」、医療ビッグデータ分析を行う「Awesome Intelligence」があります。これらのプラットフォームを活用して事業を進めています。
QDTx:治療⽤アプリ開発プラットフォーム
それぞれのプラットフォームについてご紹介します。
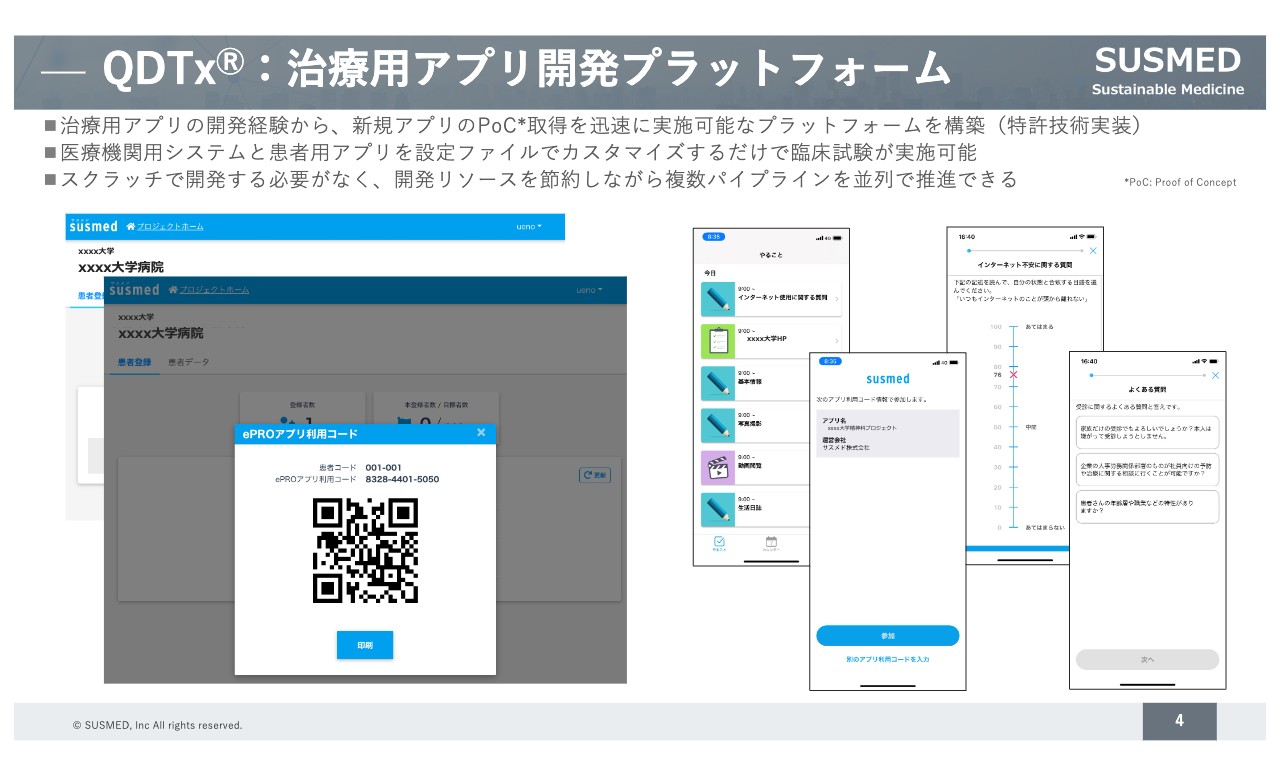
治療用アプリ開発プラットフォームの「QDTx」は、これまで治療用アプリを開発してきた経験や技術を実装したプラットフォームです。治療用アプリで使用する機能をモジュールベースで組み合わせることで、効率よく開発することができます。また、この後にご説明する当社の臨床試験システムと連動させることで、臨床試験の実施までを見据えた開発が可能となっています。
これらのプラットフォームを活用しながら、自社の複数のパイプラインを開発しており、最近では、製薬企業との共同開発の際にも、こちらのプラットフォームを活用しています。
SUSMED SourceDataSync:臨床試験システム

臨床試験の効率化のために用いている「SUSMED SourceDataSync」というプラットフォームについてご説明します。こちらは、ブロックチェーン技術を臨床試験に用いるという、弊社の特許技術を実装した仕組みになっています。
治験などの際にはデータの信頼性を担保することが規制により求められていますが、このシステムでは、これまで人が担保してきた部分をブロックチェーン技術が代替します。すでに複数の治験で活用されており、製薬企業との共同開発事例でも稼働しています。最近では、「レジストリ」という治験以外の分野にも活用する取り組みを進めています。
Awesome Intelligence:機械学習⾃動分析システム
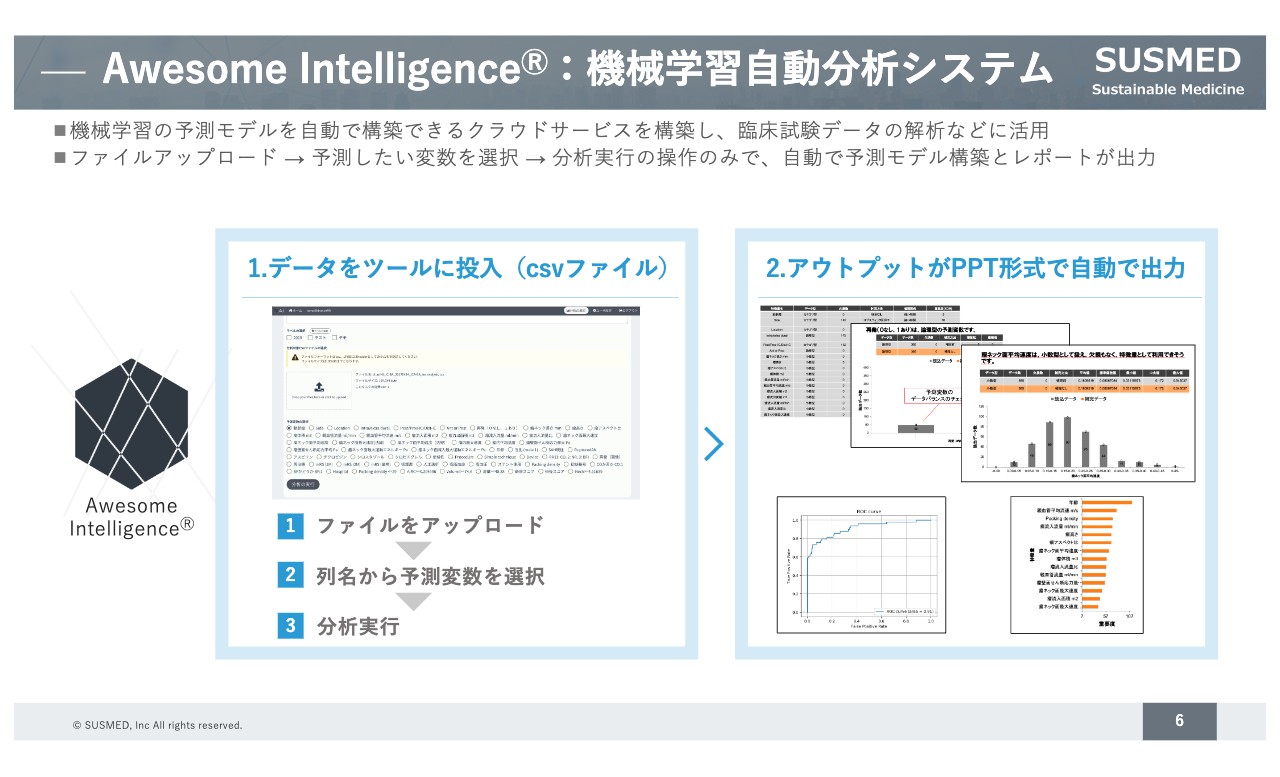
医療ビッグデータ分析のプラットフォームの「Awesome Intelligence」についてご説明します。機械学習を効率よく実施するシステムを活用することで、すでに保有している医療ビッグデータや今後保有する治療用アプリのビッグデータを効率よく分析できます。
治療⽤アプリの提供の流れ
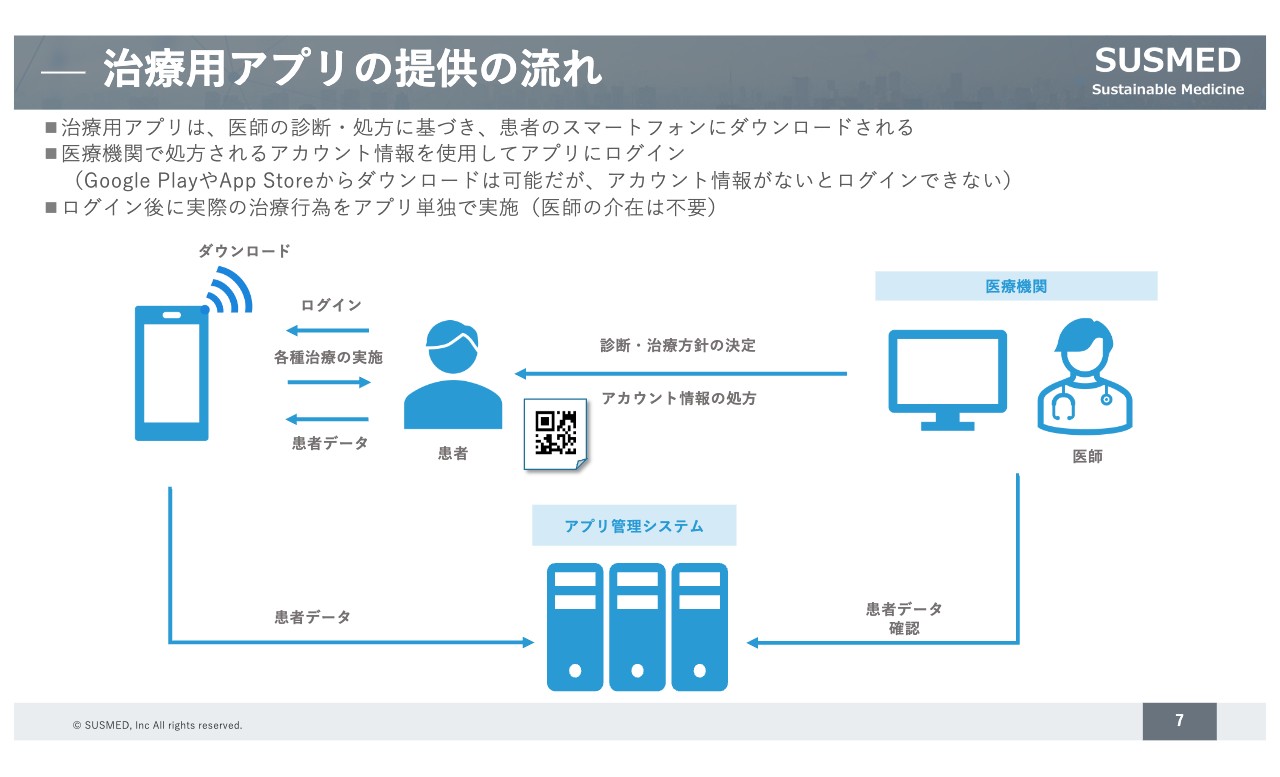
これらのシステムを活用することで、治療用アプリの開発を進めています。治療用アプリは、行政用語では「プログラム医療機器」と呼ばれます。医師が診断した患者に対してアカウントを処方することで、患者が自身のスマートフォンに治療用アプリをダウンロードし、自宅にいながら治療を受けられる仕組みになっています。
実際の治療はアプリのアルゴリズムで実施するため、いわゆる遠隔診療とは違い、医師が介在することなく治療が実施できます。日々生み出される患者のデータを、医療機関の医師が確認できるシステムも提供しています。
このようなシステムを活用することで、医師が効率よく患者のデータを確認して診療に用いることができます。
ヘルスケアアプリと治療⽤アプリの違い
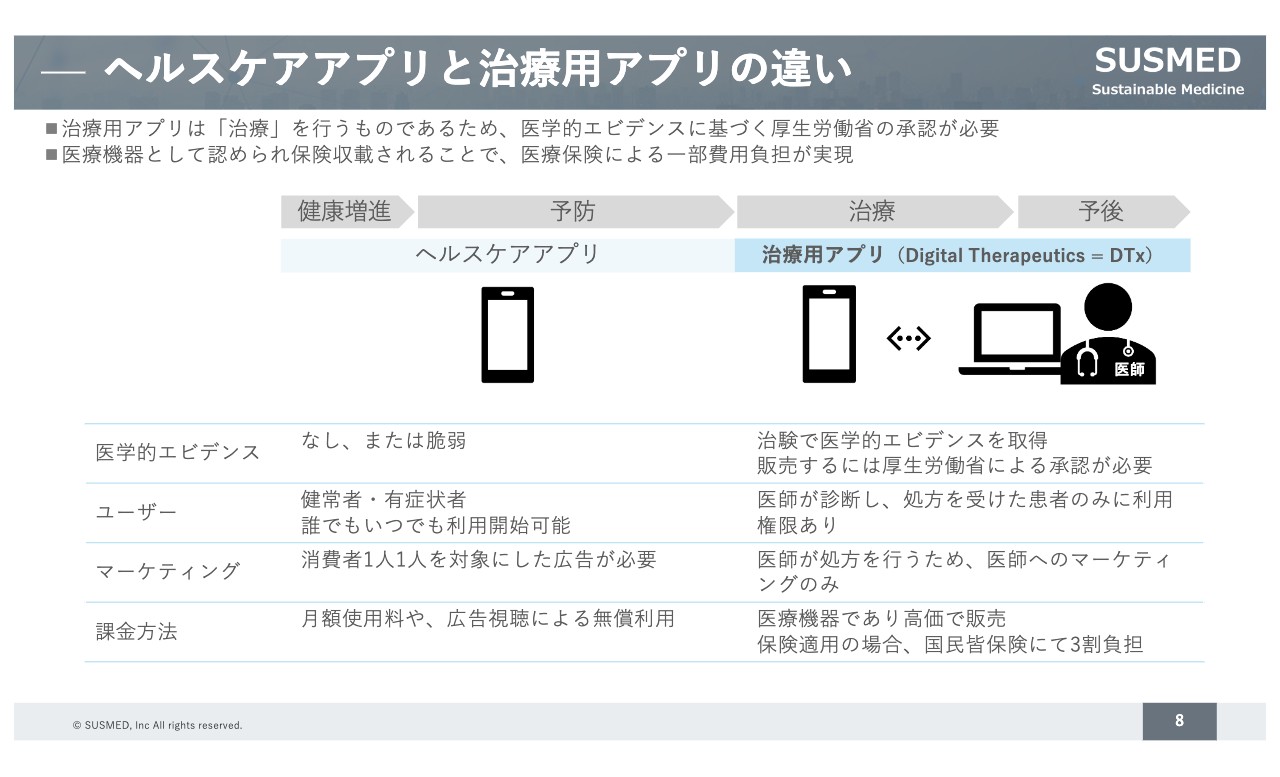
一般的なヘルスケアアプリと治療用アプリの違いについてご説明します。現在世の中にあるヘルスケアアプリは、健常者が健康増進を目的として使うものとなっています。
一方で、弊社の治療用アプリは医療機器に該当し、治療を行うものになります。そのため、医薬品や医療機器と同じように医学的なエビデンスに基づいた厚生労働省の承認が必要です。
開発パイプライン①(2024年2⽉14⽇現在)
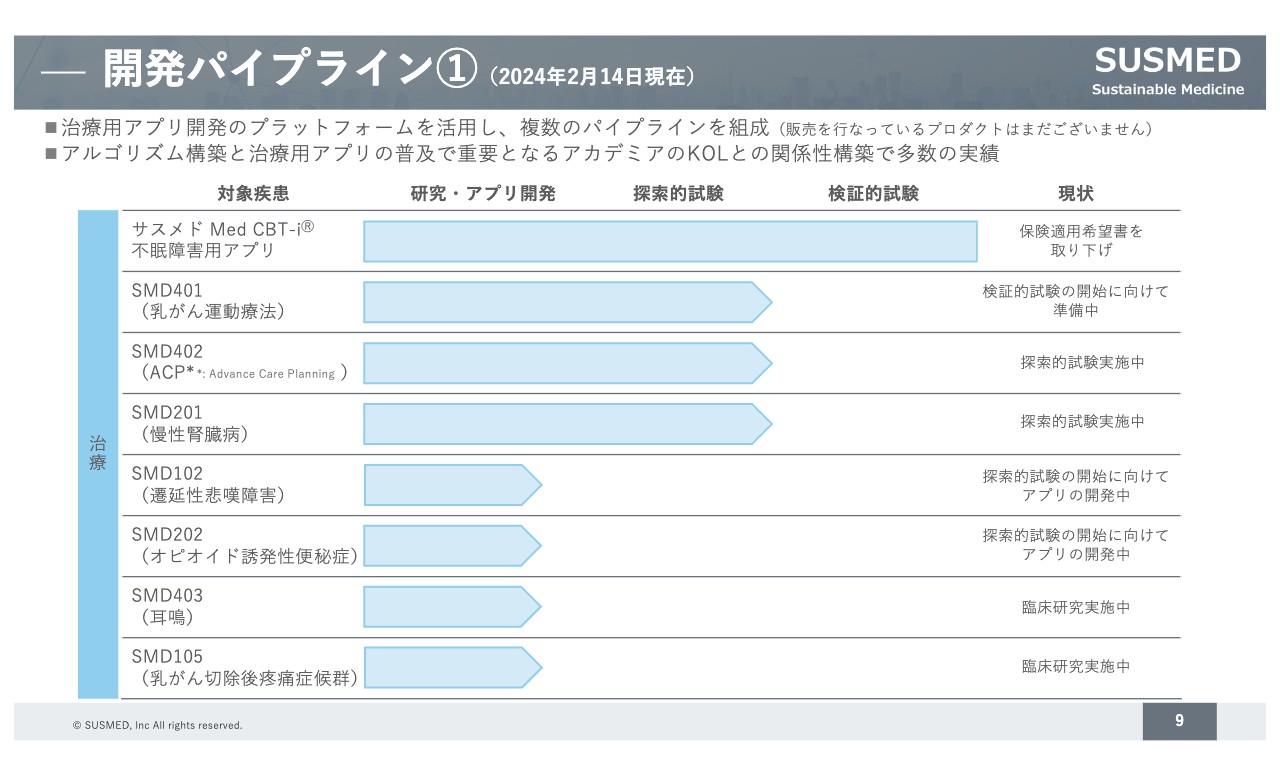
スライドには、弊社が保有する治療用アプリの開発パイプラインを掲載しています。不眠障害治療用アプリはすでに承認を取得しています。現在、保険適用希望書については一時的に取り下げていますが、今後は、保険収載されることで患者の一部の自己負担で処方できる状態を目指して、あらためて保険適用に向けた手続きを進めていきます。
その他のアプリもそれぞれ開発を進めており、特に、がん患者や慢性腎臓病向けのアプリのフェーズが進んでいます。製薬企業と開発を進めているものとしては、杏林製薬と進めている耳鳴治療用アプリや、あすか製薬と進めている産婦人科領域のアプリがあります。
開発パイプライン②(2024年2⽉14⽇現在)
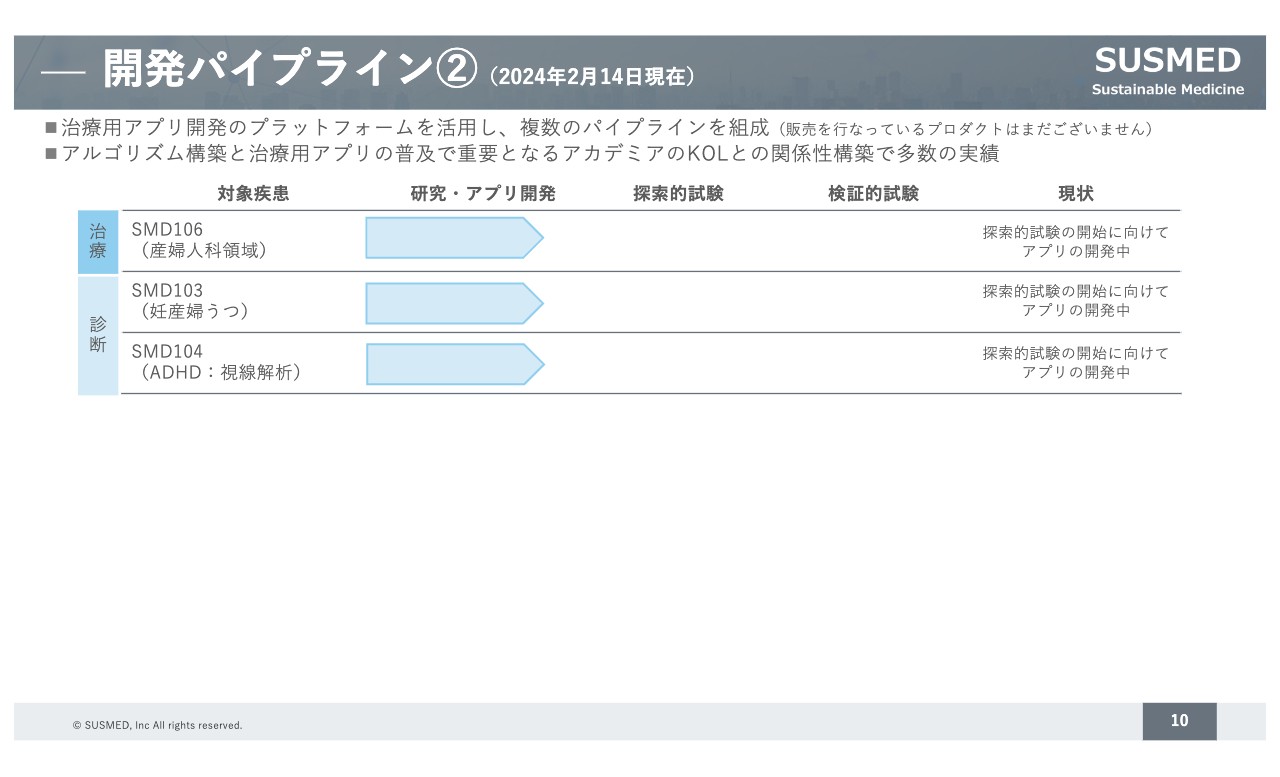
治療用以外に診断用のアプリも開発しています。診断プログラムも医療機器として承認対象となるため、妊産婦うつの早期診断や視線解析を用いた発達障害の診断プログラムの開発を進めています。
2024年6⽉期 重点施策

今期の重点施策についてです。これまでお伝えしていたように、不眠障害治療用アプリの販売開始に注力するとしています。その他のいくつかの治療用アプリについても、開発を進めていくこととしています。
プラットフォーム事業では、臨床試験システム「SUSMED SourceDataSync」の新規案件の獲得を目指しています。加えて、治験以外の分野で医療データを活用するための取り組みとして、レジストリ構築でのブロックチェーン技術の活用も重点施策としています。
重点施策① 不眠障害治療⽤アプリの販売開始
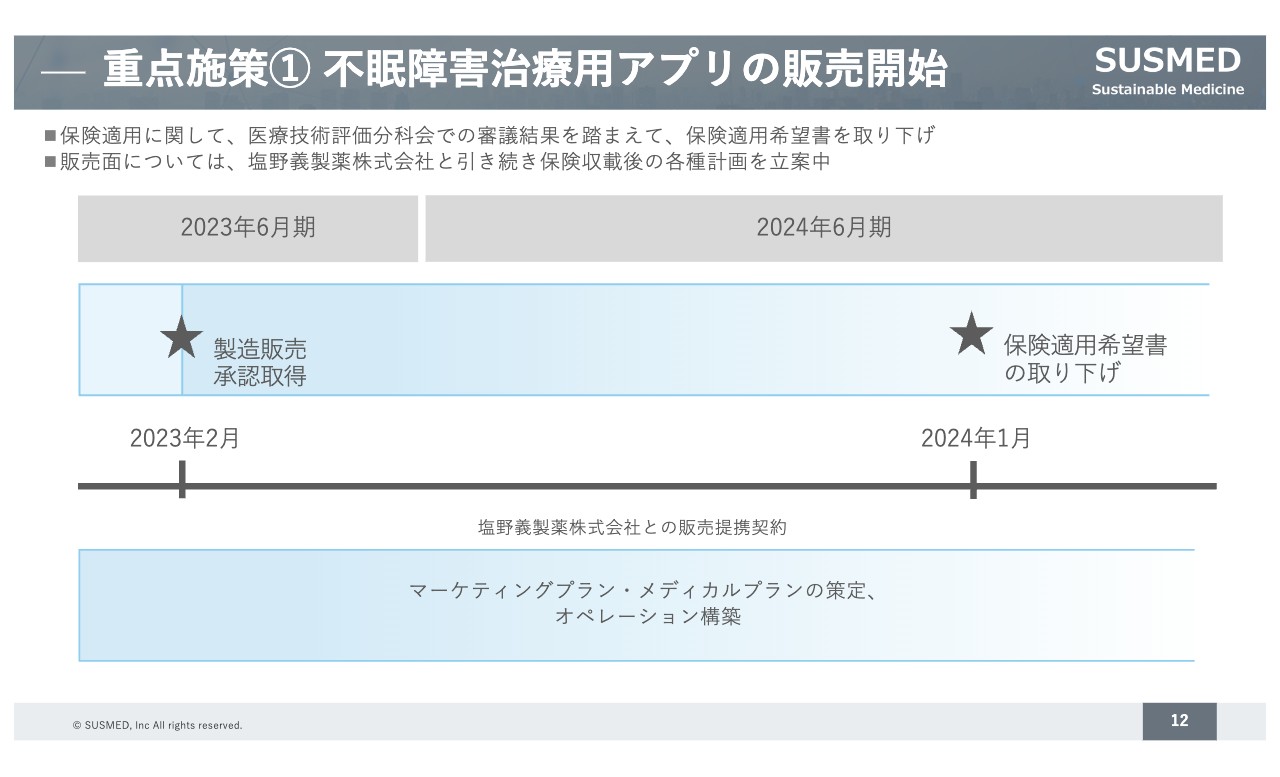
1点目の重点施策である、不眠障害治療用アプリの販売開始に向けた取り組みについてご説明します。
保険適用については先日リリースしたとおり、令和6年度の診療報酬改定の議論において、「対面式の認知行動療法の診療報酬算定を見送る」という審議結果が出て、同時に当社の治療用アプリについても「保険収載を見送る」という結論が出されました。こちらを受け、弊社としては保険適用希望書を取り下げています。
販売面については、塩野義製薬との関係性は特段変わらず、このアプリを医療現場に届ける計画および保険収載後の各種計画立案を引き続き進めています。
重点施策① 不眠障害治療⽤アプリの販売開始

保険適用希望書の取り下げについては、1月29日にIRリリースを出しています。先ほどお伝えしたように、令和6年度の診療報酬改定のタイミングでの保険適用は見送られる方針となったため、取り下げました。
一方で、医療機器として製造販売の承認を取得している事実は変わらないため、不眠障害治療用アプリの保険収載を目指す方針は今後も変わりません。
重点施策② パイプラインの開発進捗

2点目の重点施策である、パイプラインの開発進捗です。前期から行っている杏林製薬との耳鳴治療用アプリは、今期に特定臨床研究を開始することができました。
昨年11月2日に最初の被験者による治療用アプリの利用が開始され、マイルストンを達成したため、1億円を受領しています。第2四半期は、前期に受領した契約一時金の1億円と合わせた計2億円を収益として計上しています。特定臨床研究については、現在も粛々と進めている状況です。
重点施策④ レジストリ構築の開始(再掲)
4点目の重点施策である、弊社のブロックチェーン技術を用いた治験以外の分野への活用事例をご説明します。こちらは東北大学に事務局となっていただき、学会や医療機器メーカーとともに、静脈疾患レジストリの構築を行うことで基本合意しています。
ブロックチェーン技術をレジストリデータに活用する意味は、データの信頼性を担保し価値を向上させることにより、データ活用の幅を広げられる点にあります。このような技術を活用してデータのクオリティを上げることは、医療技術開発の効率化につながると考えています。
2024年6⽉期 重点施策の進捗状況

今期の重点政策の進捗状況です。不眠障害治療用アプリは、保険適用希望書の取り下げを行っていますが、今後の保険収載に向けた検討を開始しています。
耳鳴治療用アプリは、特定臨床研究を進めているのと同時に、ブロックチェーン技術を用いた臨床試験システムの活用も開始しています。治療用アプリのパイプラインを開発することに加えて、弊社のプラットフォームを活用し効率的な臨床試験を実施するという、2つの意味があるプロジェクトになっています。
レジストリ構築については、静脈疾患レジストリの構築に関するプロジェクトを進めています。
その他
第2四半期のその他の進捗としては、文部科学省科学研究費助成事業指定研究機関として承認を受けました。今後は、こちらも活用していきます。
業績ハイライトと今期の業績予想
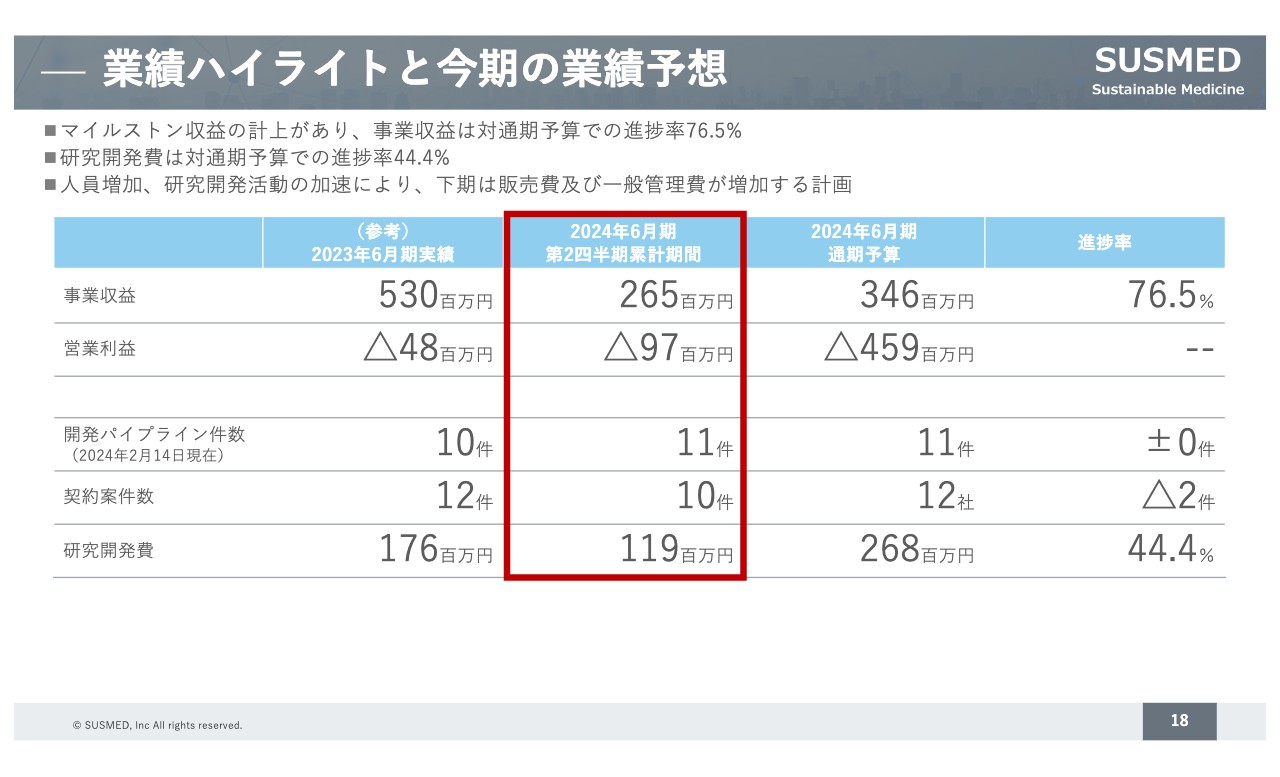
業績ハイライトです。第2四半期の事業収益は、先ほどお伝えしたマイルストン収益の計上があったため、2億6,500万円となっています。営業利益はマイナス9,700万円となりました。研究開発はそれぞれのパイプラインを進めていくために、引き続き投資を行っていきます。
セグメント業績
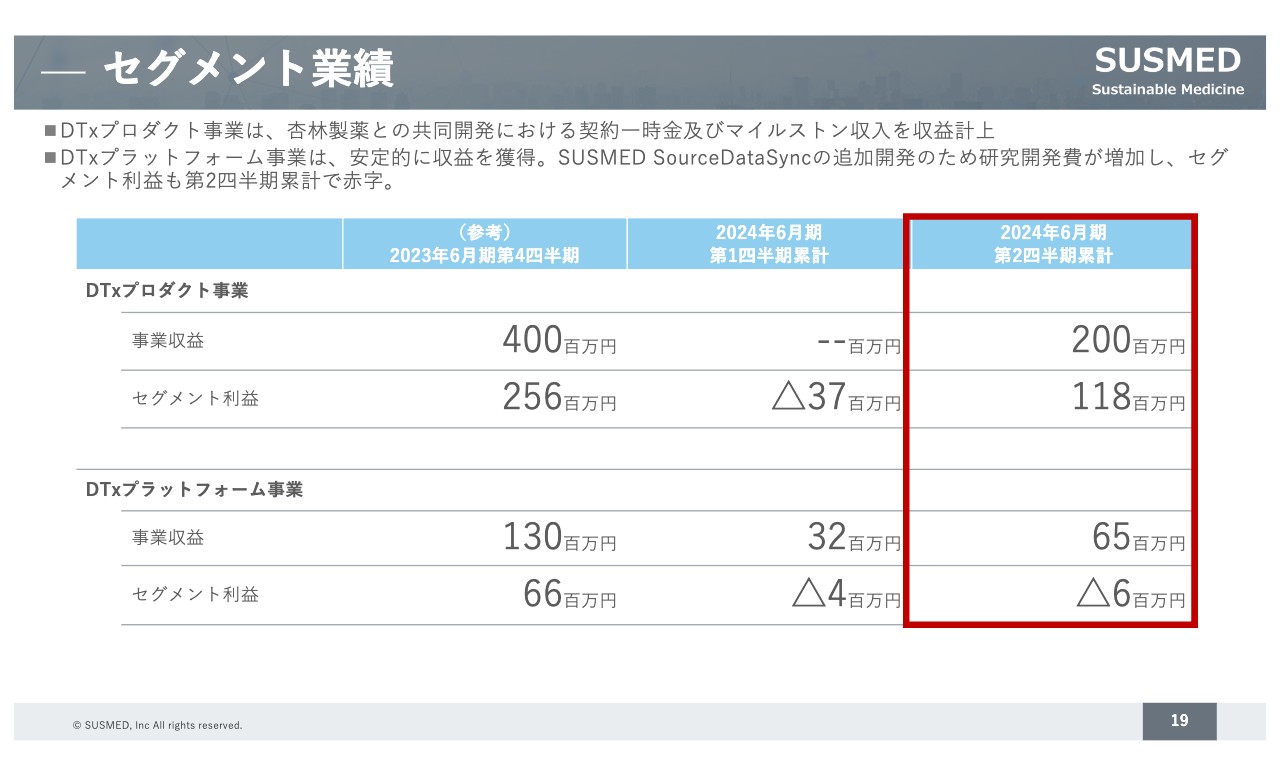
セグメント別の業績についてご説明します。先ほどお伝えしたように、杏林製薬との耳鳴治療用アプリで受領した2億円は、DTxプロダクト事業の収益となっています。プラットフォーム事業は「SUSMED SourceDataSync」の収益を計上している一方で、追加開発等により研究開発費が増えています。
財務状況
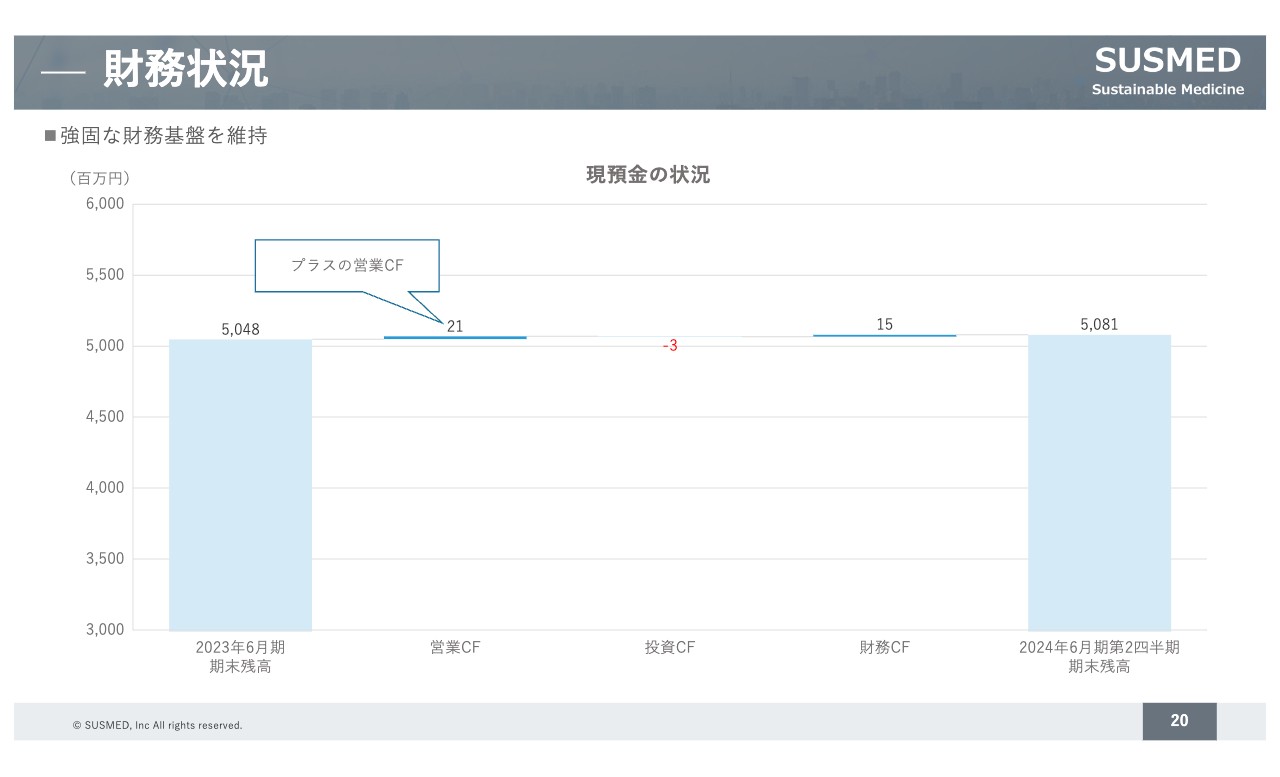
財務状況については、強固な財務基盤を維持しています。約50億円のキャッシュがあるため、研究開発や保険収載に向けた取り組みを問題なく安定的に継続できる状況です。
質疑応答:治療用アプリの保険収載に対するハードルについて
質問者:不眠障害治療用アプリの保険収載が取り下げになりましたが、アプリの保険収載に対するハードルについてはどのように捉えていますか? 今回の経緯や、全体のアプリに対する考えをお聞かせください。
上野:現在の制度面についてご説明します。令和6年度の診療報酬改定に向け、当社のアプリは「診療報酬の技術料の準用」としての保険適用を希望していました。要は、医師が診療行為として行う対面の認知行動療法の技術料を準用するかたちで保険適用するということです。
しかし、弊社のプロダクトと関連する、医師が行う対面式の認知行動療法の不眠症への適応拡大が見送られました。また、同時に当社の治療用アプリについても「保険収載を見送る」という結果となり、弊社は保険適用希望書を取り下げることにしました。こちらが令和5年度までの動きです。
一方で、厚生労働省からは令和6年度以降の方針が出されており、治療用アプリは原則として「特定保険医療材料」での評価に変えていくとされています。特定保険医療材料とは、イメージとしては薬価に近く、医療機器そのものに対して価格をつける評価方法がとられます。これまでも、心臓のペースメーカーなどが特定保険医療材料として薬価のような評価をされ、保険収載されています。
実際に、すでに保険収載がされているプログラム医療機器である禁煙用アプリや高血圧用アプリについても、今までの技術料の準用ではなく、特定保険医療材料という枠組みでの保険点数にシフトすると発表されています。
今はちょうど転換のタイミングだと推測しています。今後、特定保険医療材料としてプロダクトそのものを評価するかたちが整備されれば、技術料の準用時に生じる混乱はある程度解消されるだろうと期待しています。
質問者:素人のため理解が難しいのですが、行政の後出しじゃんけんのようにも聞こえます。一度は決めたけれども再び見直すということで、逆に言えば今後の保険適用の可能性はまったく小さくなっていないという見方でよいですか?
上野:おっしゃるとおり保険適用の可能性に変化はなく、混乱が解消されるという意味ではより予見性が高くなるのではないかと期待しています。
質問者:つまり、保険収載へのハードルがそれほど上がったわけではないということですね。今後の目処としては、粛々と申請し保険収載を取っていくかたちになりますか?
上野:そのとおりです。弊社としては、整備された新しい制度の中で粛々と手続きを進めていくかたちになると思っています。
質問者:薬価と同じ評価方法になると、現在の薬と同基準で毎年改定になると見ておいたほうがよいですか?
上野:いわゆる「引き下げ圧力」に関しては、診療報酬の技術料よりは薬価や特定保険医療材料のほうが若干あるのは事実だと思います。
質問者:行政はやはりそのように進めたいのでしょうか? 価格は最初に決めたけれども、再算定のようなかたちで見直しも行いたいため、そちらの方向に制度を変更したいということですか?
上野:制度の意図についてはお答えしかねます。しかし、特定保険医療材料としての評価に変更となり今までのように技術料に依存することがなくなる一方で、過去の薬価改定の経緯などを見ていると、再算定などはあり得ると考えています。
質疑応答:肥満に対する治療用アプリの可能性について
質問者:現在アメリカでも非常に話題になっている肥満については、ヘルスケアアプリや治療用アプリが一番有効なイメージがあります。加えて、マーケットも大きいため、素人的にはむしろ肥満治療用アプリを開発したほうが、患者にとっても先生方にとっても大変便利かつ株式市場にとっても極めてプラスになる印象がありますが、社長はどのように考えていますか?
上野:確かにマーケット規模は非常に大きいと思います。一方で、優れた薬がすでにある領域でもあるため、治療用アプリを出してもどこまで使ってもらえるのかという問題はあります。
最近もいろいろなニュース等になっていますが、抗肥満薬はイノベーションが非常に進んでいる分野で、肥満に対して本当に有効なGLP-1作動薬という薬も出てきています。そのようなものがない段階であれば、アプリで対策を取る選択肢はあると思うものの、今はお薬で簡便に肥満対策ができる時代に入ってきています。そのように考えると、弊社としては治療用アプリの優先度は決して高くはないと考えています。
質問者:新しい薬も出てきているものの、薬には当然副作用もたくさんあります。特に肥満は病気なのかわからないからこそ、そのような分野では薬に頼らない治療のほうがよく、アプリでの治療が有効だと言えるかと思っていましたが、そうではないのでしょうか? やはり何もない分野のほうが有効だと考えた方がよいですか?
上野:おっしゃるとおり、副作用とのバランスはとても重要だと思います。そのような意味では、不眠症においてもまさに睡眠薬の依存性が大変大きな問題になっているため、実際にガイドラインでも「睡眠薬よりも、認知行動療法を行いましょう」と言われています。
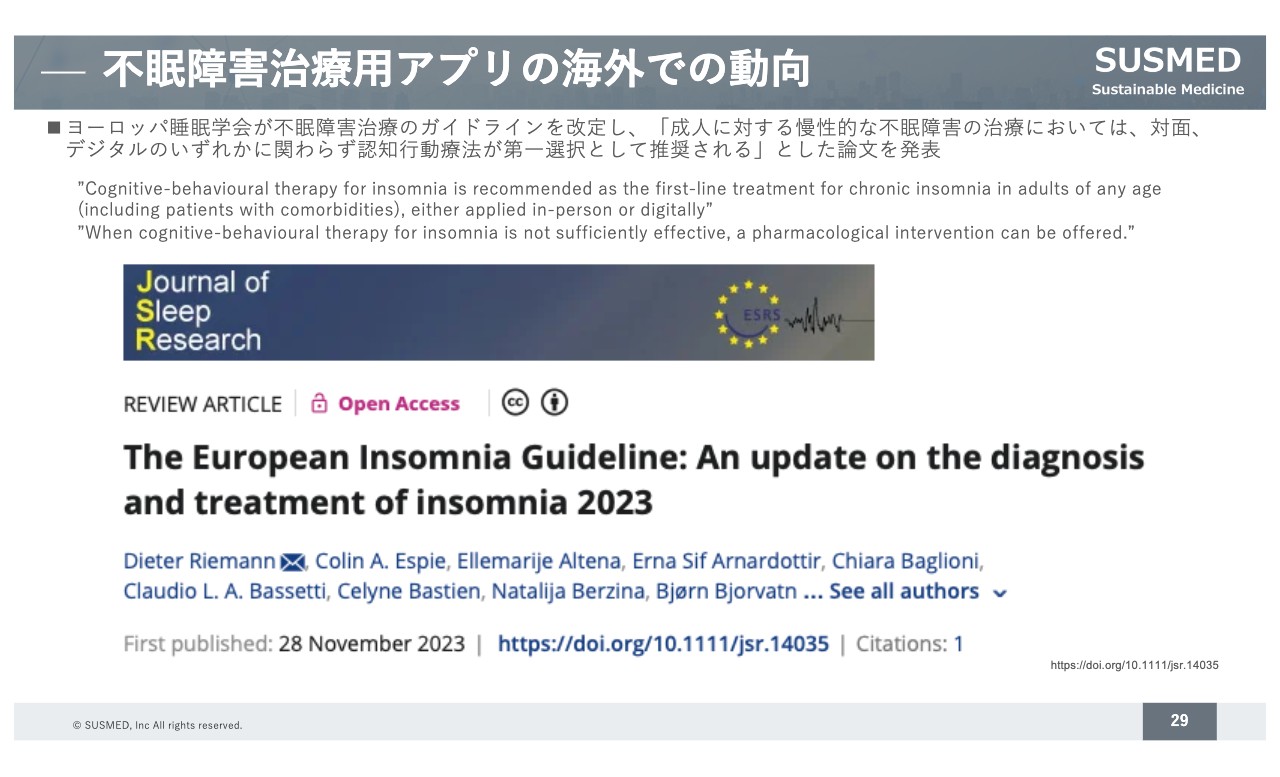
さらに最近では、スライドにも記載しているとおり、ヨーロッパの不眠症のガイドラインが改訂され、対面で行う認知行動療法とデジタルで行う認知行動療法が第1選択として併記されました。そのような意味では「睡眠薬のように依存性などの副作用が問題になる分野ならばアプリのほうがよい」というコンセンサスは得られると思います。
そのため抗肥満薬についても、副作用が問題視されるかたちになるのであれば、治療用アプリ開発の可能性はあると思っています。
質疑応答:アプリの保険適用の評価方法について
質問者:先ほど「これまで出ているアプリも、プログラム医療機器に関しては特定保険医療材料となる」とのご説明がありましたが、アプリは今後すべて特定保険医療材料になるということでしょうか?
上野:すべてが特定保険医療材料として保険適用となるかどうかについてはお答えしかねますが、厚生労働省が出している令和6年度からの方針では「原則、特定保険医療材料として評価する」という記載になっています。
そのため、一部異なる可能性はあるものの、基本的には特定保険医療材料になると認識しています。
質疑応答:医療技術評価分科会資料記載の文言の意図について
質問者:1月15日開催の医療技術評価分科会の資料に「評価すべき医学的な有用性が十分に示されていない」と記載されていたことが気になるのですが、これについてはいかがでしょうか?
上野:その文言については、対面式の認知行動療法の不眠症への適応拡大に関する評価でもまったく同じ記載がされていたと思います。
弊社は厚生労働省が出している書類について発言する立場にはありませんが、弊社のプロダクトは実際に治験を実施し、その結果として有効性や安全性が認められたことをもって製造販売承認を取得していますし、推測にはなりますが「対面式の認知行動療法自体」に対する評価と同じ内容をそのまま弊社のプロダクトに対して当てはめているものと認識しています。
質疑応答:保険適用制度の変更が普及スピードに与える影響について
質問者:もともと御社は技術料の準用を意図した保険適用を目指していたものの、国の方針で特定保険医療材料としての評価に変わってしまっているわけですが、このことは普及スピードに影響を与えるのでしょうか? 臨床医が採用するにあたって、今回の変化はどのような影響を与えると考えていますか?
上野:基本的に医療や臨床の現場では、技術料の準用なのか特定保険医療材料なのかはそれほど意識せずに使われていると思います。保険適用を希望する企業側からすればかなり大きな分かれ道ではあるものの、医療現場の医師側からすれば、そこを意識して使用の判断をすることにはあまりならないと認識しています。
質問者:御社の不眠障害用アプリに対する収益の期待値に関しては、確か「5年後にピークを目指したい」というご説明だったかと思います。そのイメージは今回の制度変更によって何か変わりますか?
上野:基本的にはその見通し自体は変わるものではありません。もちろん、現時点では保険収載のタイミングが後ろにずれる可能性が高くなっていますが、ピークセール到達までの期間については変わるものではないと考えています。
先ほどの臨床医の採用意向への影響に関するご説明に補足して、今回の診療報酬改定では「プログラム医療機器管理料」が新設されています。こちらは、治療用アプリなどのプログラム医療機器を使って診療を行う行為そのものについて、医療者側に別途保険点数がつくものです。今回は、その部分で保険請求ができるように整備されていることもお伝えしておきます。
質疑応答:再申請後のスケジュールについて
質問者:まだ再申請は行っていないと思うものの、再申請後のスケジュールについて、時期的な目途はどのように考えればよいですか?
上野:新しい制度が施行されて以降に再申請することになると思います。その後のスケジュールについては、厚生労働省の出している資料に基づきますと、新しい医療機器は通常その特定保険医療材料等で保険適用希望書が出てから、だいたい5ヶ月から6ヶ月で区分決定するとされています。
また販売開始については、新医療機器だと1年に4回のタイミングがあるため、決定されてすぐ販売というわけではなく、5ヶ月から6ヶ月経過して区分が決定された後、一番近い3ヶ月ごとのタイミングで実際に販売が開始されるというのが一般的であると公開されています。そのため期待値としては、そのような時間軸で考えています。
質問者:厚生労働省に前回出した市場規模などの資料があると思うのですが、今回何かを作り替えなければいけないなどでいろいろと時間がかかるということはありませんか?
上野:もちろん先ほどお伝えしたように、技術料の準用なのか特定保険医療材料なのかは企業側にとってはかなり大きな分かれ道でもあるため、それに合わせた資料作成が必要になります。
加えて、そもそも新しい制度ですので、その部分の確認は厚生労働省に相談するかたちで進めることになると思います。そのような作業を、これから行っていきます。
質疑応答:今回の保険収載見送りの経緯について
質問者:私自身は、政府や国は治療用アプリを基本的にプッシュしており、促進していきたいと考えていると認識しています。今回の保険収載見送りについて、医療技術評価分科会が評価しないとなれば保険適用希望書を取り下げるしかないことは理解はしているものの、なぜこうなったのかが気になります。
そもそも特定保険医療材料にするか、診療報酬かというのはずいぶん前から見えており、かつ国もプッシュしている中でのたらい回し感は、他の先行品の点数の付け方を見ても、少し解せないところがあります。
今現在も当局と次の保険収載申請に向けて話をしているとは思いますが、どのような経緯で何があったのかを少し説明していただけますか?
上野:まず、プログラム医療機器を技術料の準用で評価するのか特定保険医療材料で評価するのかという部分については、大きな制度の話だと捉えています。
令和6年度以降に施行される制度については、当然令和5年度中にそのような議論がなされていたはずですが、制度としての施行タイミングの問題もあり、弊社の個別の品目についてそれを前倒しで適用することはしなかったのだと理解しています。
今回の医療技術評価分科会での判断の実際の背景は、繰り返しのご説明になりますが、認知行動療法の保険点数を準用するかたちで保険適用の希望書を出していたために、対面の認知行動療法を不眠症に適応拡大するかどうかの判断に引き摺られたと認識しています。
おっしゃるとおり国や政府も本来はプログラム医療機器を推進しているはずで、加えて、国として取り組んできている睡眠薬の過剰処方の問題解決にも資する製品であることは間違いないため、弊社しては対面の認知行動療法の不眠症への適応拡大とは切り分けて評価検討を行ってほしいと思う部分があるのは事実です。
実際の議論を見ているわけではなく推測の部分、わからない部分もありますが、このように理解しています。
質疑応答:令和6年度の保険適用について
質問者:令和6年度については、当局からも「特定保険医療材料として評価してよい」という基本方針が出ているため、そちらに向けて原価を積み上げるロジックを作り直すと思いますが、保険収載希望書をどう出すかなどの議論は始まっていますか? また、本当に特定保険医療材料として評価されるということを、ある程度は握れていますか?
上野:厚生労働省とはお話ししています。おっしゃるとおり、技術料の準用と特定保険医療材料の出し方には違う部分があることから、実際の出し方について相談している状況です。
特定保険医療材料は技術料の準用と考え方が大きく異なり、評価方法も原価積み上げ方式と類似のものを参照するかたちに大きく分かれることから、しっかり相談を行っています。
完全に握れているかについては、まだ新しい制度が施行されていませんので、当局として何か文書を発表するという確実なところには至っていないのが事実です。
質疑応答:中医協が資料で示した新たな方針について
質問者:中医協(中央社会保険医療協議会)がプログラム用医療機器の審査等々でいろいろな案を出している資料に「A3(既存技術・変更あり)とC2(新機能・新技術)として希望のあったプログラム医療機器は、保険医療材料等専門組織で議論し、既存の点数と見合わせて評価すべきではないかという議論について、医療技術評価分科会で審議を求めることができる」と書いてありました。
こちらのルートに乗ってしまうと、長年にわたり対面での認知行動療法の不眠症への適応拡大を希望しても厳しかった背景もあることから、御社のアプリの保険収載がさらに厳しくなったのではないかと懸念しています。この点について何かコメントできることはありますか?
上野:弊社もその資料の中で今引用された記載内容を確認していますが、「プログラム医療機器については、原則として特定保険医療材料として評価する」という方針との整合性について真意を図りかねています。こちらについては、厚生労働省に確認する必要があるかもしれないと思っているところです。
一方で、記載が該当する区分はかなり限定されているとも認識しています。プログラム医療機器や治療アプリについては、原則として特定保険医療材料として評価するという方針との関係性や、どちらを方針のメインとして考えているのかについては、これから確認したいと考えています。
質疑応答:保険収載の制度変更の背景について
質問者:今回の保険収載見送りについてです。もともと保険収載が遅れていたところに、規制当局側から技術料準用から特定保険医療材料へと変更する話があったということはありますか?
上野:政府の資料に特定保険医療材料へ移行する話が出たのは、昨年の暮れぐらいからです。ですので、弊社が保険適⽤希望書を出した時点では、そのような方針は出ていなかったと認識しています。
そのような意味では、保険収載に時間がかかっていたことと制度変更の話は、関連はないと思っています。
質疑応答:再申請時に発生するリスクの見込みについて
質問者:令和6年度に再申請したタイミングでは、追加の解析や試験が必要になるといったリスクは考えなくてもいいでしょうか?
上野:いわゆる治験等の大がかりな対応が必要になることはないと認識しています。
質疑応答:厚生労働省とのコンタクト頻度について
質問者:1月16日に厚生労働省が資料を発表してから2月までの約1ヶ月間に、厚生労働省などの当局側と何らかのコンタクトは取れていますか? 基本的には数ヶ月に1回程度しかコンタクトを取れないのか、担当者とすぐにやり取りできる環境なのかを教えてください。
上野:この発表以降の1ヶ月の間に複数回、厚生労働省とはお話ししています。
質疑応答:日本医師会の動きについて
質問者:例えばスイッチOTC医薬品などについて、日本医師会は総論賛成でも各論になると徹底的に潰しに来ます。不眠症治療薬を処方している医者はやはり開業医で、日本医師会の平均年齢は60歳を超えていることから、普通に考えるとアプリでの治療には腰が引けるのだと思います。
そこで、既得権益がこのようなものを潰しにくることはありますか? そもそも、不眠症治療用アプリが保険収載されないことが現実としてあり得るのかと思ったのですが、医師会としては最先端で既得権益にマイナスとなる面にはネガティブなところがあるのでしょうか? 社長も医師ですが、そちらについてはどのように考えていますか?
上野:不眠症治療用アプリに対して、特別ネガティブなところはないと思っています。
「睡眠薬の多剤処方や長期使用することはよくない」というご認識は、開業医の先生方も含めてみなさまお持ちだと思います。大量の睡眠薬をずっと投与していてもまったく問題ないという時代は、さすがにもう終わっていると思います。
しかし、ヨーロッパ睡眠学会が出したガイドラインなどを見ると、デジタルを含めた認知行動療法が第一選択で、睡眠薬による治療はその後と明記されており、日本が相対的に取り残されているのは事実です。世界的にはこのような流れがすでにできており、日本でも「睡眠薬を減らしましょう」という合意がされています。今後は、睡眠薬の利用低減を実現するための手段の1つとして治療用アプリを使用することへの合意形成を、日本では時間をかけて行っていく必要があると思っています。
不眠症の課題自体はみなさまに認識されてきていることから、それを解決する手段としてデジタルを使うところに対して時間をかけるのが大切だと認識しています。
質問者:総論ではみなさまが賛成でも、不眠症の治療薬を処方している現実的な医師にはやはり開業医が多いというのは間違いないですか?
上野:不眠症は患者数も多いため、診ているのはやはり開業医の先生方が非常に多いです。不眠症治療用アプリがすでに活用されているヨーロッパとは異なり、現実的なその他の治療手段がないため、ほとんどが睡眠薬で治療されている現状は事実かと思います。
質疑応答:株主や機関投資家への説明機会について
質問者:御社のパイプラインを見て、治験の最終段階でプライマリーによい結果が出たとしても、保険収載の状況が不透明であれば我々としてもなかなか投資しづらいのが正直なところです。
一方で、一昨日の中医協の資料を見ると、当局が何をしたいのかも正直わかりません。当局との関係性もあるので言えない部分もあると思いますが、もう少しクイックに状況をアップデートし、説明してもらえる機会を作っていただけませんか?
上野:プログラム医療機器の評価について、ご指摘いただいた不透明なところは私たちも課題だと思っていますし、実際に壁にぶつかっているところでもあります。厚生労働省内のワーキンググループでも、業界全体の課題・問題点として指摘されており、弊社もその一例として、改善を主張していかないといけないと考えています。
弊社としては、可能な範囲で、株主や投資家のみなさまに丁寧に情報発信を行っていきたいと考えています。
質疑応答:今後の保険収載における当局間との議論について
質問者:我々が想定しうる最悪のシナリオは「保険収載できない」ことだと思いますが、当局とのコミュニケーションの中でこちらを匂わせるコメントは聞いていますか? 単に規制や保険収載の細目が変わるという制度に振り回されただけだと素直に受け止めてよいのでしょうか?
当局と前向きに議論をしているのかどうかや、何らかの課題があるのかどうかなどを確認させてください。
上野:不眠症治療用アプリが保険収載できないという話はまったく聞いていません。不眠症治療用アプリが薬事承認を受けている点は変わらない事実です。一方で、今回の診療報酬改定における判断については、技術料を準用するという枠組みの中で、別途適応拡大を希望されていた認知行動療法が、このタイミングで認められなかったことの影響だと思っています。
令和6年度の制度改正では、プログラム医療機器は特定保険医療材料として評価すると示されていますし、弊社としては、当然ながら保険収載できるものと考えて厚生労働省とも話を進めている状況です。
質疑応答:不眠症治療用アプリの発売遅延による他パイプラインへの影響について
質問者:不眠症治療用アプリについて、いったん保険適用申請を取り下げて再度申請し直すとしても、当初の計画からは1年から2年ほど販売時期が遅れる可能性があると思っています。
その中で、来年は2つほどのパイプラインが検証ステージに入りそうですが、こちらは目先の売上が立たないため少し遅らせますか? それは別として、多少赤字を拡大させても通常どおり進めていく予定ですか? 来期の収益にかなり関わってきますので、スピード感など現状の考え方を教えてください。
上野:後続のパイプラインの開発計画自体を、不眠症治療用アプリの上市タイミングのずれを理由に変えるつもりはありません。これらのパイプラインを早期に開発することが次の収益の矢になると考えています。不眠症治療用アプリの収益発生が少し遅れたとしても、これらのパイプラインの開発をできる限り早く進めるべきだと考えていますし、財務状況を考慮してもそれが可能な状況にあると思っています。
質問者:来期中に不眠症治療用アプリが認可されなければ、研究開発費が増えることで少し赤字が拡大する可能性はあるという認識でよいでしょうか?
上野:おっしゃるとおり、後続のパイプラインが進んだ分の研究開発費が増えると思います。
新着ログ
「情報・通信業」のログ





