テラ株式会社 2018年12月期決算説明会
テラ、通期は赤字で着地 細胞医療事業での大幅減収に加え、子会社の連結除外等が影響
あらためて、当社のCore Competence

遊佐精一氏(以下、遊佐):代表取締役社長の遊佐精一でございます。2018年12月期のテラ株式会社決算概況について説明させていただきます。
本日の内容は3つです。1つ目が2018年12月期の進捗状況、2つ目が2018年12月期の決算概況、最後に2019年12月期以降の経営課題について説明いたします。まず、2018年12月期進捗状況につきまして、私から説明させていただきます。
最初に、あらためて、当社の強みについてお伝えします。当社は、2004年の創立以来 、樹状細胞ワクチン療法を中心に、がん免疫療法の研究開発を続けてまいりました。
当社の強みは、少なくとも3つございます。樹状細胞というものは、製造工程が非常に難しく、間違えると、逆に免疫を抑制してしまうことがあります。当社の樹状細胞は、がんに対して非常に効果が期待されると考えております。
また、樹状細胞に覚え込ませるがんの特徴を抗原ペプチドと呼んでおりますが、これついては大阪大学あるいは北海道大学で開発されたものを使用しております。当社だけが、独占的に使うことが可能になっております。
また、当社はこれまでに1万症例以上の治療実績があります。 この治療実績を、欧米論文で発表してきました。その結果、日本国内だけでなく、 海外からの知名度も上がってきています。
当社のビジョン・ミッション
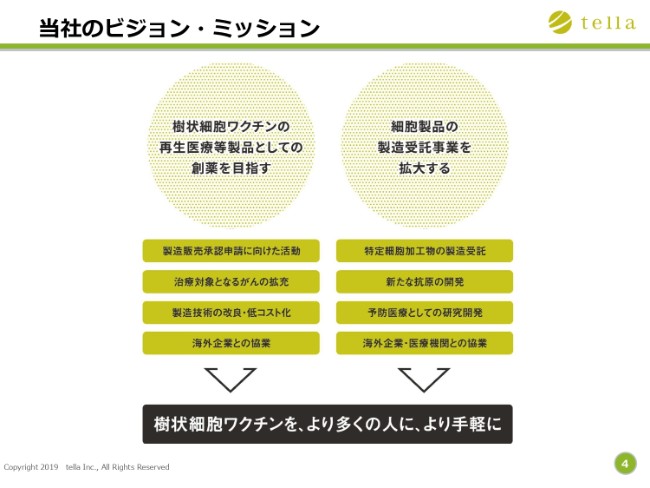
当社のミッションです。 樹状細胞ワクチンを、より多くの人に、より手軽に届けていきたいと考えております。 そのためにも、樹状細胞ワクチンの創薬、そして製造受託事業で樹状細胞を届けるという2点に、選択と集中をしていきたいと考えております。
2018年12月期トピックス

本日のトピックスです。1つ目は和歌山県立医科大学の治験の進捗、2つ目は台湾への技術移転、3つ目は細胞加工受託業の進捗です。
治験の概要

まず、1つ目のトピックです。和歌山県立医科大学での治験の概要について、簡単にご説明いたします。
対象は、膵臓がんの標準治療、一次治療が効かなくなった患者さんです。評価項目は、どれぐらい(の期間)生存されたかというところで見てまいります。目標症例数は185症例で、期間は2021年9月末頃あるいは12月末頃までに終了する見込みです。
TOPIC 1 和歌山治験、有効性検証へ①
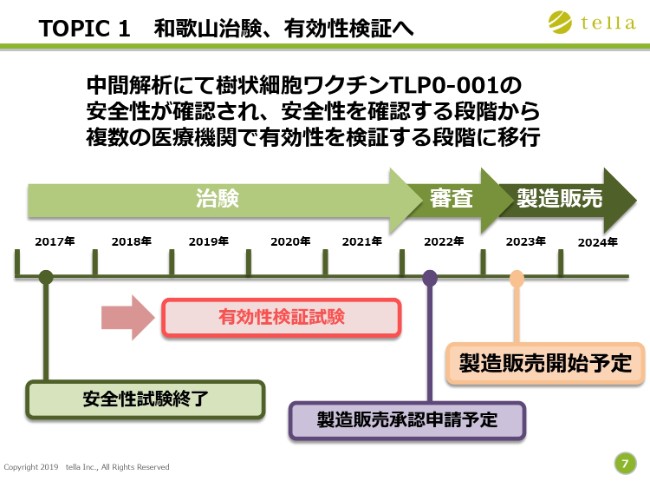
昨年(2018年)12月末に発表したように、中間解析にて(樹状細胞ワクチンの)安全性が確認され、安全性を確認する段階から、複数の医療機関で有効性を検証する段階へと移行いたしました。治験は順調に進んでおります。
TOPIC 1 和歌山治験、有効性検証へ②
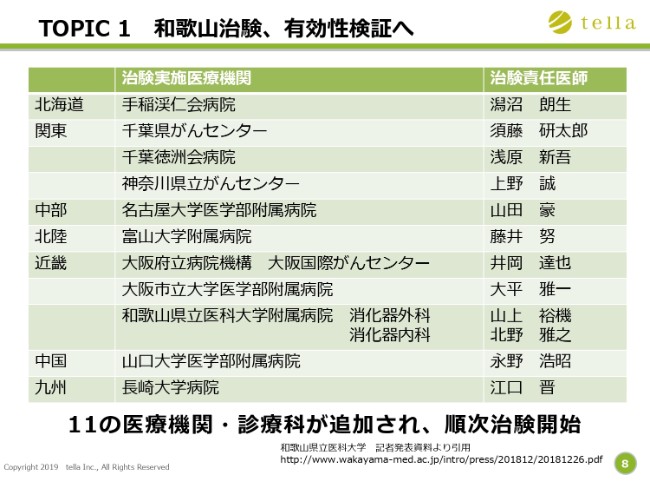
(治験の)参加医療機関に関する情報です。北は北海道、南は九州まで、11の医療機関、12の診療科が参加される予定です。今後も、参加される医療機関数が増える可能性がございます。
TOPIC 1 和歌山治験、有効性検証へ③
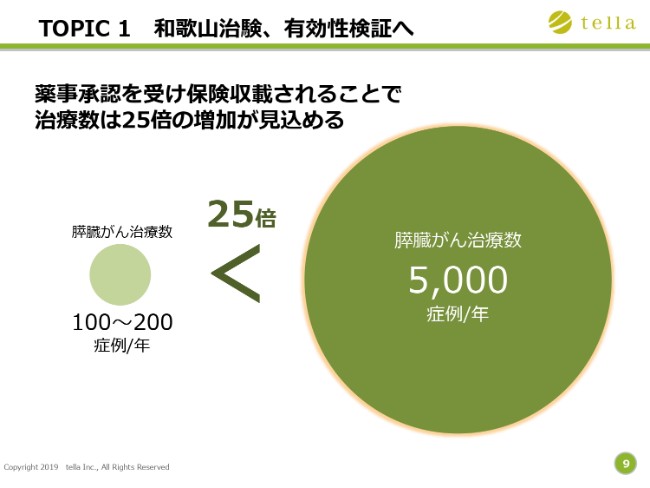
(膵臓がん治療の想定)マーケットについてです。現在、当社は膵臓がんに対して、年間100~200症例の(治療数)実績があります。薬事承認後は、保険収載されることで治療数が25倍になると見込んでおり、年間およそ5,000症例になると考えております。
TOPIC 1 和歌山治験、有効性検証へ④
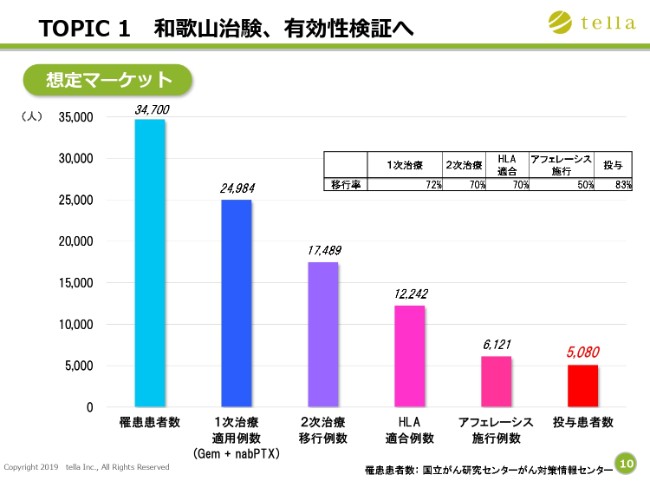
その算定根拠です。膵臓がんの患者さんは、年間で3万人を超えます。その中で、二次治療に移行する患者さんが約1万7,000人。そのうち、遺伝子(HLA)型が一致すること、そしてアフェレーシスと呼ばれる(血液浄化療法の)施行が可能であるという条件を満たした患者さんは、最終的に5,000症例ほどになると見込んでおります。
TOPIC 2 台湾への技術移転が成功①

2つ目のトピックとして、台湾への技術移転が成功したことを説明させていただきます。2018年9月10日に発表させていただきましたが、Vectorite Biomedical社と業務提携契約を締結いたしました。
台湾では、再生・細胞医療に関心が高く、それを推進するための法整備や規制緩和が強力に進められています。2018年9月、リスクが低い一部の細胞医療が医療機関で提供可能になりました。当社の樹状細胞も、このリスクが低い一部の細胞医療に該当いたします。
Vectorite Biomedical社は、当社と同様に2004年の創立で、Taipei Exchangeに上場しています。また、バンキング事業で収益を伸ばしていた企業で、細胞の保存に強みを持っています。一方で、当社は細胞を加工する方に強みを持っていますので、両者のシナジーが期待されます。
TOPIC 2 台湾への技術移転が成功②

台湾の(がん治療)マーケットについてです。台湾の人口は、日本のおよそ6分の1にあたる2,357万人です。台湾の教育水準は高く、健康に対する意識も非常に高いという報告があります。がんは36年連続で死因のトップ。2017年のがんによる死亡数は、過去最多の4万8,037人で、(部位別では)肺がんが1位となっています。
台湾は日本と比較すると人口は少ないですが、実は中国等からの患者さんが多く来られます。台湾としても、医療ツーリズムに注力しています。2017年の医療インバウンド実績は30万人以上で、マーケットは635億円に相当すると考えています。
TOPIC 2 台湾への技術移転が成功③

2019年2月19日に発表いたしましたとおり、Vectorite Biomedical社が当社の技術を用いたがん治療用細胞の加工を開始いたしました。Vectorite Biomedical社は、同社の提携する台湾内の医療機関に対して、細胞製品を納入いたします。Vectorite Biomedical社での細胞加工実施件数に応じたロイヤリティが当社に支払われるというビジネスモデルです。
TOPIC 3 細胞加工受託業の進捗①

3つ目のトピックです。細胞加工受託業の進捗を報告いたします。お伝えてしておりますとおり、関西圏で自社の細胞培養加工施設を整備中ですが、2018年7月に厚生局に特定細胞加工物製造の許可申請を行いました。一般的には、許可申請を行ってから6ヶ月で承認が下りるといわれているので、もうそろそろだと考えております。
細胞加工受託業の新しいビジネスモデルのメリットは、医療機関としては、医療機関における細胞加工施設の設置・維持が不要になり、培養スタッフの雇用も不要になることです。当社といたしましては、初期投資・維持コストを削減でき、提携先の拡大ができると考えております。
TOPIC 3 細胞加工受託業の進捗②
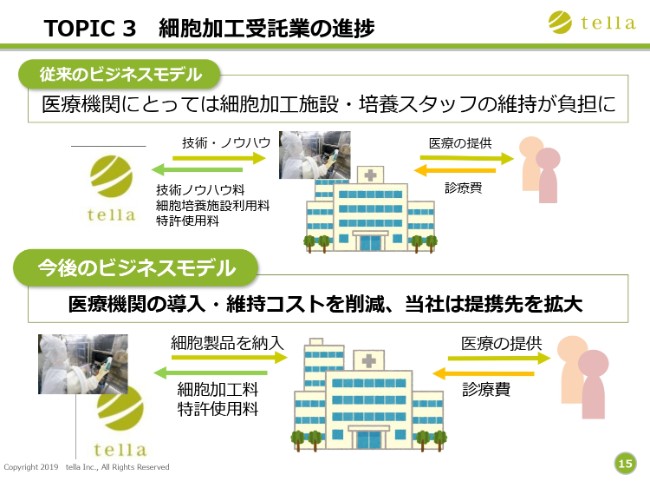
医療機関にとっては、細胞加工施設や培養スタッフを維持する必要がなくなりますので、免疫細胞療法への参入障壁が低くなります。それにより、当社は提携先を拡大していきたいと考えています。
TOPIC 3 細胞加工受託業の進捗③

昨日(2018年2月27日)発表させていただきましたが、学校法人慶應義塾より、TIL(腫瘍浸潤Tリンパ球)と呼ばれるリンパ球の製造を受託開始いたしました。このように、今後は大学あるいは企業等からの細胞製造を受託し、販路を拡大していきたいと考えております。
2018年12月期 損益概要(連結)
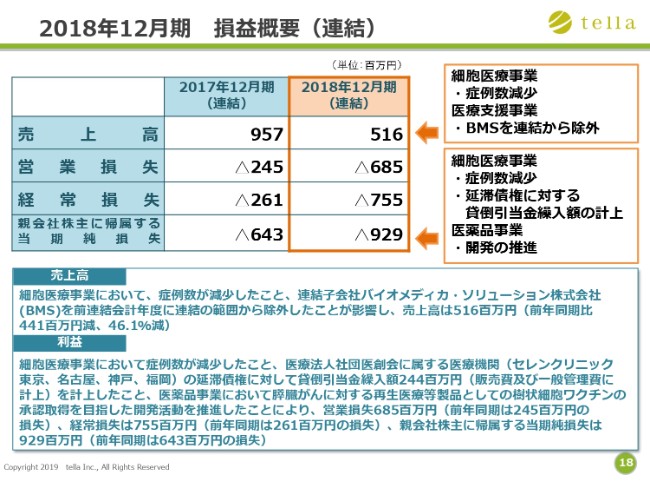
吉田光氏(以下、吉田):経理財務部の吉田でございます。2018年12月期の決算概況を説明いたします。連結損益の概要ですが、売上高は5億1,600万円で、前年同期比で4億4,100万円の減少です。各段階利益においては、営業損失が6億8,500万円、親会社株主に帰属する当期純損失が9億2,900万円です。
第三者機関の設置による調査費用、および2015年12月期から2017年12月期の有価証券報告書の訂正に対する監査費用が確定したため、特別損失に特別調査費として1億6,200万円を計上しております。
売上高および利益面の減少要因に関しては、次のセグメント別の損益概要でご説明いたします。
2018年12月期 損益概要(セグメント別)①
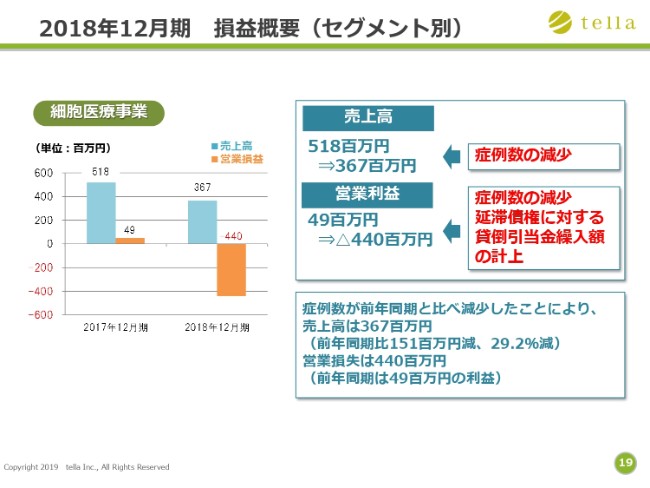
はじめに、細胞医療事業です。売上高は3億6,700万円で、前年に比べて1億5,100万円の減少となりました。原因は、症例数の減少によるものです。
営業損失は4億4,000万円です。前年同期の4,900万円から、大幅に減少いたしました。原因は、症例数の減少により売上高が減ったこと、また、医療法人社団医創会に属する医療機関の延滞債権に対して、貸倒引当金繰入額を2億4,400万円計上したことによるものです。
細胞医療事業における収益の回復に関しては、この後、遊佐から2019年12月期以降の経営課題のパートで説明がございます。
2018年12月期 損益概要(セグメント別)②
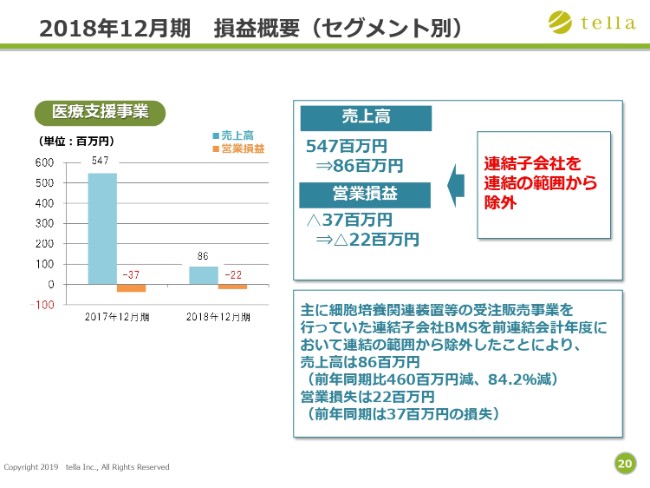
次に医療支援事業です。売上高は8,600万円で、前年同期から4億6,000万円の減少です。原因は、2017年12月期第3四半期において、連結子会社社バイオメディカ・ソリューション株式会社の株式を売却し、連結の範囲から除外したことです。営業損失は2,200万円です。
2018年12月期 損益概要(セグメント別)③
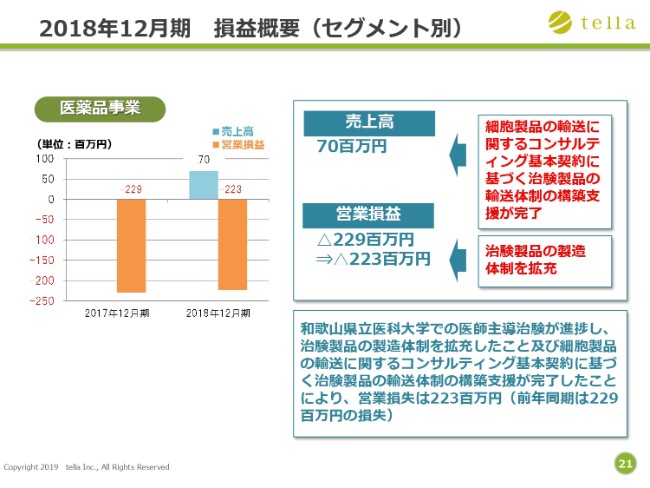
セグメントの最後は医薬品事業です。2018年12月期において、売上高7,000万円を計上しております。これは、細胞製品の輸送に関するコンサルティング基本契約に基づき、治験製品の輸送体制の構築支援を実施し、完了したことによるものです。
営業損失は2億2,300万円です。前年同期は2億2,900万円の損失でした。営業損失は前年同期とほぼ同額になりますが、2018年12月期の売上高を考慮に入れると、2018年12月期の和歌山県立医科大学の医師主導治験の開発費用は約3億円です。前年同期は2億3,000万円でした。
この開発費用の増加は、和歌山県立医科大学の医師主導治験の安全性試験が本格化し、完了したことが要因です。先ほど説明があったように、治験は安全性試験が2018年12月末に終了し、現在、有効性検証試験に移行しております。
以上が、連結損益およびセグメント別の損益概要です。
貸借対照表(連結)
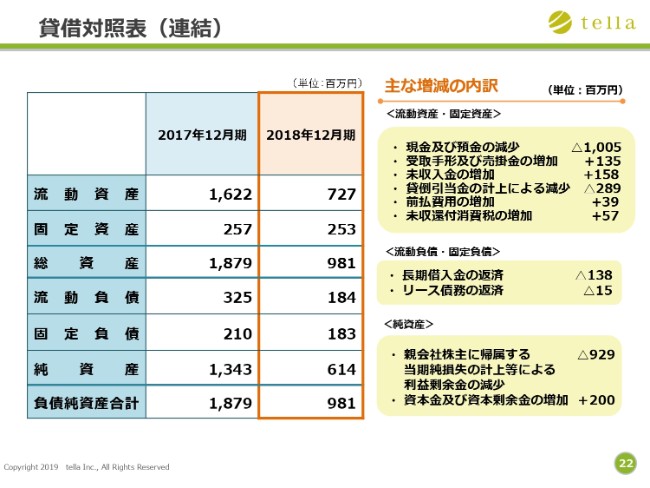
連結貸借対照表の説明に入ります。総資産額は、前連結会計年度末から8億9,800万円減少して、9億8,100万円となりました。減少の主な要因は、現金および預金が10億500万円減少したことです。総負債額は前連結会計年度末から1億6,800万円減少し、3億6,700万円となりました。
純資産額は、前連結会計年度末から7億2,900万円減少し、6億1,400万円となりました。純資産額の減少要因は、第三者割当で資本金および資本剰余金がそれぞれ1億円増加したものの、親会社株主に帰属する当期純損失で9億2,900万円を計上したためです。増減の詳細については、スライド内の「主な増減の内訳」をご確認ください。
キャッシュフロー計算書(連結)
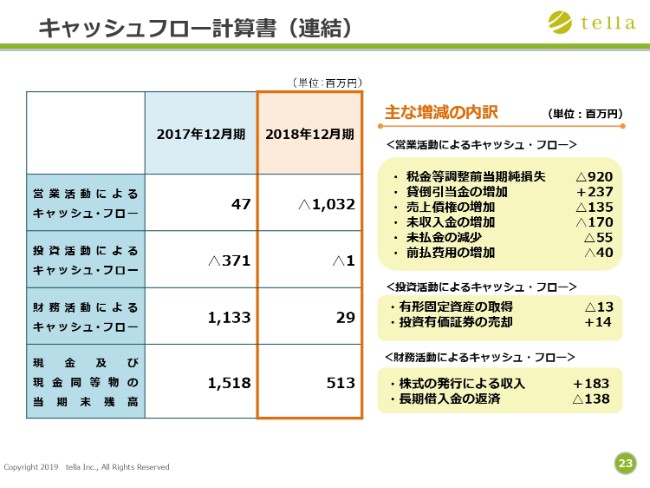
連結キャッシュフロー計算書の説明をいたします。現金および現金同等物は、前連結会計年度の15億1,800万円から10億500万円減少して、5億1,300万円となりました。営業活動によるキャッシュフローで10億3,200万円の減少が生じたことが要因です。
各キャッシュフローの増減に関しては、スライド内の「主な増減の内訳」をご確認ください。以上で、2018年12月期の決算概況の説明を終わります。
2019年12月期 通期業績予想(連結)
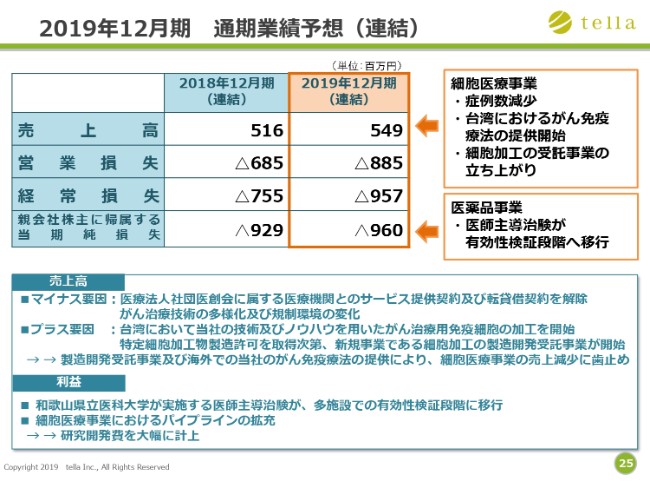
遊佐:それでは、2019年12月期以降の経営課題について説明させていただきます。まず、2019年12月期通期業績予想です。
主要な収益源が、これまでのノウハウ提供モデルから、細胞を製造して提供するというモデルに替わります。今年度はその移行期であるために、著しい売上増は期待できませんが、現状維持を目指していきたいと考えています。(売上高の通期予想は)およそ5億4,900万円です。
2019年12月期以降の経営課題

2019年12月期以降の経営課題として、4つ挙げております。1つ目は創薬のための資金獲得、2つ目は細胞医療事業における収益回復、3つ目は治験パイプラインの拡充、そして4つ目がガバナンス体制の強化です。
課題1 創薬のための資金獲得

1つ目の課題です。樹状細胞ワクチンの再生医療等製品としての創薬は、当社の使命であると考えております。よって、資金獲得は必須と考えており、新たなエクイティファイナンスの実行を、現在検討しております。また、台湾のVectorite Biomedical社のように、企業とのアライアンスによる開発協力金等の獲得も目指してまいります。
課題2 細胞医療事業における収益回復①
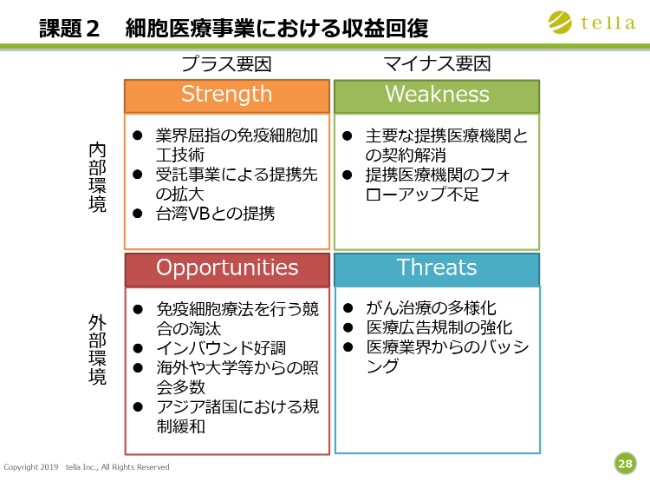
(2つ目の課題である)細胞医療事業における収益回復のマイナス要因としては、主要な提携医療機関との契約解消があります。また、免疫チェックポイント阻害薬にみられますように、がん治療の多様化、そして(医療広告)規制の強化が考えられます。
一方、当社の強みは、免疫細胞加工技術にあります。受託事業による提携先の拡大、また、台湾のVectorite Biomedical社のように、海外での提携を進め、海外市場を開拓していくといったことで、収益の回復を目指してまいります。
課題2 細胞医療事業における収益回復②

日本国内では、(医療広告)規制が強化され、適切な運用をしていなかった医療機関等が淘汰されているということもあります。
日本国内の患者さんは減少しているのですが、海外からのインバウンドの患者さんは逆に増加しております。そして、アジア諸国において規制緩和が進められていますので、これらは当社にとって追い風になると考えております。
細胞医療事業では、国内の自由診療市場は横ばいということをお話ししていますが、インバウンド患者を対象としたニーズは好調ということで、インバウンドに強い医療機関との提携強化・新規提携を行ってまいります。
課題2 細胞医療事業における収益回復③
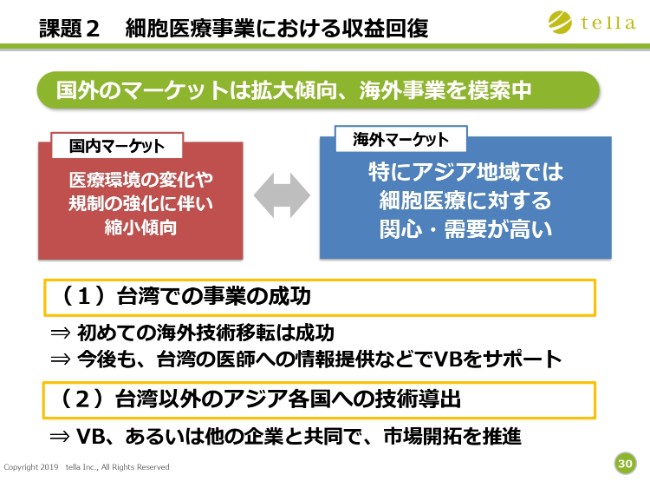
海外で規制緩和が進められており、とくにアジア地域では、細胞医療に対する関心・需要が高くなっています。今回、台湾での事業が成功したことを受け、今後、例えばVectorite Biomedical社と、台湾以外のアジア各国へ技術導出を行っていくことも検討しております。
特に、シンガポール・台湾・日本は医療が信用されていますので、(Vectorite Biomedical社と)一緒にほかのアジアの国々へ技術導出を行っていくことは、(成長の)可能性があると考えています。
課題3 パイプラインの拡充
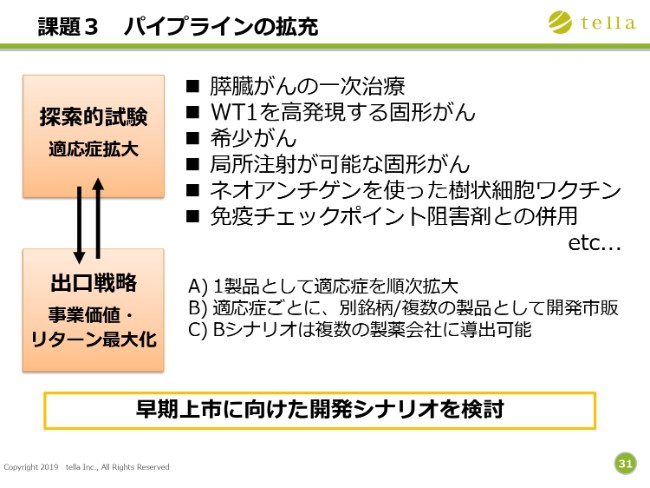
3つ目の課題は、治験パイプラインの拡充です。現在、和歌山県立医科大学では、膵臓がんの二次治療が対象となっていますが、今後は一次治療についても検討していかなければならないと考えています。
また、希少がん、がん抗原のいらない局所注射、そして新しい技術ネオアンチゲン、また、免疫チェックポイント阻害剤との併用を検討しております。当社は、樹状細胞を、より手軽に提供していくことを考えていますので、早期上市に向けた開発シナリオを進めていきたいと考えています。
課題4 ガバナンス体制の強化

4つ目の課題は、ガバナンス体制の強化です。昨年(2018年)に第三者委員会が発足されたことを受けて、ステークホルダーのみなさまには大変ご心配をおかけしております。ガバナンス体制の強化も重要な課題の1つであると、当社も受け取っています。ここ(スライド)に記載されていることは一部ではございますが、粛々と進めてまいります。
一連の問題における責任の所在の明確化として、代表取締役の解職決議を行いました。また、ガバナンス体制強化のために、情報共有による取締役会での議論の活発化を行っています。
社内規定・手続きの見直し、徹底としては、文書承認ルール等の改定を行っております。さらに、役職員のコンプライアンス意識の醸成・向上のために研修も実施しております。また、内部通報制度の周知徹底も行っております。そして、医療法人との取引の見直しをしております。
社内でダブルチェックできる体制にすることや、情報共有をより活発に強化することで、二度と同じ過ちを犯さないように努力してまいりますので、今後ともご支援をよろしくお願いいたします。ありがとうございました。
新着ログ
「サービス業」のログ