ログミーFinance 第23回 個人投資家向けIRセミナー Zoom ウェビナー 第2部・株式会社ファンペップ
ファンペップ、機能性ペプチド技術による豊富な開発パイプラインを強みに、開発意義の高い製品を創出
INDEX

三好稔美氏(以下、三好):よろしくお願いいたします。それでは、株式会社ファンペップの事業概要についてご説明します。今日のインデックスです。まず最初に、医薬品開発の動向をご説明します。
2番目に会社の概要、3番目にトピックスとして皮膚潰瘍治療薬「SR-0379」の概要、4番目に成長戦略、5番目にパイプラインの開発計画についてご説明します。
医薬品研究開発の生産性①
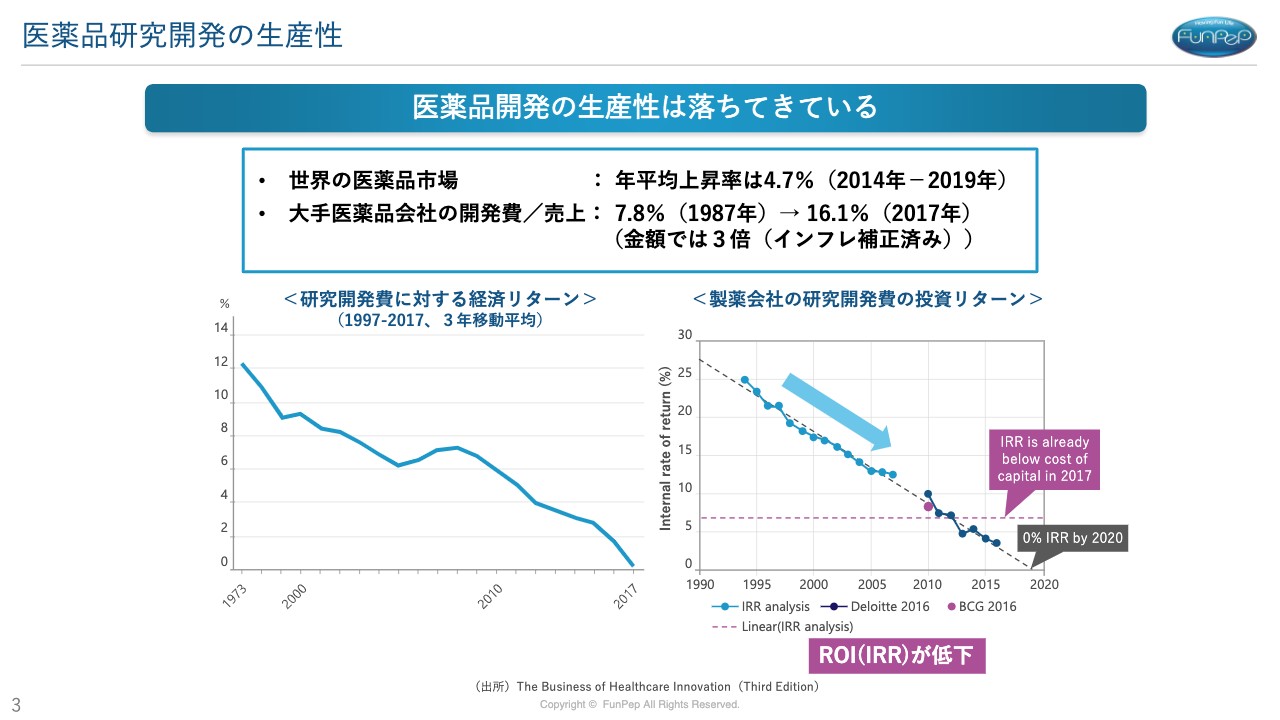
三好:医薬品開発の動向についてです。医薬品開発の生産性が落ちていることに関してご説明します。世界の医薬品市場ですが、年平均上昇率は2014年から2019年の間で4.7パーセントになっています。
日本においては薬価の抑制などによってそれほど上昇率が上がっていませんが、世界的に見ると医薬品の売上はどんどん上がっているという状況になっています。
一方で、大手医薬品会社の売上に対する開発費の割合は、1987年で7.8パーセントでしたが、2017年になると16.1パーセントに上がっています。金額では開発費用が3倍になっていることになります。
これが何を意味しているかと言いますと、医薬品の売上が上がっているにも関わらず、開発費がより多く上がっているために、売上に対する開発費用の割合が上がっているということです。これをグラフ化したものをスライドに載せています。
「研究開発費に対する経済的リターン」とは売上のリターンのことですが、どんどん下がってきていることが見て取れます。ここで言いたいことは、「医薬品の研究開発の生産性が落ちてきている」ということです。
医薬品研究開発の生産性②
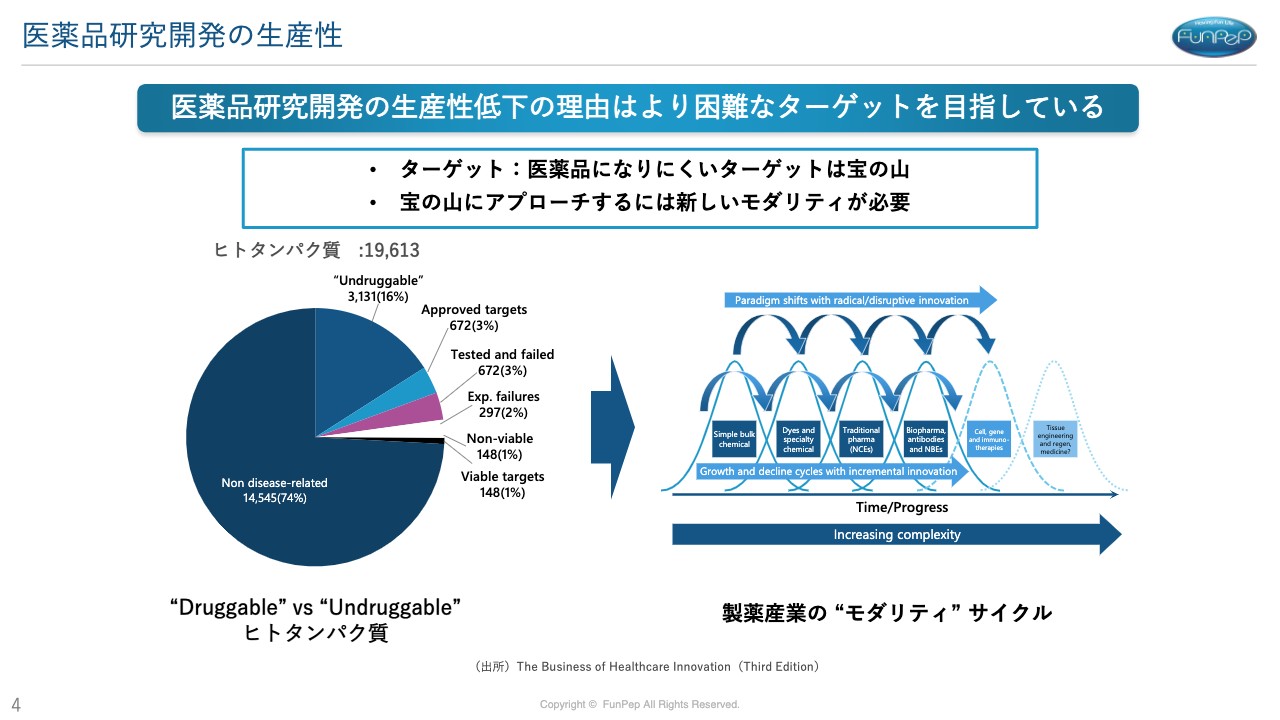
三好:そのようなことが起きている理由をご説明します。スライド左側の「”Druggable” vs “Undruggable”」と記載されている円グラフをご覧ください。生体の仕組みがこれまでもずっと研究されてきています。
体の中のタンパク質などで、病気に関係していないタンパク質などが74パーセントあります。ほとんどが栄養素になっているところです。残り4分の1くらいは、病気の原因になり得るターゲットと言いますか、そのような体の成分になっています。
この4分の1の分野の中で、薬になってきているところはまだ少ないのが現状です。薬としての開発余地があるところは「Undruggable」のところで16パーセントです。
製薬会社としてはまだ未知と言いますか、薬になっていないターゲットをどんどん見つけていかないといけません。しかし、体の仕組みもですが、研究開発でここまでどんどんターゲットを見つけてきたという流れの中で、「Undruggable」という薬になりにくいターゲットの研究開発をもっと進めていかない限り、新薬を生み出せない状況になってきているということです。
スライド右側に製薬会社のモダリティサイクルを記載しています。治療の様式ということですが、こちらはどんどん新しい領域が開発されてきています。
以前は化学合成品や天然素材などが主でしたが、抗体医薬品など生物学的な医薬品になったり、遺伝子治療などを用いて薬になりにくかった部分を攻めようとしています。
医薬品研究開発の生産性③
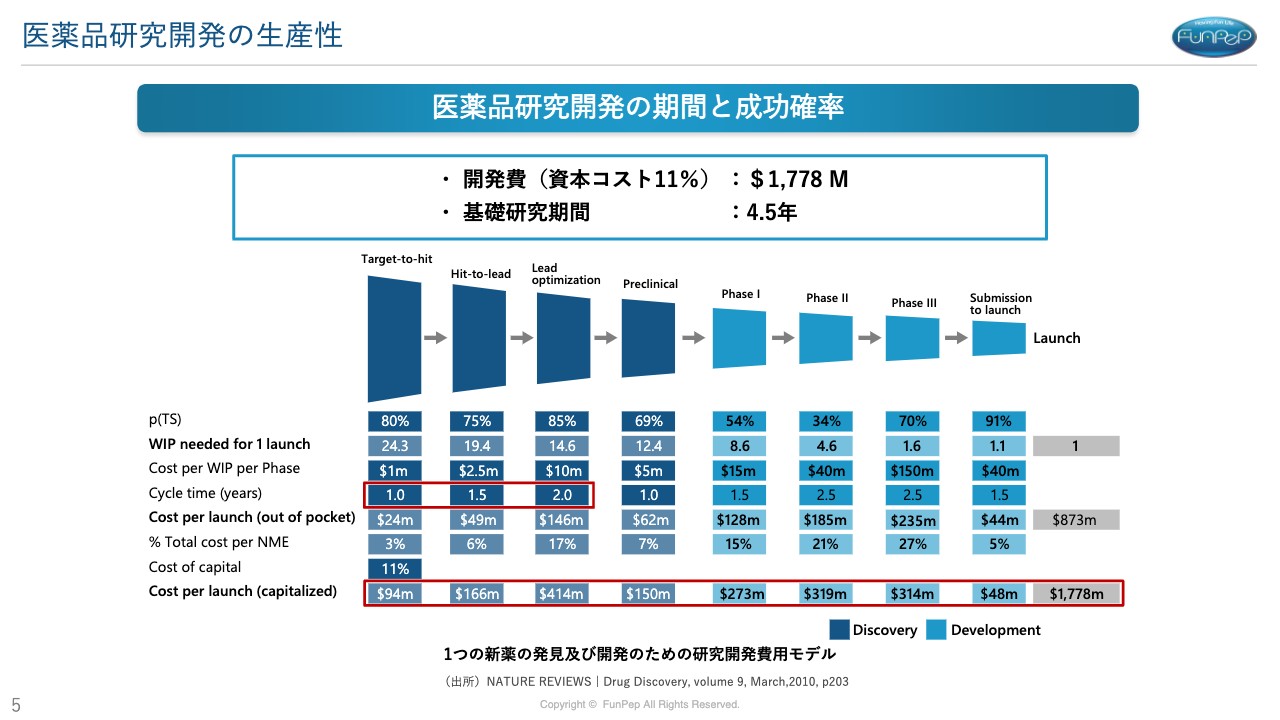
三好:研究開発のモデルです。医薬品開発はもともと成功確率が非常に低く、リスクの高い事業になっています。スライドに記載の資料は2010年の少し古いデータですが、アメリカの大手製薬会社をベンチマークとしています。
スライド下部に記載のとおり、世の中に医薬品が出るまでのコストがどれくらいかかるのかを表しています。
2010年の段階ですが、1,778ミリオンドルとなっています。100円換算でも1,800億円くらいの費用がかかるかたちです。ここでは資本コストが11パーセントほどですので、実際には873億円ほどかかっています。
もう1つ注目していただきたいところは、図の一番上に記載している開発の流れです。まず、「病気の原因となるものを抑制するため、そのような化合物を見つけていこう」というところから非臨床試験に入ります。
その後、「PhaseⅠ」「PhaseⅡ」「PhaseⅢ」となりますが、こちらは臨床試験ということで、ヒトでの試験になります。
ここで注目したいところが、サイクルタイム(Cycle time)です。医薬品の候補化合物を見つけようとする期間は4.5年となっています。論文やニュースなどでも、医薬品の候補化合物を見つけるには3年から5年くらいかかると言われています。大手の製薬会社でもこれほどの時間がかかるということです。
坂本慎太郎氏(以下、坂本):質問させていただきます。開発費用がすごく高いというお話を細分化して教えていただいていますが、このもともとの理由は何でしょうか? 化合物で薬ができなくなってきた、人件費がかかるようになった、審査が厳しくなったなど、いろいろあると思いますが、そのあたりを教えてください。
三好:今の段階でも、世の中には医薬品がたくさんあります。ですので、風邪を引いた時などの薬に関してはこれ以上開発する必要がないというくらいの量の薬が世の中に出ているのです。
今はがんなどの病気に対してもよい薬がどんどん開発されていますが、「アンメット・メディカル・ニーズ」という、十分な医療が行き届いていない疾患がまだ残されています。
このような疾患は、治療法を開発するのが非常に難しいところがあります。ですので、開発費用がどんどん上がってきているのです。しかし、開発でかかった費用に対してリターンを得なければいけません。
株式会社は当然利益を追求しなければいけないため、そのバランスを考えた上で「この疾患であればこれだけのコストをかけても売上としてペイできるぞ」といった品目について、開発がどんどん進んでいるという状況です。
もう1つは、先ほどお伝えしたとおり、簡単に開発できるものがどんどん少なくなってきていることも挙げられると思います。
医薬品研究開発の生産性④

三好:ここまででご説明したことのまとめです。製薬業界の生産性の状況ですが、市場はどんどん拡大しています。少子高齢化も関係しているのかもしれません。しかし、研究開発費用はより増大しているということで、医薬品開発の生産性は低下傾向にあります。
低下傾向の理由としては、1つは医薬品化が困難な新規のターゲットにアプローチしていかないといけないことが挙げられます。遺伝子治療など、新しいモダリティにアプローチしていかないといけないということです。
もう1つは、高額な新モダリティを応用して使うにあたって、開発費用がどんどん上がっていってきていることです。基本的にはその2つの理由から、生産性が落ちていると思っています。
しかし、我々はこれらの状況を解決できるのではないか考えています。理由としては、既知のターゲットを攻めていくため、新しいターゲットを見つける必要がないということです。「ここの病気の原因を抑えれば病気を治すことができるんだ」ということがわかっているのです。
「じゃあ開発する必要がないのではないか」と思われるかもしれませんが、我々としては世界中の人たちにより安価に薬を提供するという課題を、イノベーションというかたちで解決していこうと考えています。
会社概要 ― 会社概要

三好:会社の概要についてご説明します。当社は大阪大学大学院医学系研究科の機能性ペプチドの研究成果を実用化する目的で、2013年に設立しました。事業所ですが、バックオフィスは東京にあります。大阪大学発祥ということもあり、研究開発は大阪の千里リサーチセンターで行っています。
従業員数はまだ少なくて、12名です。そのうち、研究開発部員が7名となっています。昨年上場することができましたので、研究開発部員についてはどんどん採用していく方向で動いています。
スライド下部に、簡単な沿革を記載しています。当社は2013年に「よい機能性ペプチドがあるんだけど」という大阪大学の研究成果の紹介を受けた時に設立しました。その時は、機能性ペプチドは化粧品や医療機器、医薬品として応用できるということで、この3つの分野について進めていこうと考えていました。
2015年には大阪大学などが持っていた機能性ペプチド関連のライセンスを我々が取得して、医薬品の開発を本格的に開始しました。その後は順調に進み、2018年に皮膚潰瘍の治療薬「SR-0379」について臨床試験のフェーズⅡを開始しました。
2019年には抗体を誘導できるペプチド「FPP003」が臨床試験に入り、2020年には東証マザーズに上場できました。
会社概要 ― ビジネスモデル
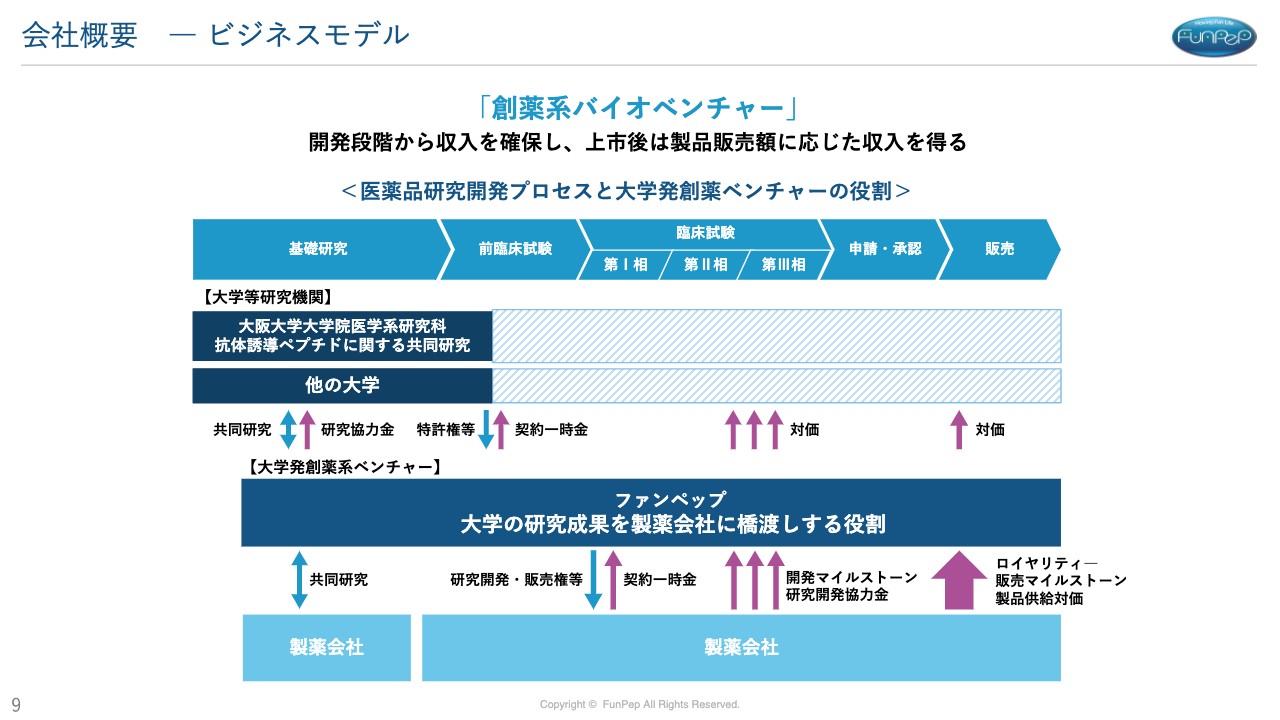
三好:ビジネスモデルについてです。主に創薬系バイオベンチャーのビジネスモデルと同様です。大阪大学とアカデミアとの共同研究や製薬会社との共同研究を通じて、我々の技術で医薬品の候補化合物を見つけていくことが中心です。
医薬品候補化合物を見つけたあと、我々が前臨床試験で動物での効果確認や、安全性の確認を行います。その後、臨床試験として第Ⅰ相でヒトでの安全性を確認し、臨床試験の第Ⅱ相の前半部分でヒトへの効果があるかを確認しています。
第Ⅱ相試験の後半部分や第Ⅲ相試験は非常に費用がかかるところですので、このあたりから製薬会社に候補化合物の開発を受け継いでいただく流れになります。その後、製薬会社が承認申請、販売を行います。
我々の収益ですが、製薬会社に我々の研究成果をすべて預けてライセンスしていきますので、その契約にあたっての契約一時金や、研究がどんどん進んだ際の成果に対する開発のマイルストーンのフィー、販売後のロイヤリティが収入源になります。
坂本:いくつかご質問させていただきます。研究開発型の医薬品の開発ベンチャーということで、開発費がかかるということはわかりました。これからご説明があると思いますが、この開発はきちんと進んでいるのでしょうか?
また、開発期間が想定より長期化した場合、研究費についてはある程度パイプがつながっている製薬会社からサポートがあると考えてよいのでしょうか?
三好:我々からすると開発については計画どおり順調に進んでいる状況です。後ほどパイプラインの開発計画の中でもご説明しますが、臨床試験は医療機関で行われます。
医療機関が新型コロナウイルスで逼迫しているという状況は世界各国で起こっているため、我々だけではなく製薬会社などでも臨床試験が想定より遅れてるという状況が起こっています。
ただし、先ほどお伝えしたとおり、我々は比較的大きな臨床試験ではなく、第Ⅰ相、第Ⅱ相の期間もそれほどかからない臨床試験を行います。ですので、我々の中で開発が遅れたり、開発費用が遅れたことで費用が増えていくという影響はそれほど出ていません。
会社概要 ― 技術概要
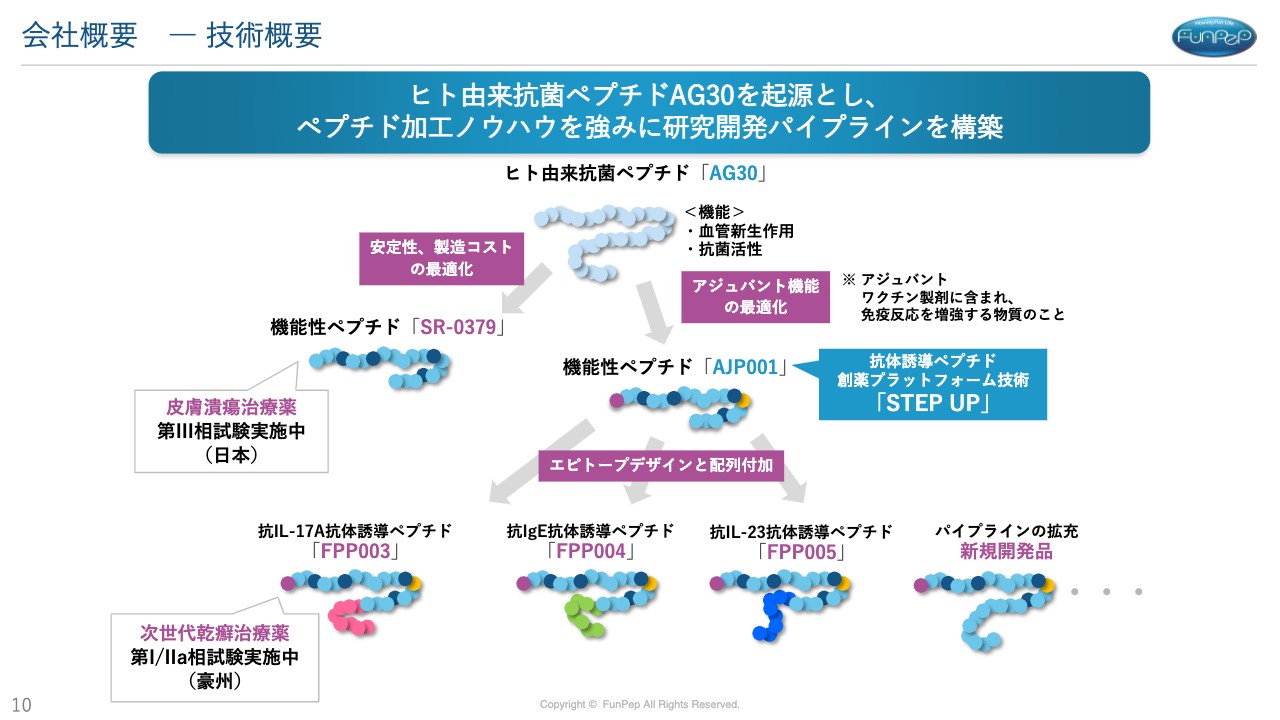
三好:我々の技術の概要です。出発は「AG30」というペプチドで、大阪大学で生み出されました。30個のアミノ酸から成る「AG30」は、新しく血管を作り出す作用と抗菌活性という菌を殺す作用があります。
しかし、30個のアミノ酸を医薬品にするためには合成費用がかかります。そのため、より製造コストを下げ、安定性を向上させるために最適化を行い、ペプチド自体を改良してきました。そこで見出されたのが20個のアミノ酸から成る「SR-0379」です。
こちらは「AG30」と同様に血管新生作用と抗菌活性を併せ持っています。この作用メカニズムは皮膚潰瘍の治療薬として最適だろうということで開発を進めました。現在、第Ⅲ相試験ということで、ヒトでの臨床試験の最終段階に進んでいる状況です。
また、最初にお伝えしたとおり、ペプチドは化粧品分野や医療機器分野にも応用できるのではないかということで、「AG30」からいろいろなペプチドを作っては「これは薬にならないね」「化粧品にならないね」とスクリーニングしてきました。
そこで、20個のアミノ酸から成る「AJP001」が見つかりました。化粧品分野で開発するために作用と副作用などを考えていましたが、「AJP001」には免疫活性があるため、これを投与すると皮膚が赤くなるなどの作用が出てきてしまいました。
これでは化粧品などでは当然使えないため、本当は捨ててもおかしくないものだったのですが、「免疫が異常に活性化していくということは、抗体をいっぱい生み出す作用がありそうだ」ということで、医薬品に応用できないかと研究を継続しました。
抗体を作り出す「AJP001」に、実際に抗体がくっつく部分を結合させた抗体誘導ペプチドを使って動物実験をすると、目的とする抗体ができました。そのため、このようなところを使ってどんどん抗体医薬品の代わりとなる抗体誘導ペプチドの開発品を作り出していこうと考えました。
我々はこれを「STEP UP」と呼んでいますが、それが1つのキーのテクノロジーになってきたということです。
スライドに記載のとおり、現在、「FPP003」「FPP004」「FPP005」の3つの医薬品候補化合物を生み出すことができました。さらにパイプラインの拡充として、新規の開発品を作り出していこうと考えています。
「FPP003」は標的タンパク質の「IL-17A」を抑制する抗体誘導ペプチドですが、こちらについては幸いオーストラリアで第Ⅰ/Ⅱ相試験、ヒトでの臨床試験まで開始できています。
坂本:ここで1つお伺いします。ペプチドというのは耳にしたことはありますが、意味がわからないという方もいるかと思います。
最近だいぶ一般化してきたと思います。化粧品に使われたり、いろいろなことに使われていると思いますが、「ペプチドはアミノ酸がくっついたもの」と考えてよろしいのでしょうか?
三好:そのとおりです。アミノ酸が2個から50個連なったものをペプチドと呼んでいます。50個以上連なったものは非常に高分子になるのですが、このようなものはタンパク質と呼んでいます。そのような区別があるということです。
通常、ペプチドクラスになると化学合成が可能になってきますが、タンパク質のように50個以上と非常に大きなサイズになってくると合成していくのが困難になってくるため、細胞などで作らせていくという流れになります。
八木ひとみ氏(以下、八木):大阪大学はもともとペプチドの研究で有名なのですか?
三好:成り立ちからご説明します。通常、細胞が増殖していくためには細胞に栄養分を与える必要があるため、血管も一緒に作られていかないと細胞も増殖していかないということになります。
血管をどんどん作らせていく因子と言いますか、そのようなものを探索していたのが大阪大学です。どのような遺伝子が血管を作っていくのかについて、遺伝子研究を行っていました。こうして、大阪大学の中で血管を作り出す遺伝子を見出していったのです。
実際に体の中で作用するのは、遺伝子から作られるタンパクです。そのタンパクはどのようなものなのかを研究して見つけたのが「AG30」などになります。ですので、もともとは血管を作り出すために「AG30」を見つけました。
我々の皮膚はバリア機能によって、空気中にたくさんいる菌から皮膚自体を防御することができますが、そのような皮膚の中にある抗菌ペプチドは世の中でも知られています。この「AG30」の構造は抗菌ペプチドに非常に似ていたため、調べてみると抗菌活性もあったのです。
もともとは血管を作らせる作用があるということで「AG30」を見つけましたが、抗菌活性もあったということで、ダブルの作用が見出されたということになります。
坂本:「AG30」は30個のアミノ酸がくっついているのに、20個(「SR-0379」)に改良したというのは合成しやすいからでしょうか?
三好:合成のしやすさもそうですが、合成のコストも下がります。もう1つは、医薬品としての安定性が挙げられます。冷蔵保存しなければいけないものから室温保存でよいものになると、医療機関や在宅で使用するにあたって非常に利便性がよいため、そのようなところまで考えています。
坂本:少なすぎるとまた問題が出てくるのですか? 10個よりも20個が最適なのでしょうか?
三好:今回の場合、5個くらいまで切ったものからどんどんスクリーニングしてきています。そのようなものも小さい作用があるものはありますが、医薬品になるような活性の強いものはありませんでした。
また、菌を殺す作用である抗菌活性は、ある程度の構造を持っていないとその作用を示さないため、あまり小さくすると抗菌活性を生み出すことができないものもあります。そこで、我々の中で最適化できたものが「SR-0379」や、たまたま生まれた「AJP001」となります。
会社概要 ― 研究開発パイプライン
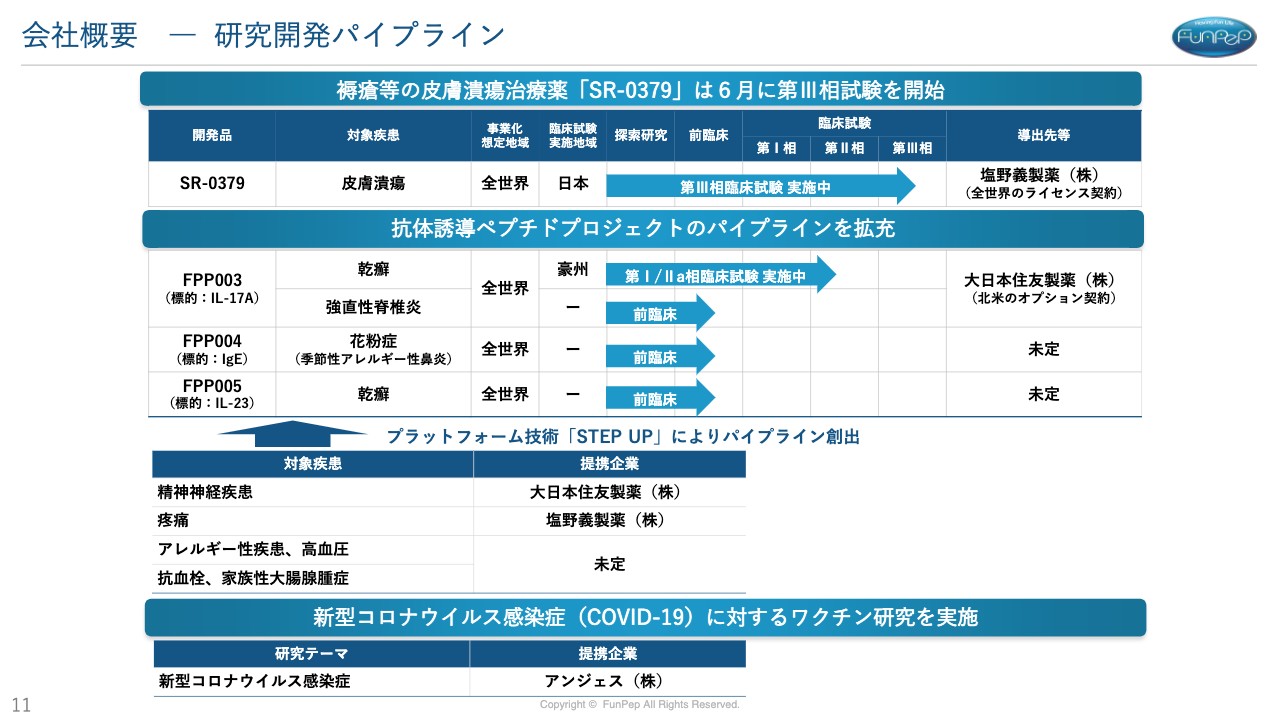
三好:パイプラインです。先頭で走っているのが皮膚潰瘍治療薬の「SR-0379」で、第Ⅲ相試験に入っています。こちらは塩野義製薬とすでにライセンス契約を結んでいる状況です。
今後の成長の源泉となる「AJP001」を使った抗体誘導ペプチドですが、「FPP003」はオーストラリアで第Ⅰ/Ⅱ相試験を行っている状況です。こちらは大日本住友製薬とオプション契約を結んでいます。
花粉症の薬の「FPP004」、乾癬の治療薬の「FPP005」は、医薬品候補化合物を見つけて前臨床試験を行っているところです。我々のプラットフォーム「STEP UP」を用いて、「このような医薬品候補化合物をどんどん見つけていこう」と言っている状況です。
八木:乾癬も花粉症も悩んでいる方は多いですからね。
三好:乾癬に関しては日本では数は少ないですが、白人と言いますか、コーカシアンの患者さまは非常に多いです。
会社概要 ― 当社の優位性と開発意義

三好:我々の優位性についてです。1つは、開発パイプラインをどんどん見出すことができるのが我々の会社の強みになっていると思います。
先頭で走っている「SR-0379」が国内で臨床試験の第Ⅲ相まで入っていることや、抗体誘導ペプチドについては抗体の産生のみを誘導するペプチド「AJP001」の特許を持っているため、他の会社は真似できないというところがあります。
それから、抗体医薬品の代わりになるものを見つけていくことを考えているため、他の新しいメカニズムを持った医薬品よりも低い開発リスクで開発できます。
抗体医薬品は世の中でたくさん開発されており、現状でも数多くあります。そのようなものの代替を狙っていくため、候補化合物と言いますか、医薬品候補となり得るようなものはどんどん生み出すことができるということになります。
冒頭で、「医薬品候補化合物を見つけるのに大手の製薬会社でも3年から5年かかる」とお伝えしました。我々は2015年から本格的に医薬品開発を始めましたが、6年間で3つの医薬品候補化合物を見つけています。
小さなベンチャー企業ですが、「3つ見つけられたのはこのような技術があったから」という証明になるのではないかと考えています。
このようなものについても社会に貢献できるようなものでないと、我々の存在意義がありません。ですので、存在意義があるということをスライドの下段に記載しています。皮膚潰瘍は、高齢化社会になるにつれてどんどん多くなると考えています。
治療が困難な皮膚潰瘍を早期回復する「SR-0379」を開発していますし、我々の抗体誘導ペプチドは抗体医薬品による治療よりも安く提供することができます。日本も含めた先進国では医療財政問題に関するニュースがありますが、その解決にもなると思います。
また、よく効く抗体医薬品が高額なため適用できない患者さまに対しても、我々の抗体誘導ペプチドであれば届けることができるのではないかと考えています。これはSDGsの持続的な開発目標の達成に大きく貢献すると思っています。
皮膚潰瘍治療薬「SR-0379」 ―高齢者のQOL改善に向けて
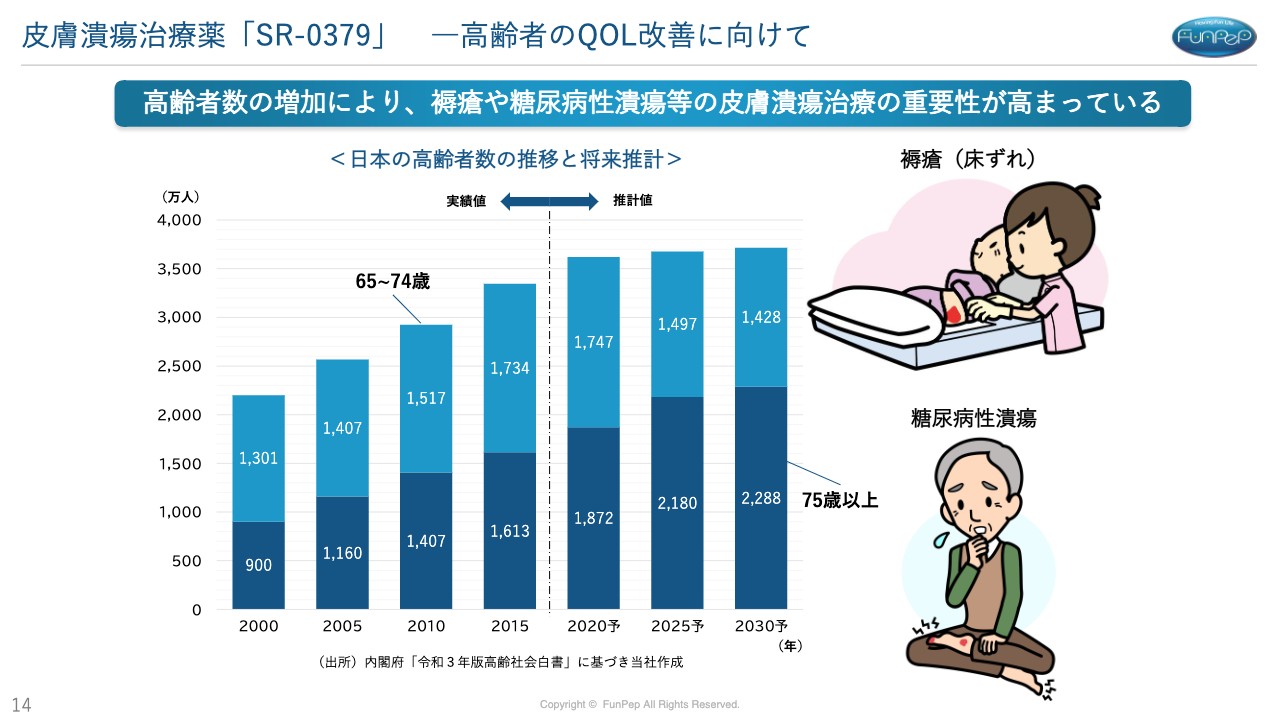
三好:トピックスとして、「SR-0379」の特徴をご説明します。先ほどお伝えしたとおり、日本の場合は高齢化社会がどんどん進んでいます。
高齢化が進むにつれて寝たきりになる患者さまが増えるため、褥瘡も増えてくるだろうと考えます。また、生活習慣病である糖尿病も増えてくるということで、糖尿病性潰瘍の患者さまも増えてくると推定されます。
皮膚潰瘍治療薬「SR-0379」 ― 皮膚潰瘍治療の課題
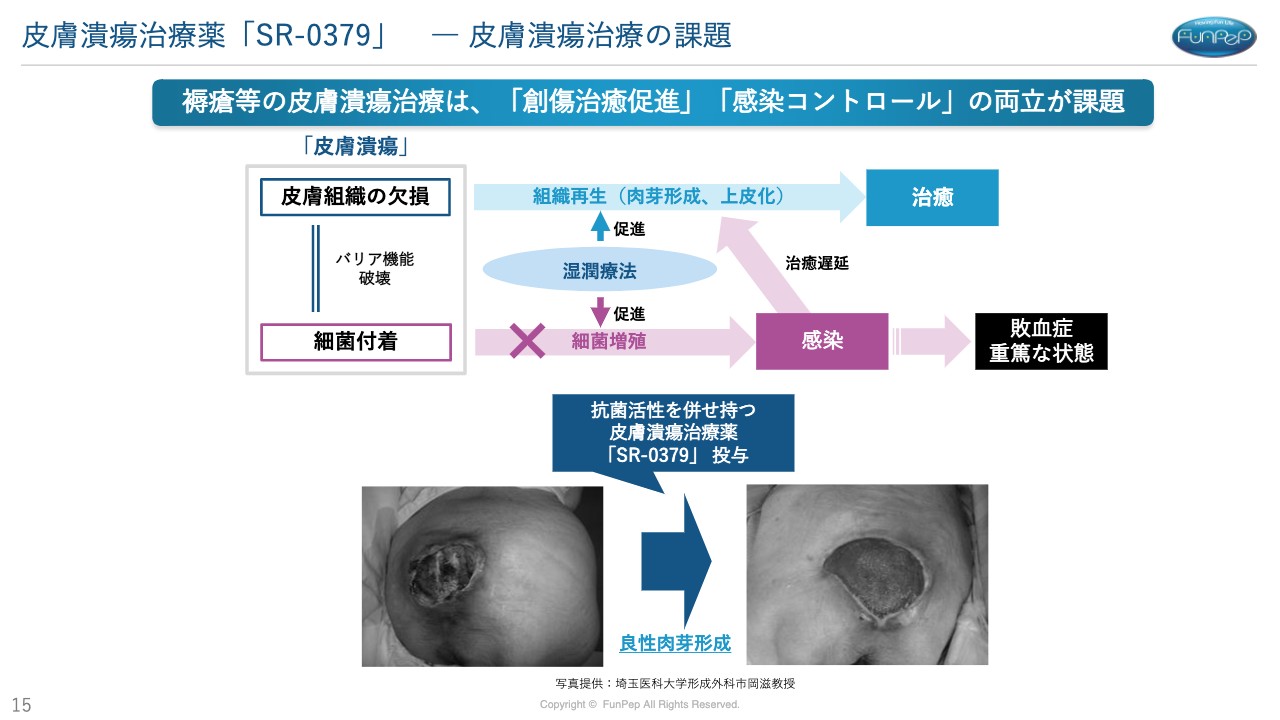
三好:褥瘡の治療法です。先ほどの抗菌のところでもご説明しましたが、皮膚は基本的にはバリアされているため、細菌などが繁殖しないようになっています。
そのため我々は外でも生活できるのですが、褥瘡の患者さまはこのようなバリア層がない状況になっています。栄養分もあるため、細菌が増殖しやすい環境になるのです。
敗血症のように生命に危険を及ぼすような感染症になる可能性もあります。通常では褥瘡の治療は、スライドに記載のとおり湿潤療法が使われますが、これは細菌も増やしてしまうことがあります。
感染の可能性があると、通常は治療に入らないという状況になります。感染していないことがわかってから褥瘡の治療が行われていくというのが、褥瘡や糖尿病性潰瘍の現状の治療方法となっています。
皮膚潰瘍治療薬「SR-0379」 ― 作用メカニズムと優位性
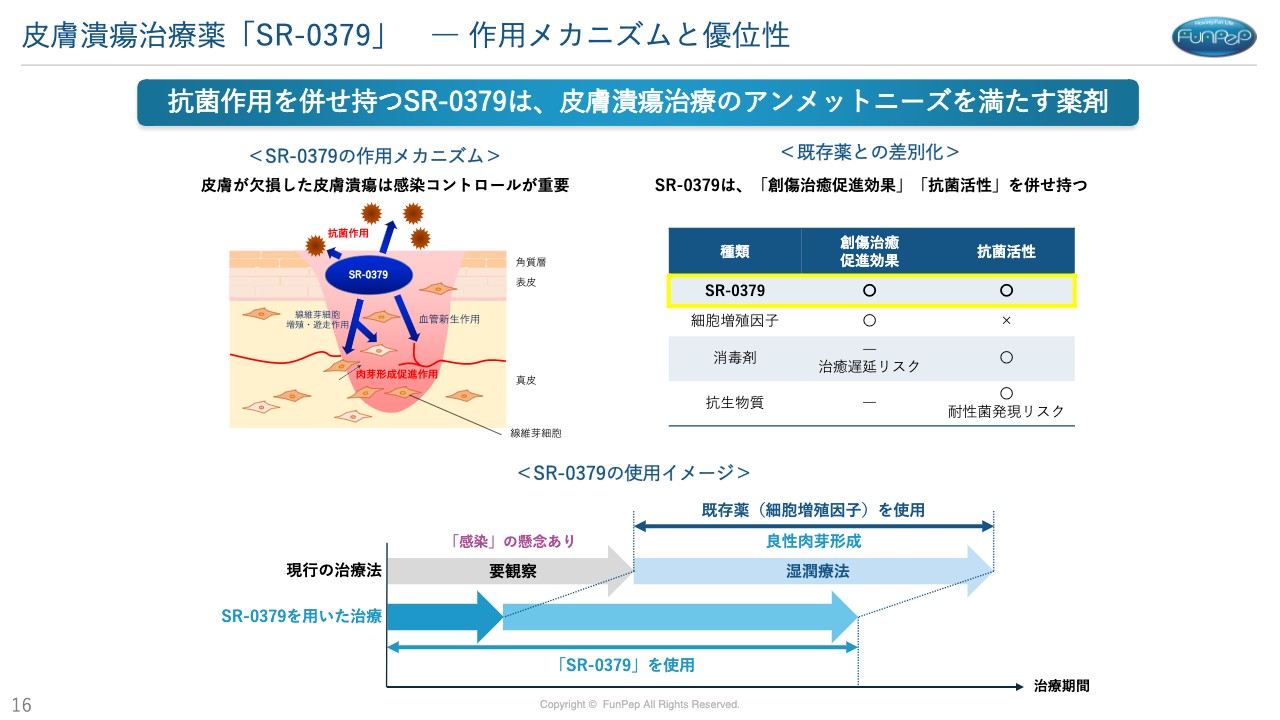
三好:ところが、我々の「SR-0379」は、スライド右側に記載のとおり、血管新生作用からくる傷を治していく作用と、抗菌活性を併せ持っています。
スライド下部の治療のイメージ図をご覧ください。これまでの治療では、感染しているかどうかが非常に重要になってきますので、感染しているかをまず観察しなければいけません。感染していないことがわかった状況からやっと薬を使う治療に入っていきます。
しかし、我々の「SR-0379」は抗菌活性を持っているため、感染の懸念があるところから使用できます。医学専門家や褥瘡などの先生方からは「褥瘡などで苦しんでいる患者さまの治療期間を短くすることができる」「社会に貢献できるような医薬品になるのではないか」と言っていただきました。
坂本:褥瘡の薬ですが、抗菌活性と治す力の両方を持っているということでよろしいですか? また、こちらは塗り薬なのでしょうか? いろいろなパターンがあると思いますが、どのような薬になるのかを含めて教えてください。
三好:先ほど安定性などのお話もしましたが、この薬は冷蔵保存ではなく室温で保存できるスプレー剤として提供します。
坂本:なるほど、イメージが湧きました。
三好:先ほどお伝えしたとおり、抗菌活性と併せ持っているところが患者さまにとって非常に有用だと考えています。
皮膚潰瘍治療薬「SR-0379」 ― 第III相臨床試験の計画
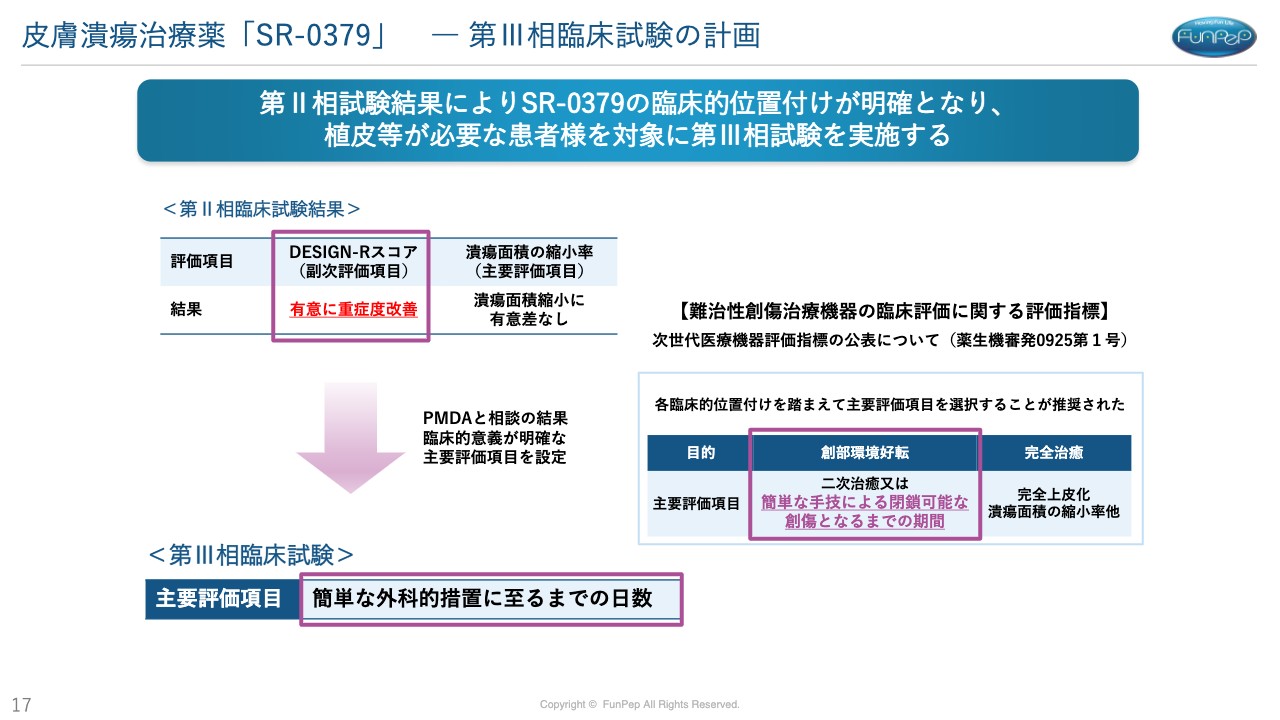
三好:第Ⅲ相試験にあたって、規制当局に「第Ⅲ相試験はこのようなことで行いますよ」と伝えたのですが、「このような臨床試験は確かに重要だよね」ということで了解いただきました。
皮膚潰瘍治療薬「SR-0379」 ― 成長性
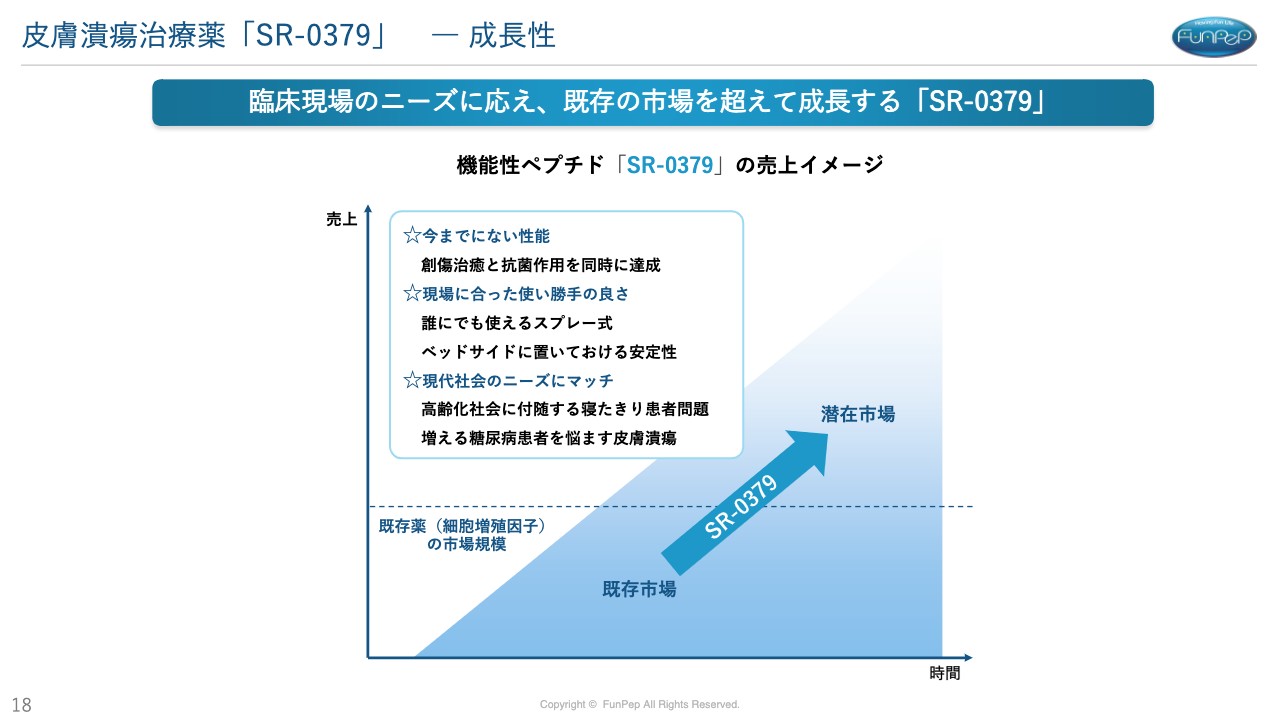
三好:売上のイメージです。現在使われている褥瘡の薬は冷蔵保存のため、我々の薬のほうが使い勝手がよいと考えます。
また、現在の治療薬は褥瘡のみにしか適応がありませんが、先ほどお伝えしたとおり、規制当局に「このような臨床試験を始めたい」と相談した際に「糖尿病性潰瘍でも使えるような薬にしてほしい」というお返事がありました。ですので、我々の薬は糖尿病性潰瘍にも使えるような薬として開発しているところです。
皮膚潰瘍治療薬「SR-0379」 ― 患者数

三好:患者数についてです。褥瘡の患者数は日本で20万人と言われています。ところが、糖尿病性潰瘍はさらに多くて、褥瘡の4倍の80万人です。
坂本:すごい差ですね。
三好:今の薬は感染の懸念があると使えず、加えて褥瘡にしか使えないことと比べると、我々の薬は非常に使用勝手がよく、よい薬になるだろうと考えています。スライドの下段には米国の患者数を記載しています。
坂本:多いですね。
三好:米国のほうが3倍くらい人口が多いこともあり、患者数としては非常に多くなっています。
坂本:今後も生活習慣は変わらないと思いますので、褥瘡と糖尿病性潰瘍の方は増え続けるというイメージでよいのでしょうか?
三好:おっしゃるとおりです。生活習慣が変わる、または寝たきりだとしてもよいベッドなどが開発されない限りは、褥瘡や糖尿病性潰瘍は増えていくと考えています。
ですので、このような患者さまに対してクオリティ・オブ・ライフとして生活の質を向上させるような薬は非常に重要になってくるだろうと思い、開発を進めています。
坂本:おそらく投資家の中には、上市までにどのくらいかかるのかを知りたいという方がいらっしゃると思います。新型コロナウイルスの影響があるかと思いますので、順調に進んだ場合のパターンを教えてください。
三好:我々は、臨床試験自体は来年には終了させたいと思っています。ただし、新型コロナウイルスの影響がどこまであるかというところはあります。
そのあとも、資料を集めて申請の準備を行い、承認申請して、当局や厚労省などによる審査を待ちます。その後、薬価を決めていくという作業があるため、世の中に出るまでにまだいろいろなステップがあります。少なくとも3年以上かかるため、2024年以降には患者さまにお届けできるのではないかと考えています。
抗体誘導ペプチド ―高額な抗体医薬品の市場拡大
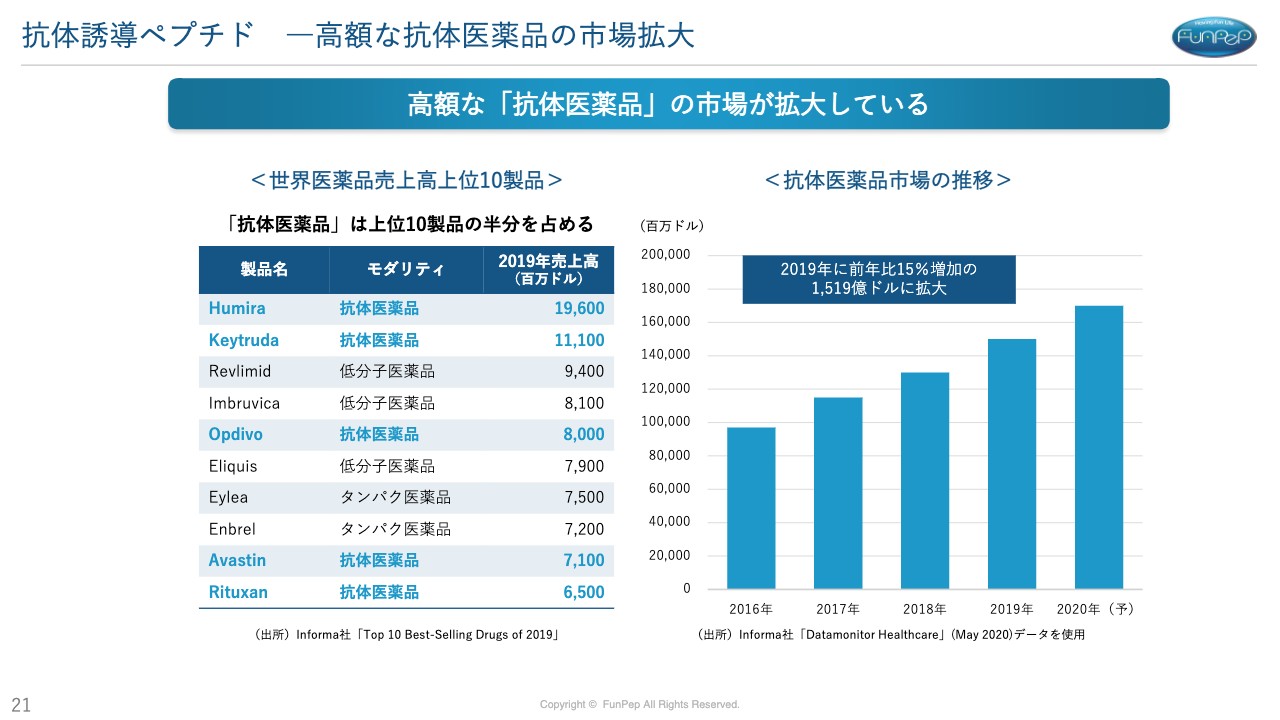
三好:抗体誘導ペプチドについてご説明します。スライドに記載のとおり、抗体医薬品は毎年伸びているどころか、世界の医薬品売上高のトップ10品目のうち5品目が抗体医薬品となっています。抗体医薬品自体は、医療モダリティと言いますか、その中心になっているということです。
抗体誘導ペプチド ―「抗体医薬品」とは?
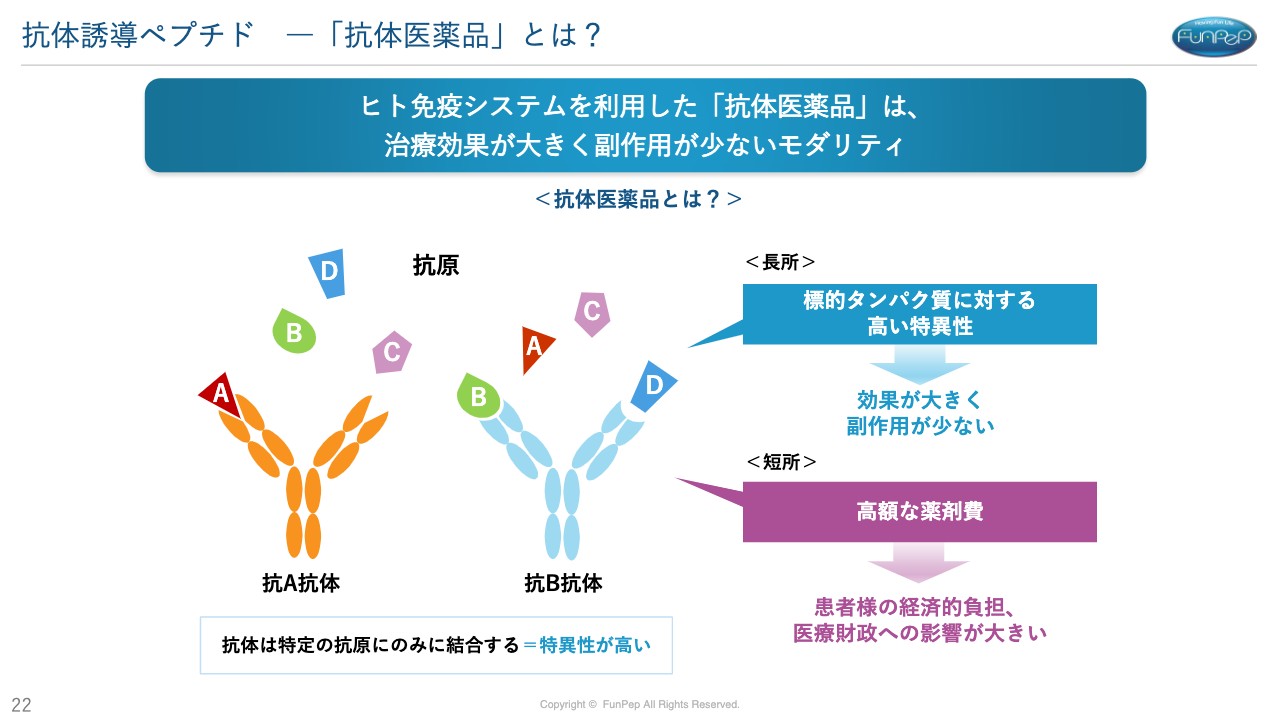
三好:「抗体医薬品はなんでいいの?」ということですが、抗体医薬品は病気の原因となるところだけに特異的にくっつくため、副作用が少なくて効果が高いという特徴があります。ただし、製造費用が非常に高いため、医薬品自体が高額になっているということにもつながっています。
抗体誘導ペプチド ― 「抗体医薬品」との違い
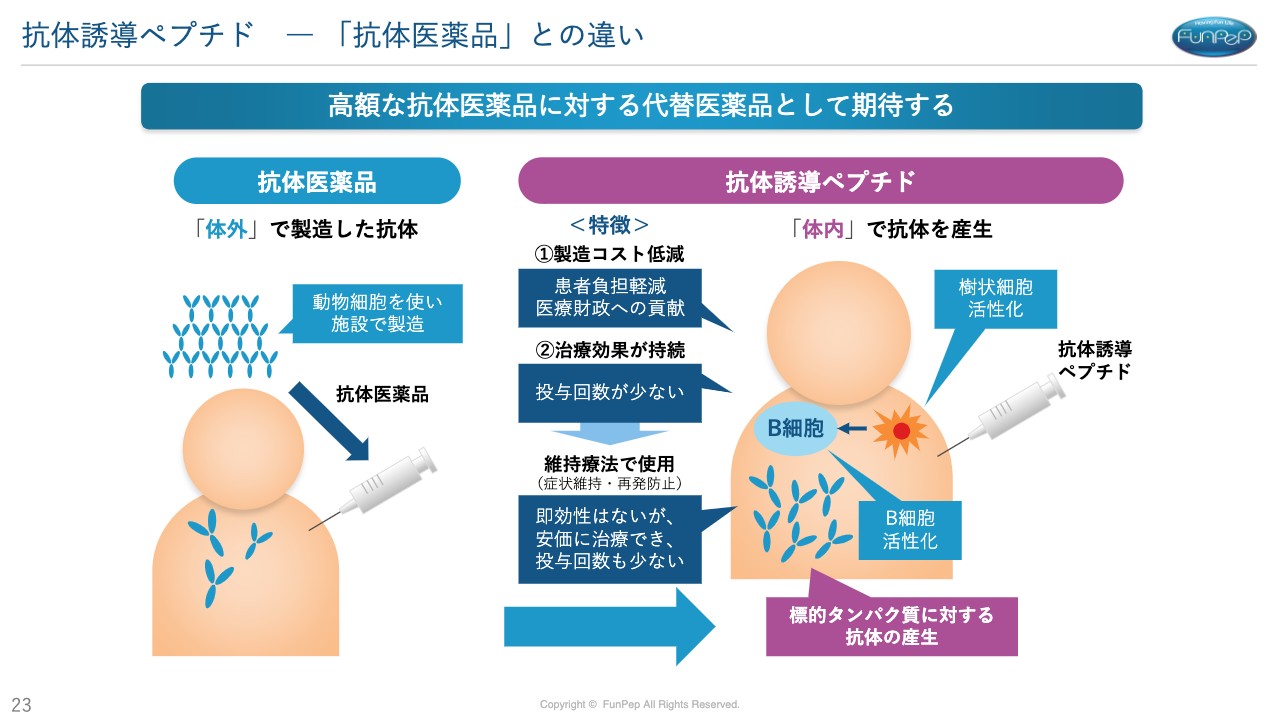
三好:我々の抗体誘導ペプチドとの違いです。抗体誘導ペプチドは、ワクチンと同様の作用があります。抗体医薬品は、病気の原因となるものを抑えるための抗体を直接投与します。抗体誘導ペプチドは、同様の抗体を体の中で作らせるというものです。抗体誘導ペプチドを打つことによって、抗体医薬品と同様の抗体を体の中で作らせます。
特徴としては、製造費用が非常に少なくて済むということです。また、ワクチンと同様の持続効果のため、抗体価が体の中で上がっていくと、なかなか下がらないということも挙げられます。年間の投与回数が非常に少なくて済むのです。この2つの効果により、年間の治療費をかなり下げることができるのではないかと考えています。
抗体誘導ペプチド ― AJP001の優位性
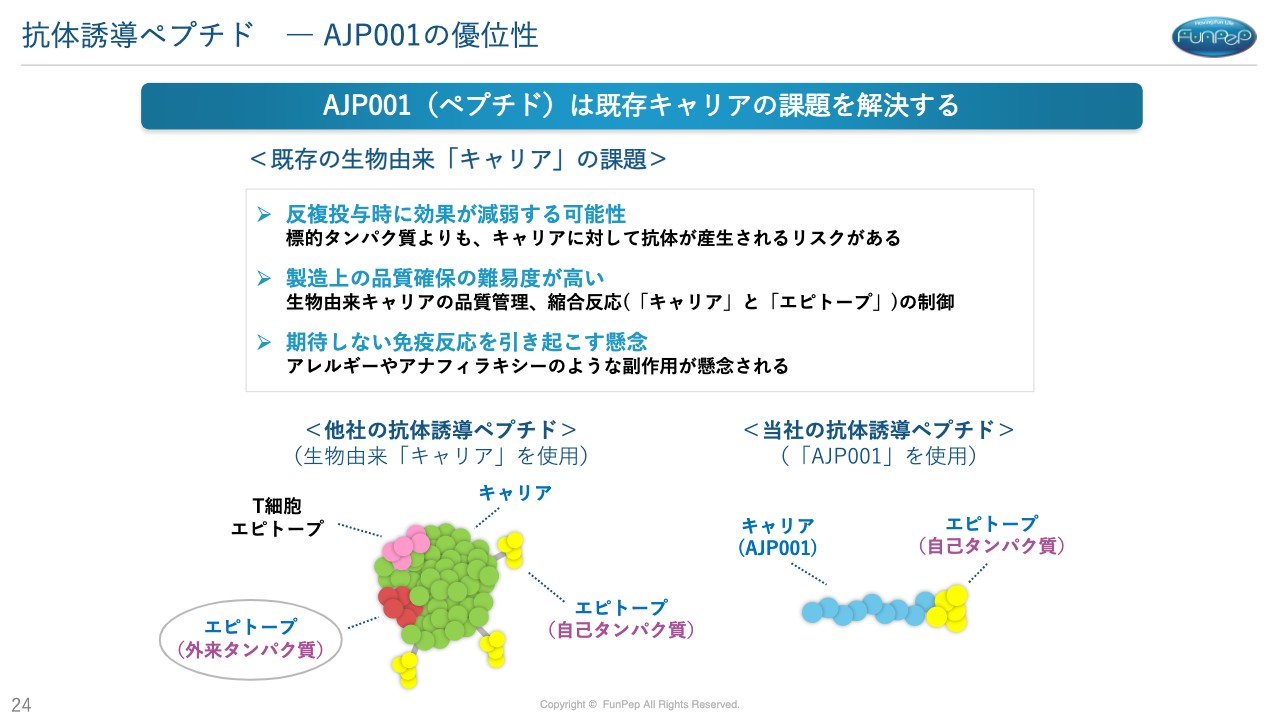
三好:「AJP001」の特徴です。ワクチンでは、どのようなものに対して抗体ができるかと言いますと、普通は高分子などの異物が入ってこない限りは免疫が誘導されないというのが、通常考えられてきたところなのです。
我々は感染症の専門家の方々とも共同研究を行っています。我々はペプチドが専門のため、どちらかと言いますと免疫学から入ってきたわけではありません。「だからできた」というところはあるかもしれませんが、このペプチドで本当に抗体ができることについて免疫学の先生方は非常に驚いていました。
高分子のものを用いてしまうといろいろな副作用が起きることもありますが、そのようなことがないという特徴もあります。
抗体誘導ペプチド ―開発パイプライン拡充
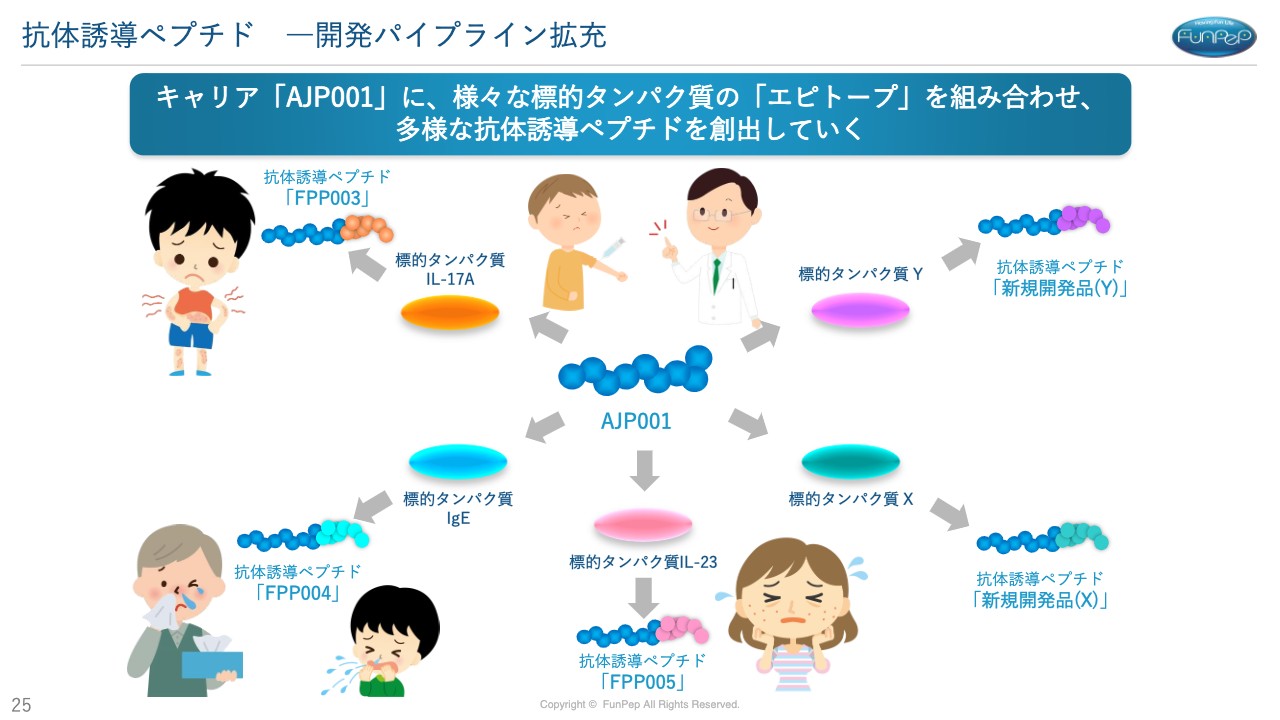
三好:抗体医薬品として売り出されているものの代わりになるものをどんどん作っていけるため、開発パイプラインを増やすことが可能となっています。
抗体誘導ペプチド ― 将来性
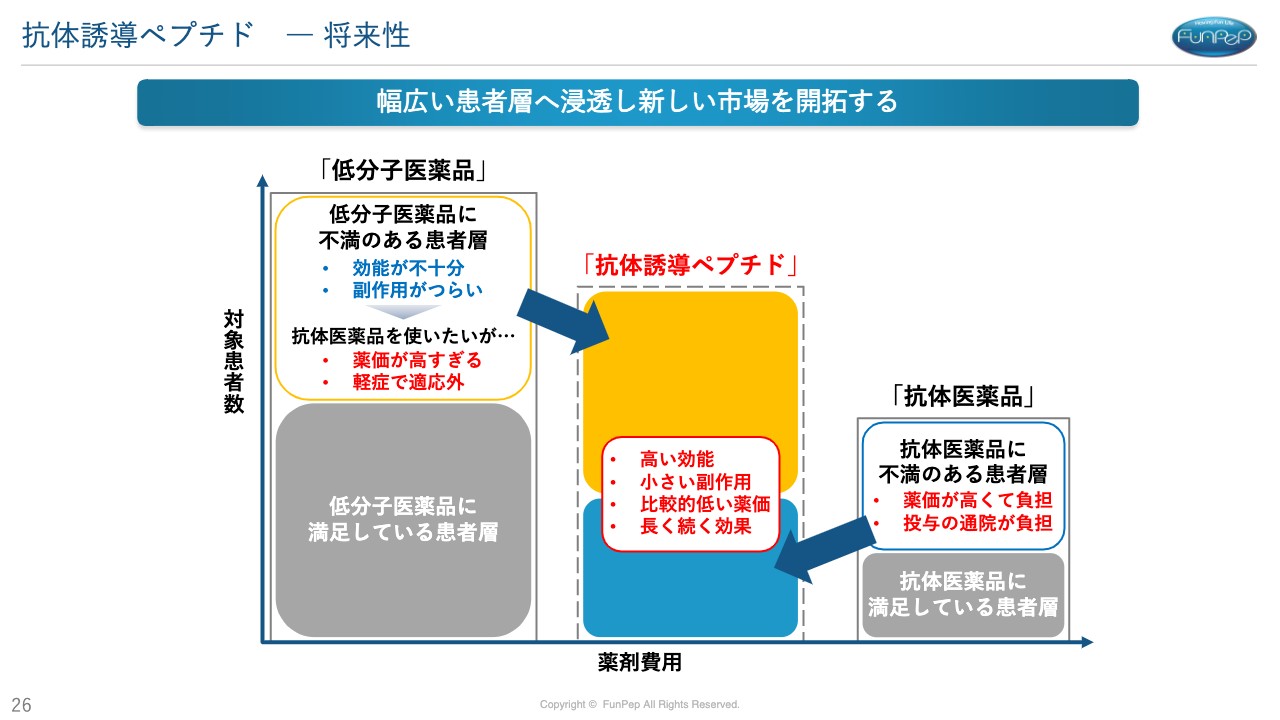
三好:どのような市場を考えているかについてです。1つは、慢性の疾患で抗体医薬品を月1回や2週間に1回打たなければいけないのに高額なものに関して、患者さまが「安くて投与回数も少なくて済むのなら」ということで乗り換えることが挙げられます。
薬剤費を下げないといけないという国家戦略にもつながってくると思いますが、抗体医薬品は非常に高額なため、重症患者にしか投与されないことがあります。よく効く薬のため、中等症の患者さまでも「本当は抗体医薬品を打ちたいよ」という方がいるかもしれません。
そのような患者さまも「同様の作用で、安価なら」ということで、我々のほうに流れてくるのではないかと考えています。ですので、市場は非常に大きくなるのではないかと想定しています。
抗体誘導ペプチド ― 将来性(ターゲット、対象疾患)
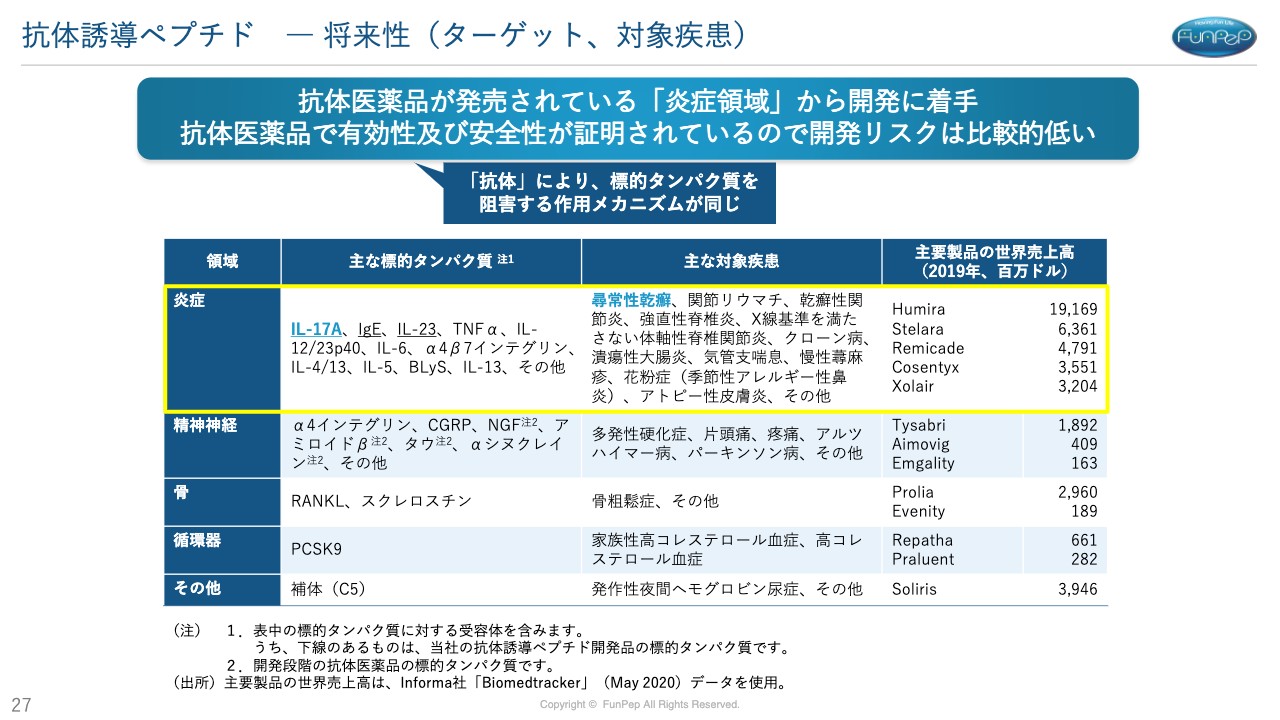
三好:どのようなパイプラインがあるかについてです。スライドに記載のものを全部開発できるかということもありますが、市場が非常に大きい抗体医薬品に対して、どんどん代替できるものを開発していきたいと考えています。
医薬品候補化合物をまだ3種類しか見つけていませんが、いろいろな標的タンパク質があるということを示しているのがスライドの表です。
抗体誘導ペプチド ― 抗IL-17A抗体誘導ペプチド「FPP003」①
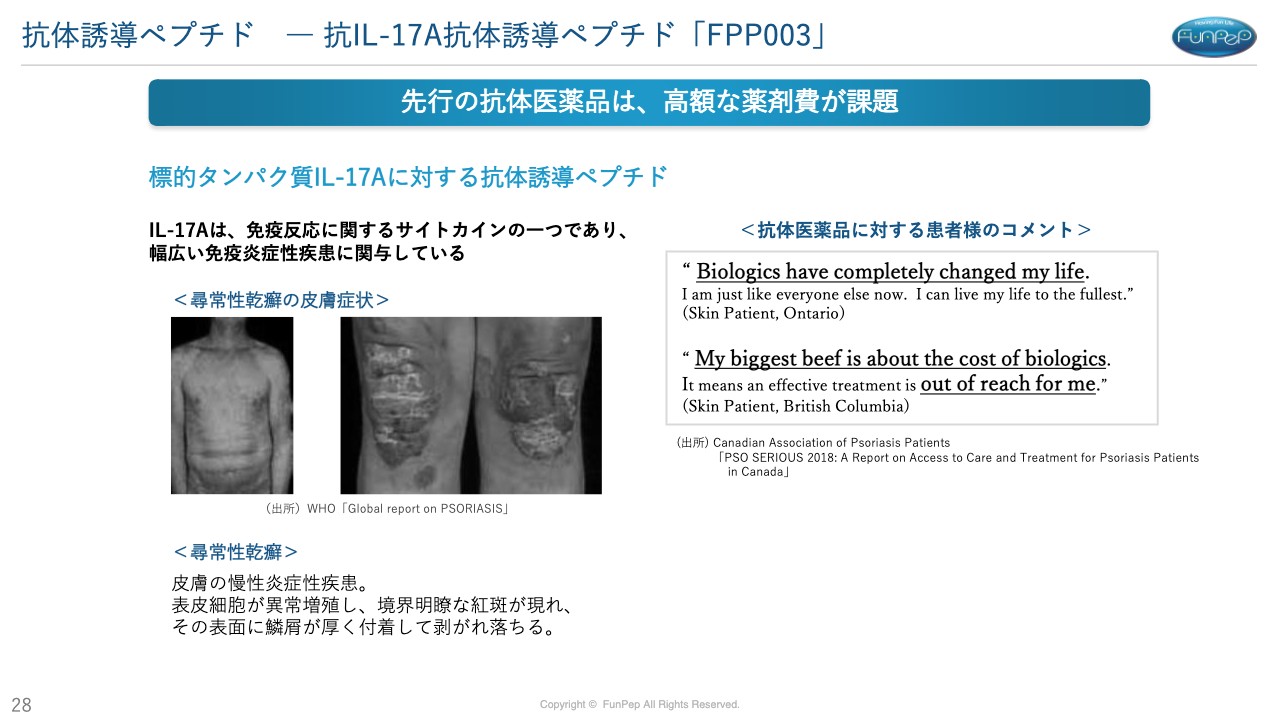
三好:「本当にそんなものができるの?」ということで、「FPP003」についてご説明します。乾癬の治療を行っています。乾癬は慢性疾患で、白人の患者数が非常に多いです。
スライド右側に記載のとおり、「biologics」です。抗体医薬品は「本当に生活を変えたよ」という喜びの声が聞こえる一方で、「高すぎて届かないよ」という声もある状況です。
抗体誘導ペプチド ― 抗IL-17A抗体誘導ペプチド「FPP003」②
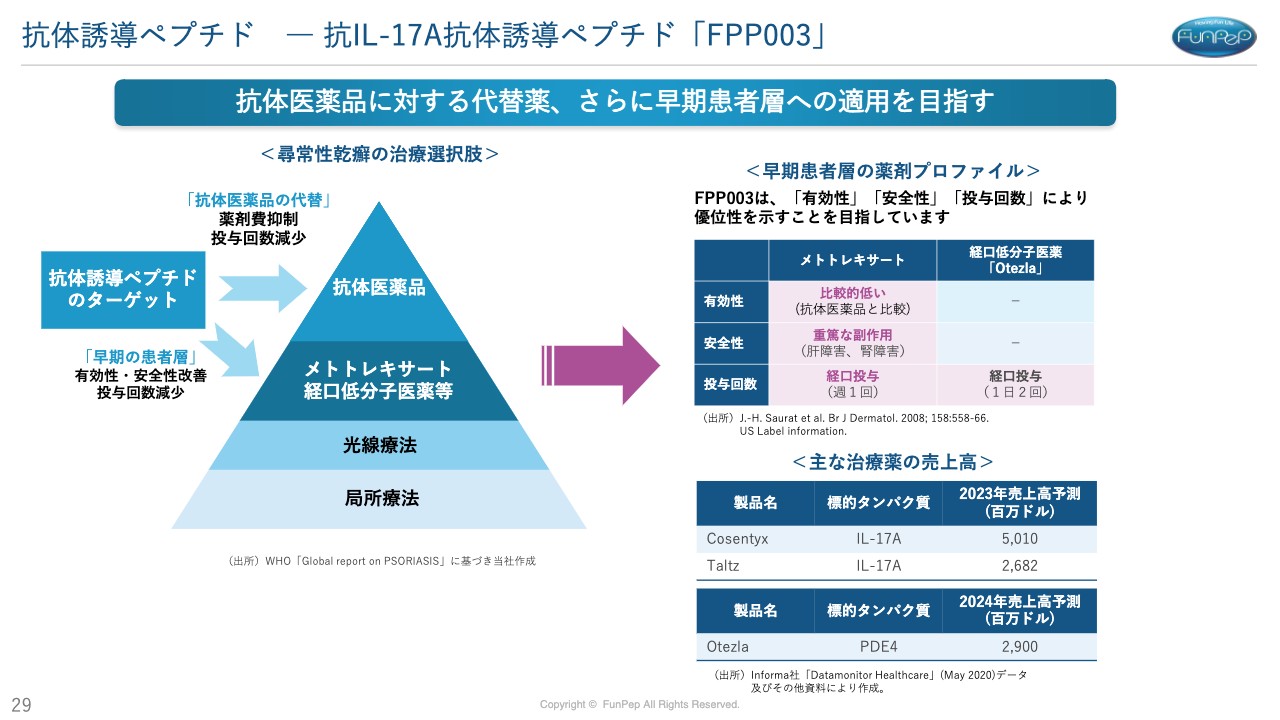
三好:我々の抗体誘導ペプチドは、先ほどお伝えしたとおり、抗体医薬品を投与している方々や、重症ではない患者さまで「抗体医薬品は高いから経口低分子医薬品などを使わざるを得ない」という方に対して使われていくだろうと考えています。
スライドの右下に「主な治療薬の売上高」を記載しています。こちらも我々が標的としている「IL-17A」です。「Cosentyx」「Taltz」という薬を合わせて8,000億円くらいの売上が予測されています。
経口低分子医薬品の新薬も2,900億円くらいの売上高予測ということで、市場は非常に高いところになっています。そのようなところに、新しいモダリティとして参入できるのではないかと考えています。
パイプラインの開発計画

三好:パイプラインの開発計画です。先ほどからお伝えしているとおり、皮膚潰瘍治療薬「SR-0379」は今年6月に治験申請を行い、今月の8月に1人目の患者さまに投与することができました。フェーズⅢを進めているところです。
乾癬の治療薬「FPP003(標的:IL-17A)」は、臨床試験の第Ⅰ/Ⅱ相を進めている最中です。計画よりやや遅れ気味ですが、目標としては来年の中頃には終了したいと考えているところです。
花粉症の薬は候補化合物が見つかり、前臨床試験を開始しています。「IL-23」の新しいターゲットについても、今年に医薬品候補化合物を見出すことができ、前臨床試験を開始しました。最後のほうは駆け足になりましたが、以上で説明は終了させていただきたいと思います。
質疑応答:特許取得について
八木:特許は何に対して取ったのかをもう一度教えてください。
三好:創薬ベンチャーで非常に重要なところは、特許が独占的に開発権を持つというところです。こちらを製薬会社に渡すため、ビジネスとして特許は非常に重要なものになっています。
我々が持っている特許は、1つは「SR-0379」の物質特許を持っています。もう1つは、抗体をたくさん作らせていくという「AJP001」自体の特許です。
「AJP001」だけでは「抗体をたくさん作らせますよ」ということになりますが、どのような抗体を作らせていけばよいのかについては、「AJP001」のペプチドにさらにもう1つ作らせたい部分のペプチドをつなげます。
つなげたものが「FPP003」「FPP004」「FPP005」ですが、これらは単独でまた特許を取っていくという特許戦略になっています。

八木:なるほど。スライド10ページの中央に記載の「AJP001」のSTEP UPがカギになってくるということですね?
三好:そうですね。現状ではキーテクノロジーになっているこのペプチドがあるおかげで、抗体医薬品の代わりとなるような抗体誘導ペプチドが開発できているということになるため、こちらがキーのパテントになっています。
このパテントを持っているため、他の会社で「AJP001」を用いた抗体誘導ペプチドを作っていくことができないということにつながっています。
坂本:現状では、「AJP001」を他の会社に導出することはないのでしょうか?
三好:ないことはないと言いますか、基礎研究という医薬品候補化合物を見つけていくためには我々はまだ研究員の数が少ないですが、製薬会社は数多く研究員を抱えており、我々の「AJP001」で製薬会社が目的としているような抗体誘導ペプチドなどを作り上げていきたいという提案をいただくことがあります。
我々は「AJP001」のパテントを持っていますので、そのような製薬会社については「それをじゃあ使ってください」「それで抗体誘導ペプチドを作ってください」というかたちの契約も行っています。
坂本:なるほど。そこが伸びてくれば、ということですね。
三好:おっしゃるとおりです。
坂本:ロイヤリティになる可能性もあるというところですね。
質疑応答:資本が減ってきた場合のデッドラインについて
坂本:財務の部分についてです。研究開発費はある程度もらっている部分もありますが、その前段階の部分もある程度お金がかかると思います。上場して現状は資本がまだ厚いと思っていますが、これが減ってきた場合のデッドラインは考えているのかを教えてください。
三好:我々の会社はまだまだ投資先行型と言いますか、研究開発費がどんどん重くなってくる状況です。研究開発費やバックオフィス費などを賄えるような収益はまだ上げられないし、まだまだ研究開発をどんどん前に進めていこうと計画しています。
ですので、キャッシュポジションと言いますか、我々の手元にあるキャッシュについては、上場してまだ間もないところですが検討している状況です。収入や、今後かかってくる開発費用などを考えて、適切なかたちで資金調達などを行っていきたいと考えています。
質疑応答:競合について
八木:ペプチドの競合はいるのでしょうか?
三好:ペプチドの競合と言いますか、我々の抗体誘導ペプチドの競合は、治療用ワクチンですね。
坂本:そうですね。
三好:新型コロナウイルスのワクチンは予防用ワクチンと言われるもので、外から感染したものについて予防していくというワクチンですが、我々のように体の中で抗体を作らせていく技術を使って、(予防用ではなく)治療に向かっていこうというところはいくつかあります。
ただし、ペプチドのみで抗体を作らせていくという競合はほとんどありません。
Zoomウェビナーに寄せられたその他の質問と回答
Zoomウェビナーの「Q&A」に寄せられた質問について、セミナー当日は時間の関係で取り上げることができなかったものを、後日回答いただきましたのでご紹介します。
<質問1>
質問:医薬品に機能性ペプチドを用いることの最大のメリット、特徴はどういったところにあるのでしょうか? 医療及び医薬品分野に詳しくないためご教示いただきたいです。
回答:医薬品開発は、これまで低分子医薬品の創薬を中心として行われてきました。低分子医薬品とは、分子量が500以下ほどであり、物質としては小さいため、低分子と呼ばれており、化学合成されるものが主です。
低分子医薬品の開発は、これまでの長い医薬品の研究開発の中心であったことから、標的となるターゲットが枯渇し、創薬研究がより難しくなっていることが製薬業界で指摘されております。そこで、医薬品を開発する別の手法が探索され、高分子である抗体医薬品が開発され、医薬品市場の上位を占めることとなっております。
当社は、機能性ペプチド、特に、抗体誘導ペプチドの研究開発に注力しております。抗体誘導ペプチドの作用メカニズムは、ヒトが持つ免疫反応を活用して、病気の原因となる生体内分子に作用する抗体を体の中で作らせます。高分子である抗体医薬品はこれまでの医薬品の変遷の中で現在中心となっていますが、当社の開発するペプチド類は抗体医薬品と同等の効果を期待しています。
高分子でないため製造費用等での利点もありますが、標的とするターゲットはわかっているため、効率的に医薬品となりえるリード化合物を見出すことが可能です。見出したリード化合物を当社のSTEP UPを活用し、医薬品候補化合物を創製しております。
<質問2>
質問:既存の抗体医薬品を代替できる抗体誘導ペプチドの創⽣⼒とありますが、貴社同様に抗体誘導ペプチドに目をつけて事業を行う競合などについて教えてください。
回答:日本国内では抗体医薬品を代替できる抗体誘導ペプチドを開発している会社は、調査した範囲ではございません。国外では、数社あります。
<質問3>
質問:特許は、機能ペプチドの化学構造に対してでしょうか? 以前、別の会社で、20年しか保護されないため、あえて特許を取らないという戦略をとる事例を知りました。貴社の場合に、特許をとる利点を教えてください。
回答:製造方法に独特の技術を有する場合などは、特許情報が情報を与え、似た新しい製法の開発を促進してしまう可能性もありますが、医薬品の場合、製法の特徴はあまり大きくないため、同じ化合物の製法は隠しても見出されてしまいます。よって、製法を公開していなくとも特許が切れると同じ医薬品が後発医薬品として上市されます。
当社に限ったことではありませんが、医薬品の開発は時間と費用が多大にかかるため、同様な医薬品(競合品)が上市されないように化合物としての独占権を得ておくのが重要になります。
<質問4>
質問:抗体を生み出す技術としてmRNAと抗体誘導ペプチドの使い分け(優位性)を教えていただけますと幸いです。
回答:mRNAワクチンは、ウイルスのタンパク質をつくるもとになる情報の一部を注射します。ヒトの体内でこの情報をもとに、ウイルスのタンパク質の一部がつくられ、それに対する抗体などが産生され、ウイルスに対する免疫ができます。
一方、当社の抗体誘導ペプチドは、mRNAワクチンに必要な、体内で抗原となるタンパク質をつくる過程は不要であることに優位性があり、投与したペプチドが抗原となり、その抗原に対する抗体が産生されます。
新着ログ
「医薬品」のログ





