2026年8月期第2四半期決算説明
Chordia Therapeutics、rogocekibの開発進展 臨床試験は日米102名の症例登録完了
目次

三宅洋氏(以下、三宅):Chordia Therapeutics株式会社代表取締役の三宅洋です。2026年8月期の中間決算について、ご説明します。よろしくお願いします。
本日の内容はスライドのとおりです。
会社概要および沿革
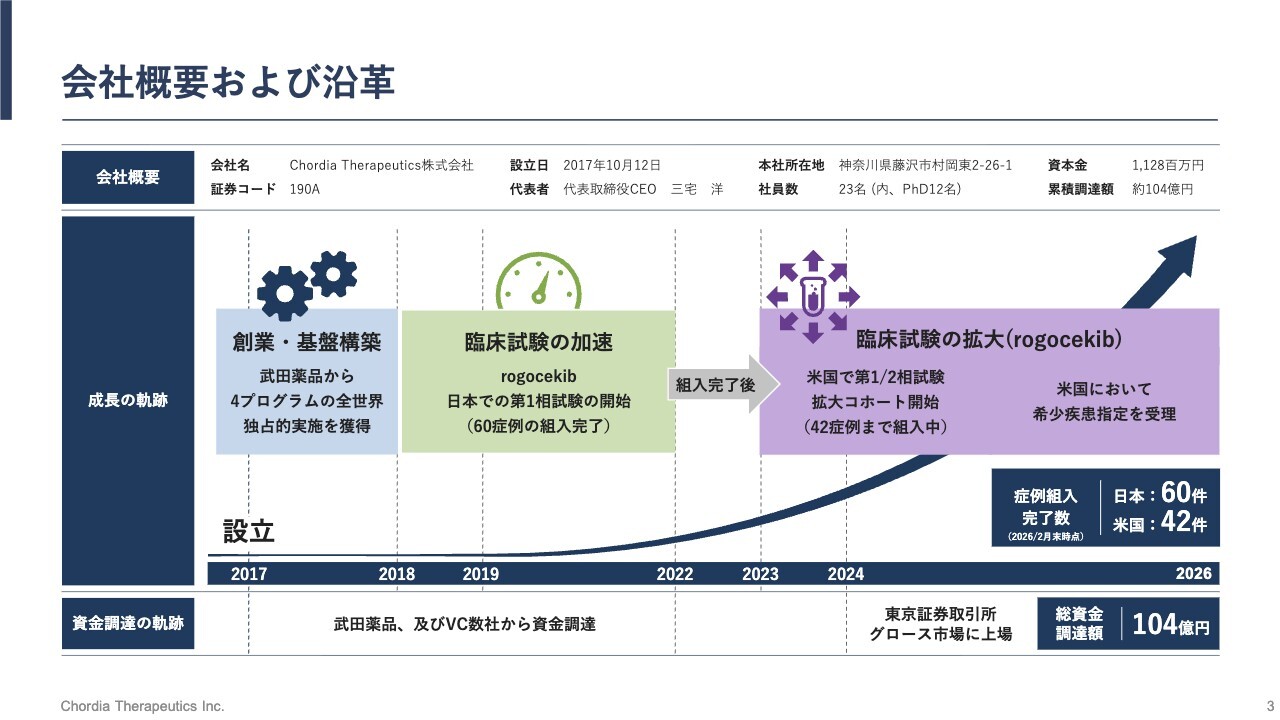
当社は、2017年10月に国内最大手の製薬企業である武田薬品からスピンアウトして創業しました。低分子抗がん薬の研究開発を行うバイオスタートアップです。
また、2年前の2024年6月には東証グロース市場に上場しており、証券コードは190Aです。
本社は神奈川県藤沢市にある湘南ヘルスイノベーションパーク(湘南アイパーク)内に所在し、従業員数は23名です。そのうち12名が博士号を有しており、少数精鋭で新しい抗がん薬の開発に取り組んでいます。
筆頭株主は、私自身の出身母体でもある武田薬品で、約15パーセントのシェアを有しています。
多様な専門性で事業成長を加速する経営体制

スライドは当社の取締役構成についてです。上場企業としてさらなる成長を目指し、昨年11月の株主総会で新たに2名の社外取締役が加わりました。土屋裕氏は、内資大手製薬会社であるエーザイで代表執行役を務めた経歴をお持ちです。
平崎誠司氏は、老舗バイオベンチャーであるアンジェスの元取締役であり、新型コロナウイルスワクチンで知られるモデルナに買収されたスタートアップ、オリシロジェノミクスの代表取締役を務めていました。
また、投資家である中村学氏を加えて、3名の社外取締役が代表取締役である私とともに、当社の企業価値の最大化を目指した経営に取り組んでいます。
なお、監査等委員3名は当社の上場前からのメンバーであり、当社の事業内容に対する深い理解を基に、経営の監督を行いながら経営判断にも貢献していただいています。
研究開発・コーポレート活動ともに順調に進行
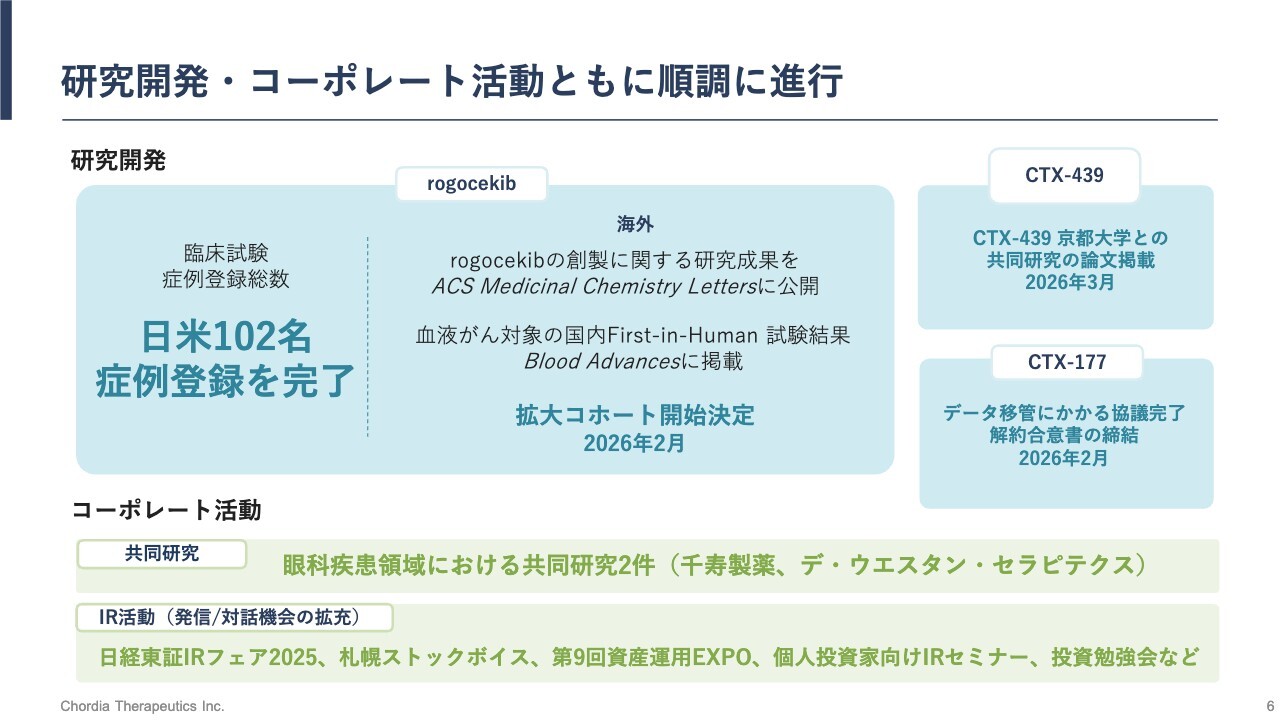
2026年8月期第2四半期の業績について、ご説明します。はじめに全体像ですが、研究開発、コーポレート活動ともに順調に進捗しています。特にリードパイプラインである「rogocekib(ロゴセキブ)」の臨床開発では、米国試験の拡大コホートを開始し、次の価値創造ステージへ進みつつあります。
米国試験では前期末から6症例が追加され、合計42症例への投与を実施しています。日米での組入れ症例数はトータルで102名となり、着実にデータを蓄積しています。
また、「rogocekib」の研究成果や臨床試験結果、3号パイプラインの「CTX-439」の研究成果は一流の国際学術誌に掲載されています。これは、当社の高い研究開発能力がグローバル水準で評価されていることを示すものと認識しています。
2号パイプラインの「CTX-177」は、小野薬品からのデータ移管がほぼ完了しました。その情報を活用しつつ、臨床開発の再開に向けた事業開発活動を鋭意継続しています。
その他、眼科疾患領域における共同研究は引き続き進行中です。IR活動としては、当社の事業活動の発信や投資家の方々との対話機会の拡充に努めています。今後も研究開発の質と対話の質の双方を高めながら、企業価値の向上に取り組んでいきます。
2026年8月期 第2四半期(中間期)の業績(損益計算書)
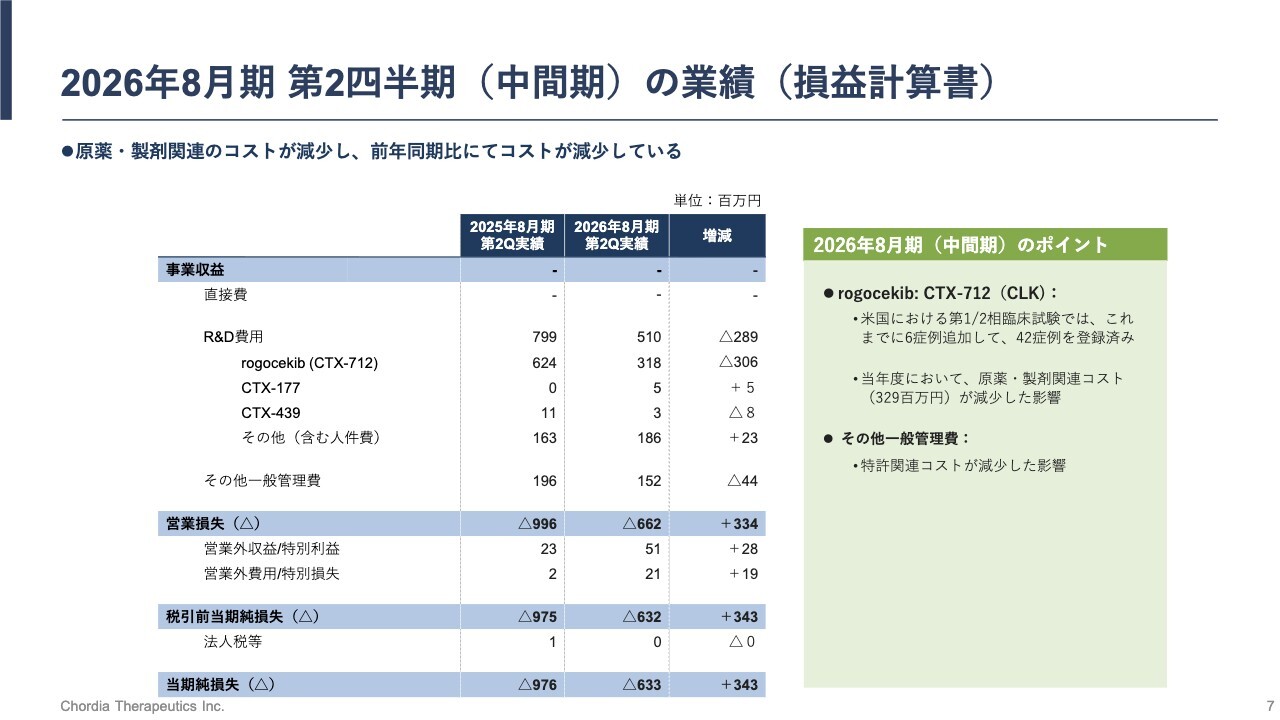
経営成績について、ご説明します。2026年8月期の上半期には事業収益はありませんでした。R&D費用は5億1,000万円であり、そのうち3億1,800万円を「rogocekib」の研究開発に充当しました。
R&D費用は一時的に予算上の想定より低位で推移していますが、こちらは主に会計上の計上タイミングによるものです。米国での臨床試験の症例組入れ自体は、概ね計画どおりに進捗しています。
以上の結果、当期純損失は6億3,300万円となりました。
2026年8月期 第2四半期(中間期)の財政状態(貸借対照表)
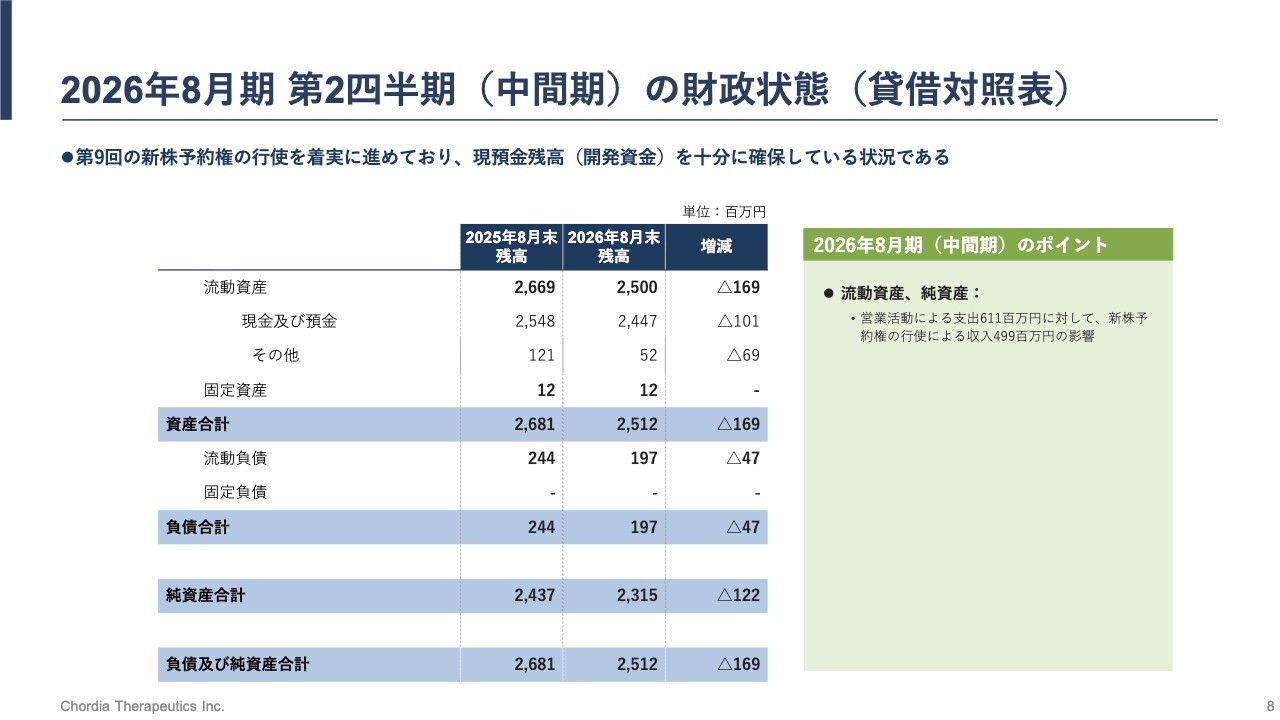
財政状態については、2026年2月末時点で約24億円の現金および預金を保有しており、当面の事業活動を継続するために必要な資金を十分に確保しています。
また、リードパイプラインである「rogocekib」の開発資金を中期的に確保する目的で、新株予約権による資金調達を進めています。
5つのパイプラインのうち、2つは臨床ステージ ~市場性の高いrogocekibに集中し、価値創出を加速~

パイプラインの進捗状況についてです。スライドは当社のパイプラインを示しています。当社は5つの低分子パイプラインを保有しており、その中で「rogocekib」と「CTX-177」の2つは臨床ステージにあるパイプラインです。
特に「rogocekib」は市場性が高く、迅速承認の可能性を考慮しており、当社は開発リソースを集中させています。
一方、他のパイプラインについては、提携や導出を視野に入れ、コストを抑えながら価値創出を進める戦略を取っています。
この集中と分散のアプローチにより、当社はリスクをコントロールしつつ、複数の収益機会を確保したいと考えています。
rogocekib CTX-712(CLK阻害薬)の開発マイルストン ~日米102名の症例登録と臨床試験のプロセスが着実に進捗~
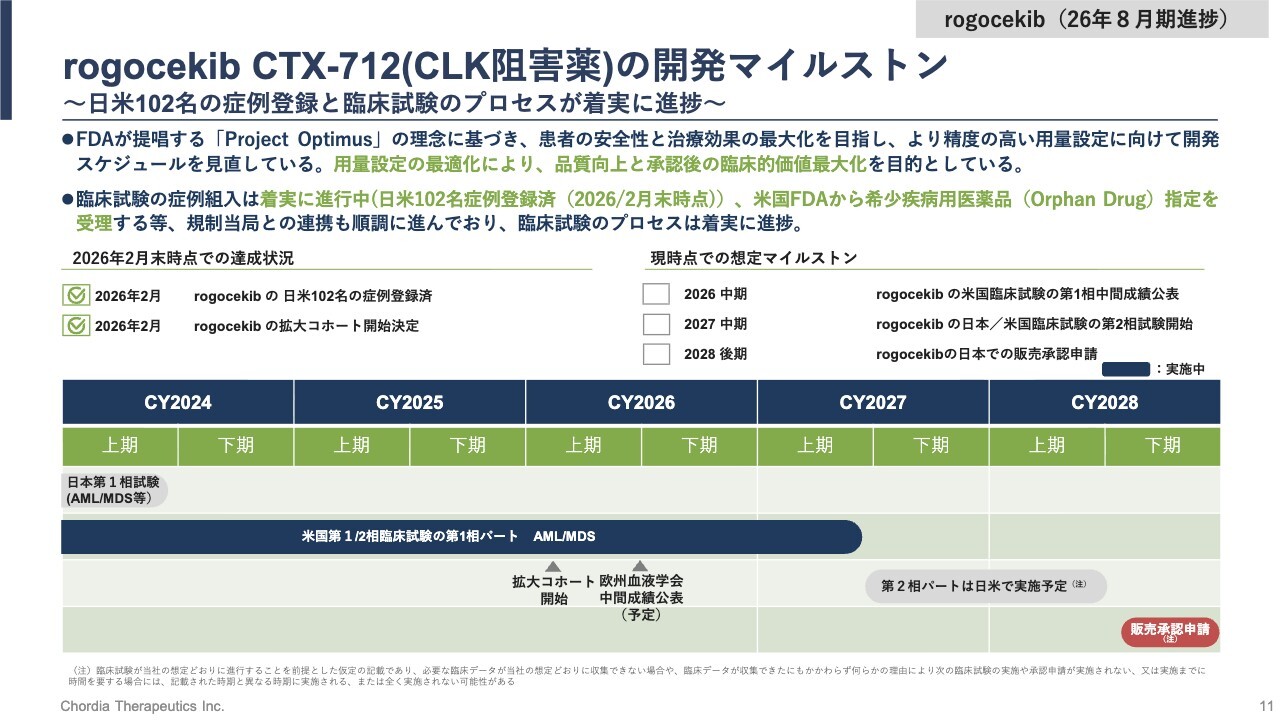
「rogocekib」の開発マイルストンです。米国試験における拡大コホートの開始は、本第2四半期において達成した最も重要なマイルストンです。また、日本および米国での症例登録数は2月末時点で102名に達しました。
今後のマイルストンとして、今年6月に開催される欧州血液学会において、米国試験の用量漸増コホートの成績を発表する計画です。すでにアブストラクトを提出しており、現在は学会からの承認を待っています。
発表内容については、発表許可が下りた後、適切なタイミングでご報告します。
Rogocekib CTX-712(CLK阻害薬):拡大コホートの開始決定
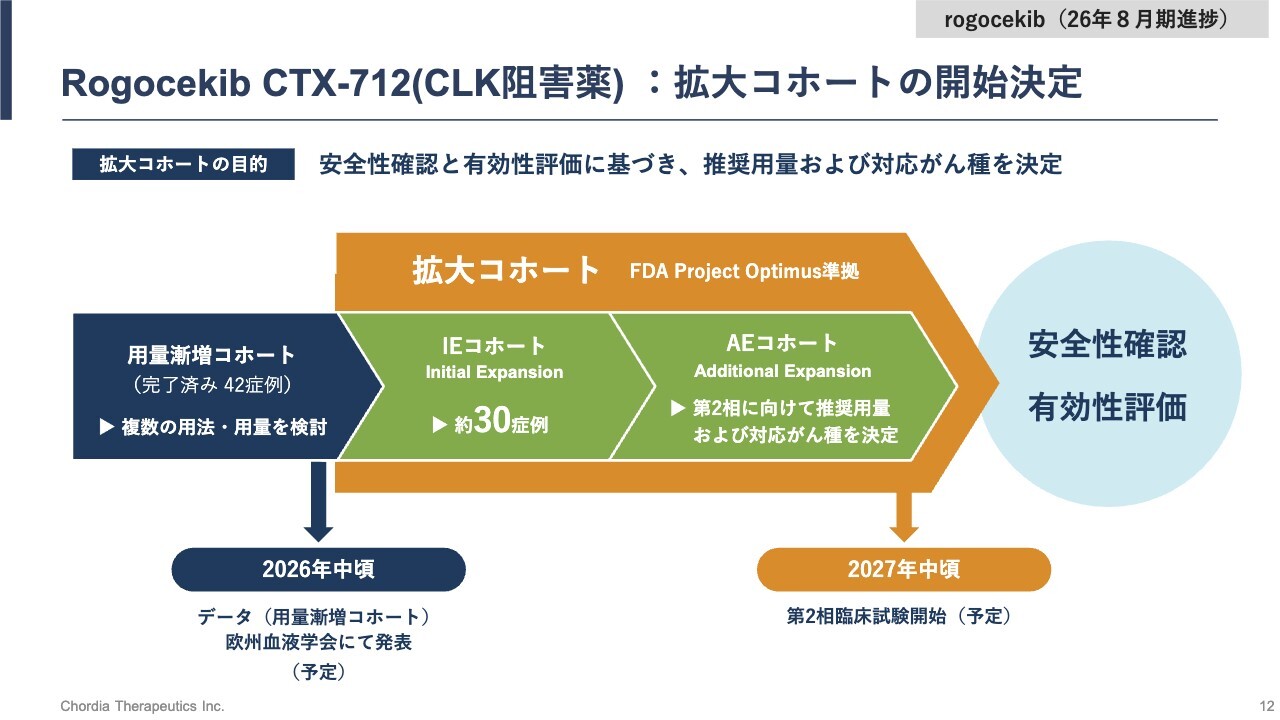
拡大コホートの詳細をご説明します。拡大コホートは、Initial(イニシャル)とAdditional(アディショナル)の2段階で組入れを進めていく計画です。
30症例程度を予定しているIE(Initial Expansion)コホートの組入れは、現在順調に進んでいます。Initial Expansionの成績を評価し、用法と用量、適応がん種を絞り込んでAE(Additional Expansion)コホートを開始する計画です。
その後、Additional Expansionの成績を含む全データを踏まえ、第2相臨床試験のデザインを決定する計画です。2027年中頃には第2相臨床試験を開始し、2028年後期には販売承認申請を行う予定です。
これらのマイルストンについては、FDA Project Optimusへの対応により2024年の上場時の計画から遅れが生じています。しかし、当社は、医療用医薬品の世界最大の市場である米国での承認申請に向けた必須の対応と考えています。「rogocekib」の価値を最大化するための戦略的な判断です。
収益化戦略と「選択と集中」~戦略(開発期間の短縮)×「選択と集中」(低分子・ファーストインクラス・プレシジョン )~
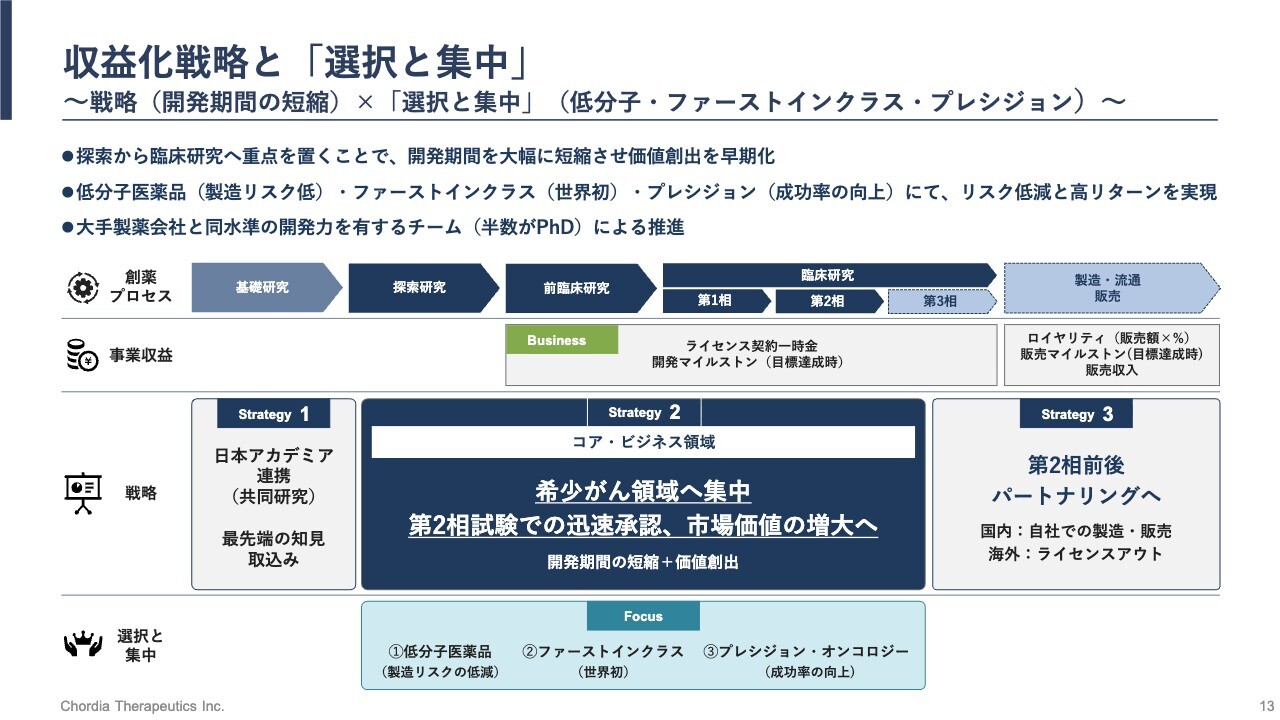
収益化戦略についてです。新薬の誕生にはおよそ20年の歳月が必要です。前半の10年は、大学などでの基礎研究から始まり、探索研究、前臨床研究を経て、ようやく人での臨床試験が始まります。
後半の10年では、臨床試験を通じて人における安全性と有効性を確認し、承認および薬価決定を経て、ようやく販売に至ります。この長い道のりは、まさにマラソンのような挑戦です。
当社は、この20年のプロセスの中で探索研究から第2相試験までを自社で担う戦略を採用しています。この戦略の背景には、開発期間の短縮と価値創出の加速という明確な狙いがあります。
具体的には、基礎研究は日本の大学に委託し、共同研究を通じて最先端の知見を取り込んでいます。日本の大学のサイエンスレベルは世界トップクラスであり、当社はその強みを最大限に取り入れています。
また、自社開発を希少がん領域に集中させることで、第2相試験の結果で迅速承認を得る可能性が高まり、通常より早く市場に到達することが可能です。さらに、第2相試験で良好な結果が得られれば、パイプラインの価値が大きく向上し、導出による収益化も実現できます。
一般的な創薬ビジネスはハイリスク・ハイリターン型ですが、当社はリスクをコントロールし、成功確率を高める体制を整えています。メンバーの半数以上が博士号を有し、大手製薬企業並みの開発力を持つ少数精鋭チームです。意思決定のスピードと柔軟性を兼ね備え、科学的優位性を確保しながら、迅速に開発を進めます。
この体制により、当社はハイリスク・ハイリターンでありながら、より確度の高い価値創出を目指していきます。
不確実性に対応しつつ、価値創出を加速する多様な資本戦略
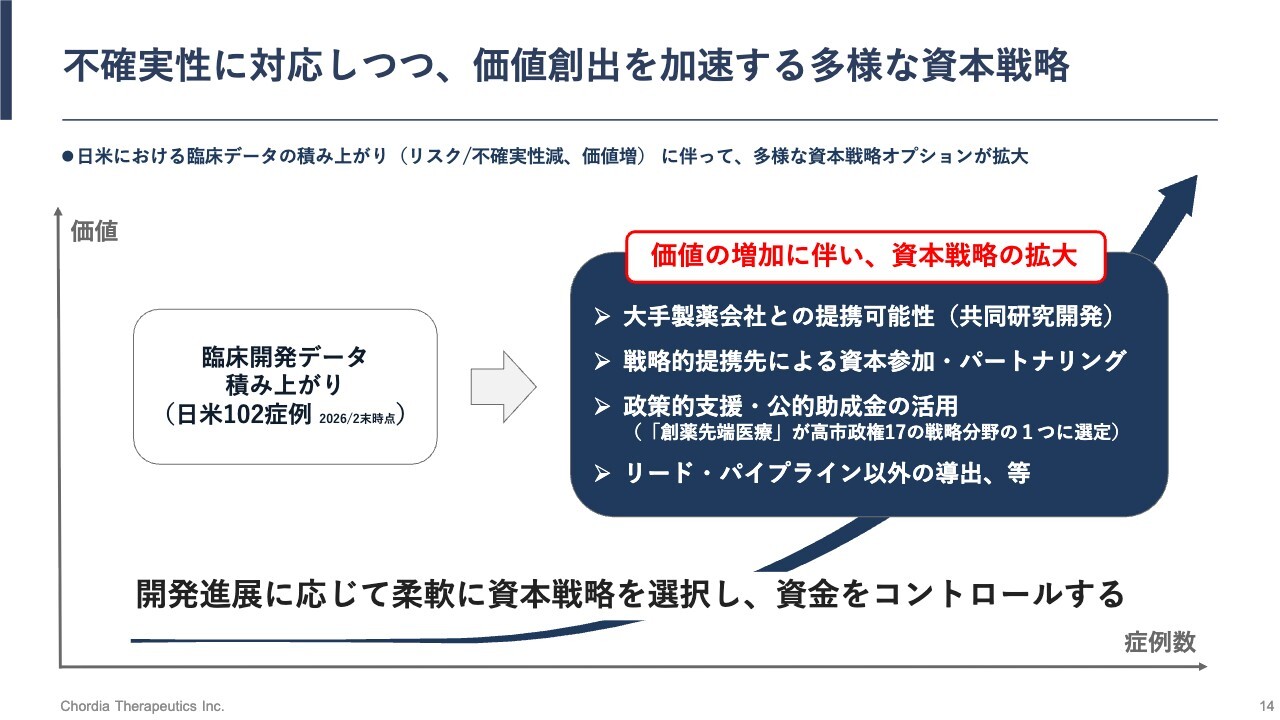
当社の資本戦略についてです。長期にわたる研究開発を支えるため、開発進展に応じて柔軟に資本戦略を選択し、資金を適切に管理していくことを想定しています。
開発の進展は、臨床開発データの積み上がりによって評価が可能であると考えています。
当社のリード・パイプライン「rogocekib」は、日米において102症例への投与を実施しており、その実績データが「rogocekib」の価値を示していると捉えています。
先行投資によって臨床データを蓄積し、パイプラインの価値を向上させ、次の臨床試験を実施するための資金を確保する計画です。
資本戦略としては、現在実施中の新株予約権による資金調達に加え、大手製薬会社との共同研究開発、戦略的提携先による資本参加、政策的支援・公的助成金の活用、リード・パイプライン以外の導出などを検討しています。
政策的支援については、「創薬先端医療」が高市政権の17の戦略分野の1つに選定されています。日本が世界に誇る創薬力の維持・発展のために、当社も貢献できると自負しています。
グローバル市場に挑む ~Chordiaのグローバル展開とAML市場~
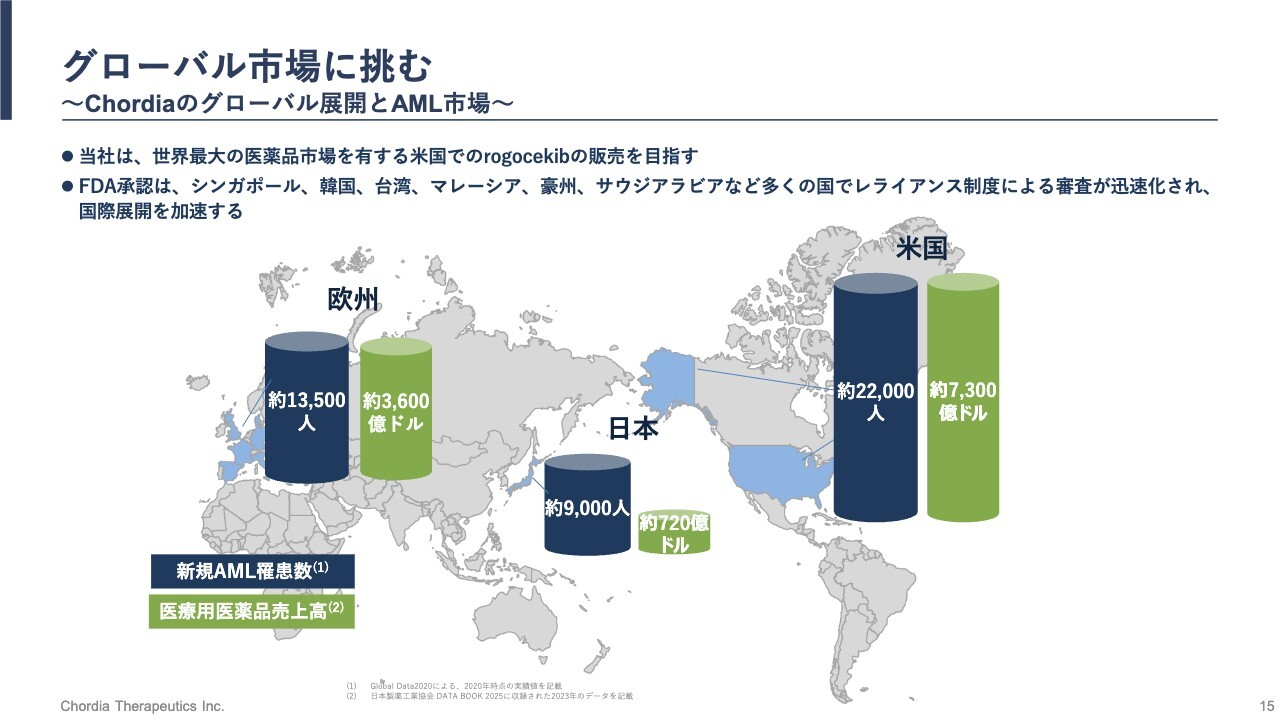
当社は覚悟を持ってグローバル市場に挑んでいます。現在、「rogocekib」の臨床開発は米国で実施されています。これは、米国が世界最大の医薬品市場を有しているためです。日本、欧州、米国を比較すると、米国には人口に比例して患者数が多く存在します。
例えば、当社が注力している急性骨髄性白血病(AML)の患者数については、毎年、日本では約9,000人、欧州では約1万3,500人、米国では約2万2,000人と報告されています。日本と米国の比較では、米国の患者数は日本の約2.5倍に上ります。
一方、医療用医薬品の年間売上高においては、その差はさらに大きく、日本では約720億ドルに対して米国では約7,300億ドルと、10倍以上の差がついています。
当社は、日本を代表する世界的な研究開発型バイオテック企業を目指し、米国での開発活動を継続しています。
2026年8月期に向けての優先事業目標の進捗
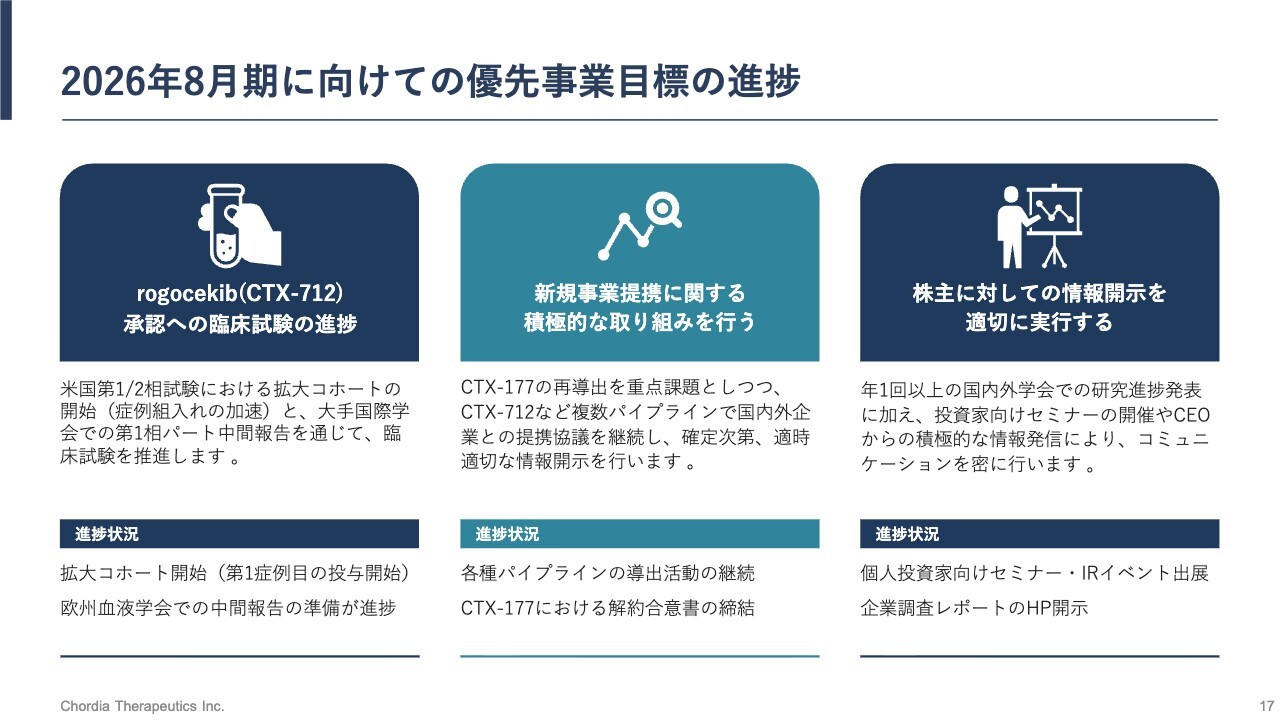
事業の振り返りと今後の見通しについてお話しします。まずは2026年8月期の優先事業目標の進捗状況です。
「rogocekib」は拡大コホートを開始しており、用量漸増パートの成績を今年6月の欧州血液学会で発表する予定です。
また、事業開発活動は「CTX-177」を中心に進めています。これらの進捗については、適切なタイミングで株主や投資家のみなさまに発信していく方針です。
情報開示にも積極的に取り組んでおり、イベントへの登壇や企業調査レポートのホームページ上での開示を進めています。
今後の主要注目ポイント
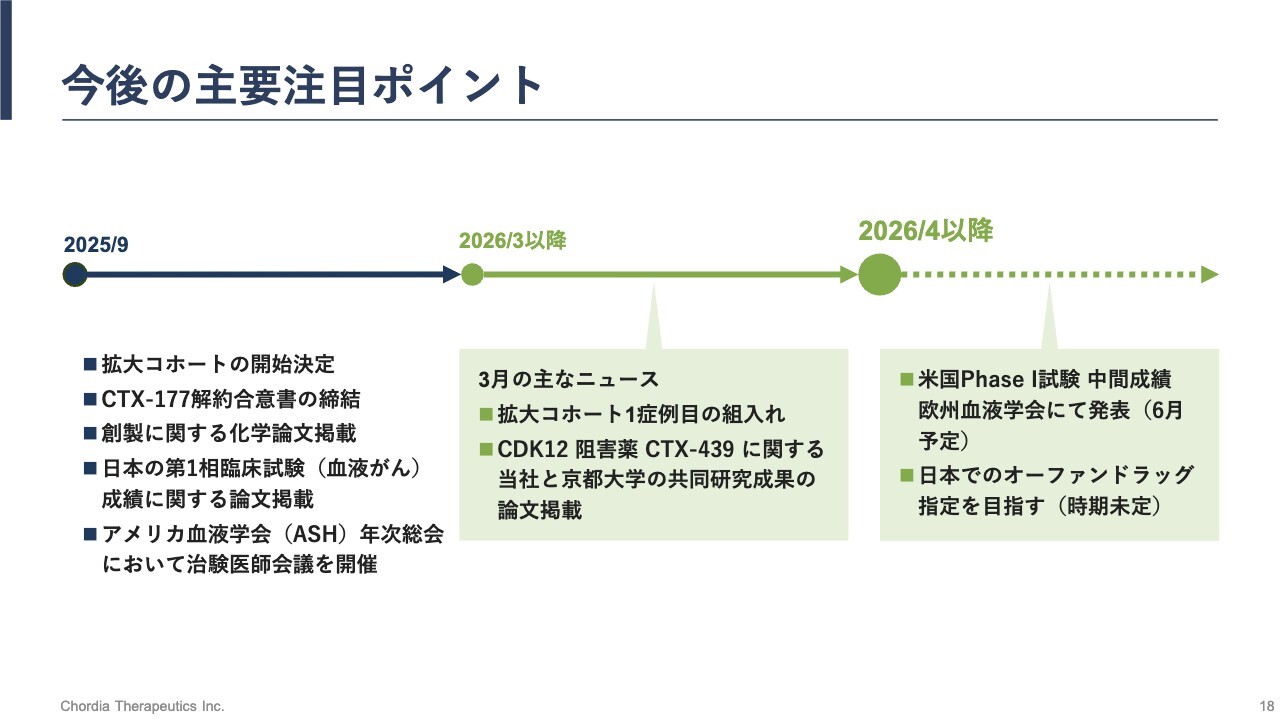
スライドには、これまでご説明した、今後注目していただきたいポイントをまとめています。「rogocekib」の開発を着実に進めていきますので、ご注目いただければと思います。
当社の経営理念と2030年ビジョン

当社の経営理念と2030年ビジョンについて、ご紹介します。
当社は、日本に本社を構えるバイオテック企業として、既存薬とは異なる働きをする新しい抗がん薬を世界中のがんと闘う患者さまに届けることを使命としています。患者さまやそのご家族が「明日になれば、今日よりもより良い治療を受けられる」と感じられる、「明日に希望を感じる社会の実現」を目指しています。
上場することで、より多くのみなさまに支えていただいています。新薬を創出し、世界的なバイオテック企業として成長していきたいと考えていますので、引き続きのご支援をどうぞよろしくお願いします。
本日はご清聴いただき、ありがとうございました。
質疑応答:「rogocekib」の学会発表の注目ポイントについて
質問者:「rogocekib」についての質問です。今年6月に欧州血液学会でPhaseI試験の中間成績を発表するとの
新着ログ
「医薬品」のログ





