ジェイファーマ株式会社(520A)新規上場記者会見
ジェイファーマ上場会見、独自開発のLAT1阻害剤で世界へ ブロックバスターを目指す
会社概要
設立:2005年12月
事業内容:「SLCトランスポーター」を標的とした薬の開発
登壇者名
ジェイファーマ株式会社 代表取締役社長 𠮷武益広 氏ジェイファーマ株式会社 取締役CFO 藤本裕 氏
上場記者会見
𠮷武益広氏(以下、𠮷武):ジェイファーマ代表取締役社長の𠮷武です。本日はお忙しい中、当社の上場記者会見にご参加いただき、誠にありがとうございます。
本日、無事に東京証券取引所グロース市場へ上場することができました。この機会に、当社の事業内容について簡単にご紹介します。
みなさまの中には医薬品を専門とするバックグラウンドの方もいらっしゃいますが、バイオ関連の企業は少しわかりにくい部分があると思います。そのため、私なりにできる限りわかりやすくご説明したいと考えています。
1 会社の事業内容について
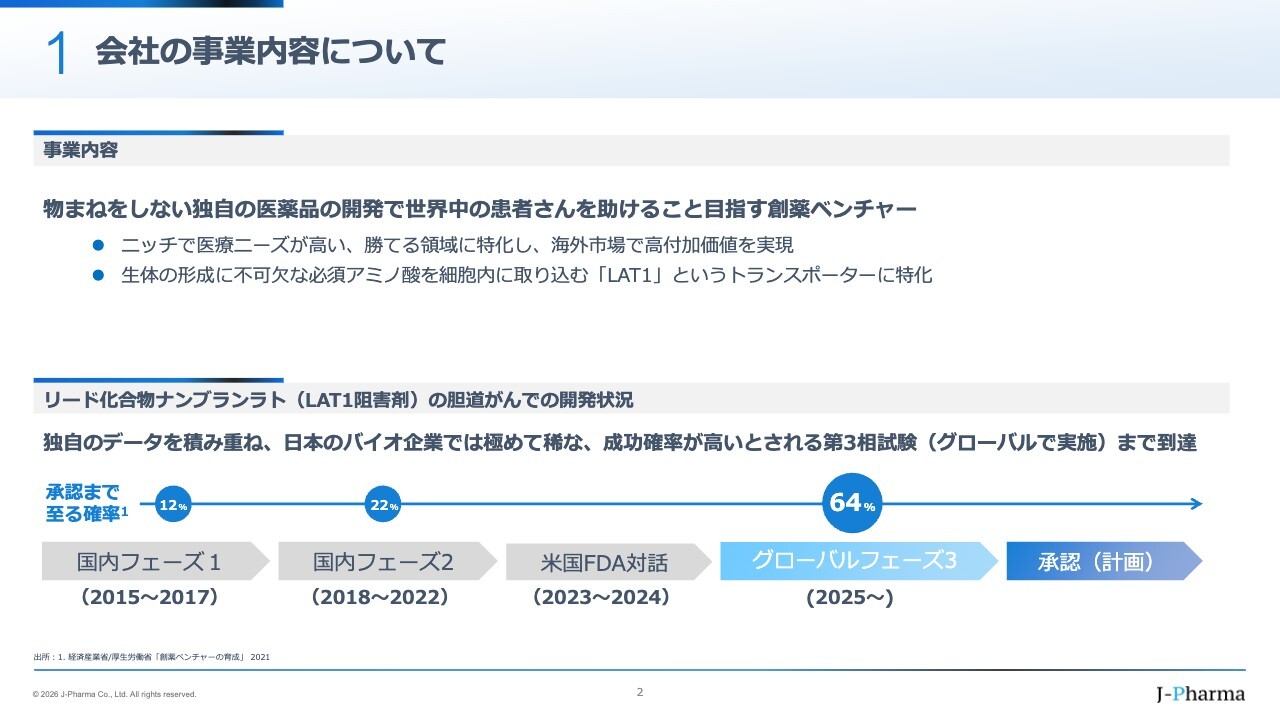
私どもの事業は、物まねをしない独自の医薬品を開発し、それを世界中の患者のみなさまに届けることです。
「独自」とは、創業者である遠藤仁が発見したLAT1という細胞が増殖するために不可欠なアミノ酸を細胞外から細胞内に取り込む入口に対する薬を開発していることを指します。これをベースに、「この領域でなら勝てる」と自信を持つニッチ分野で国際的に展開し、海外市場で付加価値をつけることを当社の事業としています。
スライド下部に、医薬品の開発ステージを示しています。医薬品の開発について、私はよく山登りに例えます。
例えば、5年から7年かけて薬を発見し、毒性試験を実施して、ようやく山に登り始める段階がフェーズ1です。その後、物資を蓄えながらさらに上を目指す段階がフェーズ2、そして最後にフェーズ3をグローバルで進めることにより、日米欧で医薬品を同時に開発し、市場に投入します。
このような取り組みにより、ブロックバスターのような大規模な医薬品に成長させることを目指しています。
LAT1阻害剤:開発パイプライン:2026年3月現在

当社の医薬品の開発パイプラインです。これは、どのようなキャラバン隊を当社が保有しているかを表しており、現在2つのキャラバン隊が進行中です。それが「ナンブランラト」と「JPH034」です。
これらはFDA(米国食品医薬品局:Unites States Food and Drug Administration)の厳格な評価を経た上で、グローバルな臨床試験に入っています。特に「ナンブランラト」は、すでにFDAとすべての試験内容について合意しており、臨床試験を詰めることができたら承認につながるグローバルフェーズ3に昨年12月から入っています。
太陽のように患者に寄り添う抗がん剤の開発

私どもはグローバルな視点で「新しい薬のコンセプトとは何か」を考えた時に、「患者さまに寄り添うような、太陽のような薬はないのだろうか」と思いました。
がん治療で化学療法を行うと、髪の毛が抜けたり、爪が傷んだり、味覚を失うといった重い副作用により、薬が効いているのに治療を中断せざるを得なくなる現実があります。
当社が開発する薬剤は、フェーズ2のデータから副作用が非常に少ないことが確認されており、患者さまが長期間服薬することで、より長く生きることが期待できます。最期の時間をご家族と過ごせるような薬を作りたいということで、私どもは「太陽のように患者さまに寄り添う抗がん剤」と呼んでいます。
L型アミノ酸トランスポーター1(LAT1)
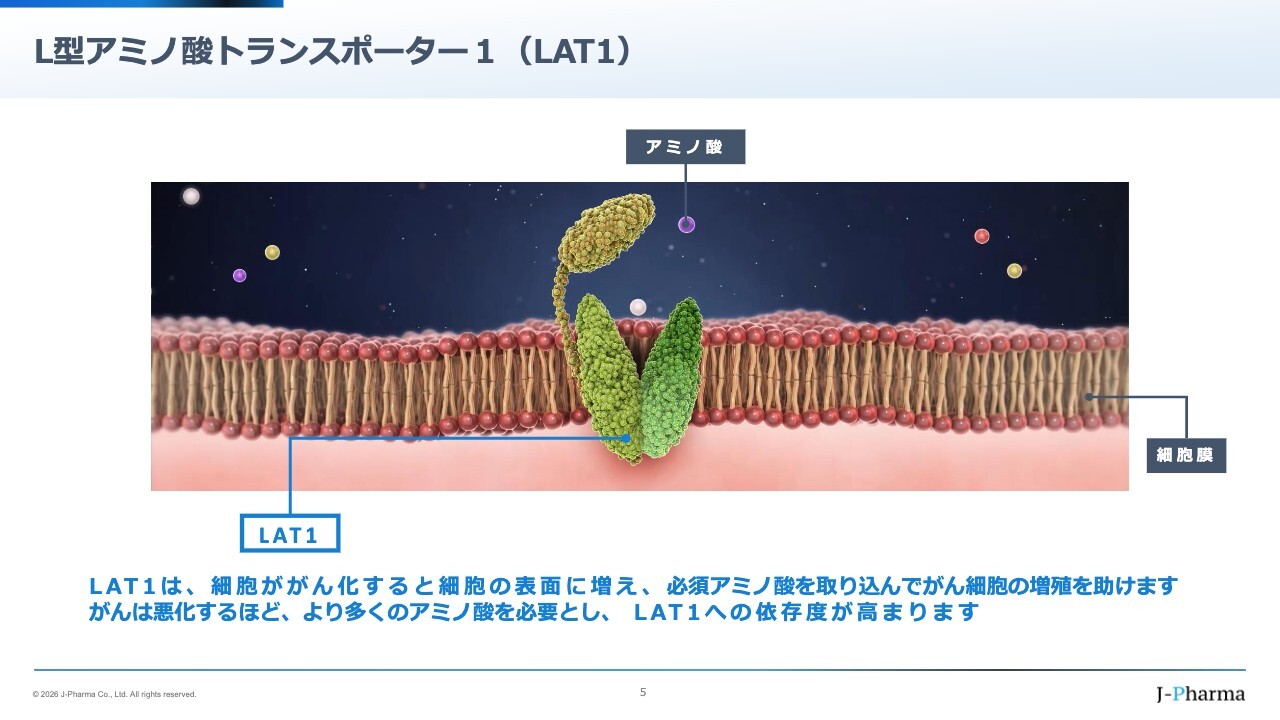
私どもがターゲットとしているLAT1についてご説明します。スライドに掲載している図の中央に、細胞膜が描かれています。細胞膜は外部からの侵害を防ぐために非常に強固に作られています。しかし、栄養を取り込む必要があるため、さまざまな栄養を取り込む入口があります。これをトランスポーターと呼びます。
正常細胞ががん化すると、通常はグルコースで生きている細胞が、アミノ酸をより多く必要とするようになります。がん細胞は5倍から8倍ものアミノ酸を取り込み、急速に増殖していきます。さらに、がんが進行するとより多くのアミノ酸が必要になると言われています。
トランスポーターは、イソギンチャクのように動きながら栄養を取り込みますが、図の中央に示しているヘッジの部分に薬剤が入り込むと、動きが停止します。私どもはこのようなところまで突き詰めて、『Nature』にも研究成果を掲載しています。
これをベースに開発した医薬品が「ナンブランラト」です。
L型アミノ酸トランスポーター1(LAT1)と、当社開発品ナンブランラト
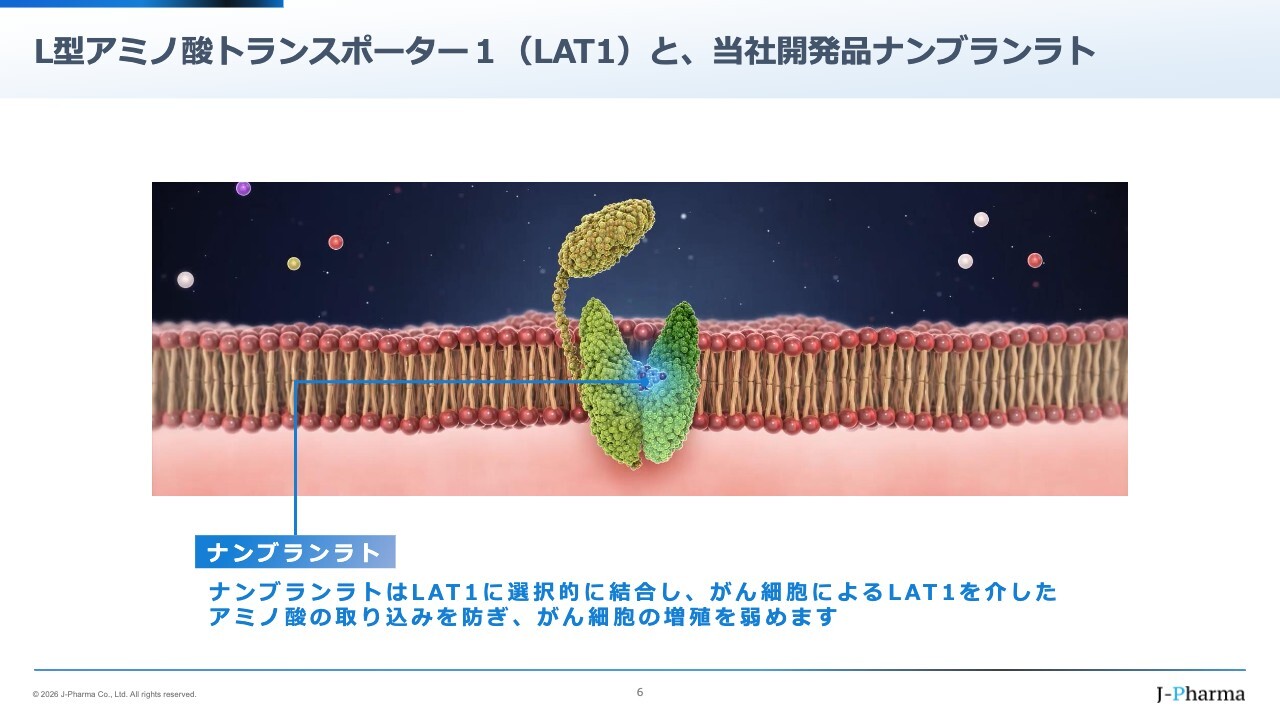
「ナンブランラト」は私どもの初の医薬品で、インディケーションとして胆道がんの治療を目的に開発しています。
胆道がん - 患者数は少ないが、極めてアンメットニーズが高いがん種
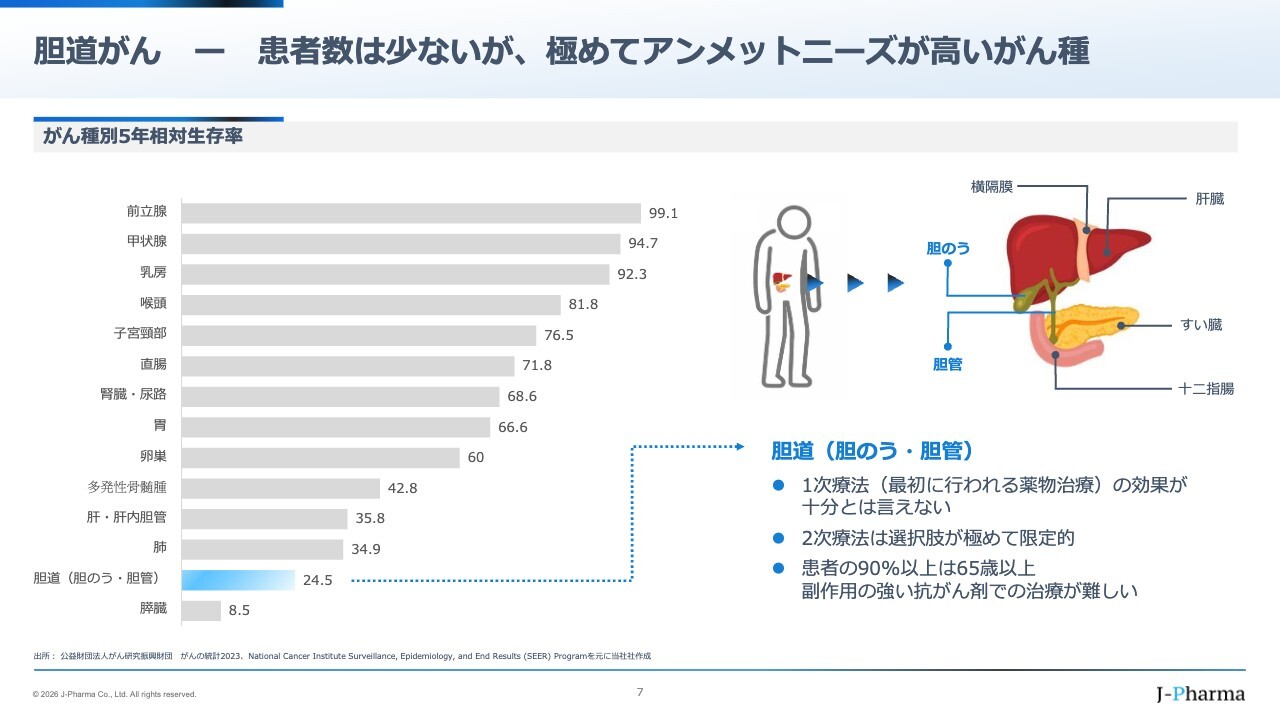
胆道とは、スライド右側の図に示しているとおり、肝臓から胆汁を取り出し、胆のうで濃縮した胆汁を十二指腸まで運ぶ管です。十二指腸の乳頭部で膵臓から来る膵液と合わさり、食べ物の消化を助けます。
しかし、管は非常に脆く、基底膜による支えがないため、がんが発生するとすぐに外部へ広がり、転移してしまいます。したがって、胆道がんは見つかった時点で多くの場合ステージ3Bまたは末期の状態で、手の施しようがないケースがほとんどです。
また、余命は約1年で、スライド左側のグラフに示しているとおり、5年生存率は膵臓がんに次いで低いとされています。さらに、胆道がんは65歳以上の高齢者に多く見られ、患者さまが薬の副作用に耐えられず、効果はあっても治療を途中で断念してしまうことも少なくありません。
このような中で、私どもの薬を継続的に使用することで患者さまに長く生きていただけることを立証するため、現在グローバルで臨床試験を進めています。
2026年3月時点で東証グロースに上場している創薬ベンチャーのうち、日本で自ら創製した化合物のデータを積み重ねてグローバルフェーズ3まで進めている唯一の事例(当社調べ)

スライドに、これまでの臨床試験の経緯を模式化しています。先ほどお話ししたキャラバン隊が始まり、フェーズ1では5種類の異なるがんの患者さまにご協力いただきました。
その中で、胆道がんだけが「なぜこれほど効果があるのか」とダイヤモンドの原石のように感じさせる結果を示しました。これが本物のダイヤモンドの原石であるかを確認するため、4年間をかけて日本で100人以上の患者さまにご協力いただきました。
その結果、本当にダイヤモンドのように輝く価値がある薬であり、副作用も少ないことを立証しています。
そして、スライドに記載しているとおり、アメリカの科学誌や学会でそのデータを発表しました。そのデータを基にFDAと2年間にわたり交渉を重ね、FDAからは次の2点について指摘を受けました。
1つ目は、この薬剤をどのような患者さまに、どのように投与すれば長生きできるのか、その基準を明確にするという点です。2つ目は、本当に長く生きられることの指標となるバイオマーカーを見つけるという点です。
当社はこの2つについて取り組みを進め、バイオマーカーではありませんが指標を見つけ出し、それを組み込んだプロトコールでFDAの合意を得ることができました。その結果、グローバルフェーズ3が現在進行中です。
先ほどお伝えしたとおり、日米欧での同時開発および同時承認を目指し、1,500億円以上の売上を目指すブロックバスターに育て上げていきたいと考えています。
2 現在の業績動向と今後の業績見通し
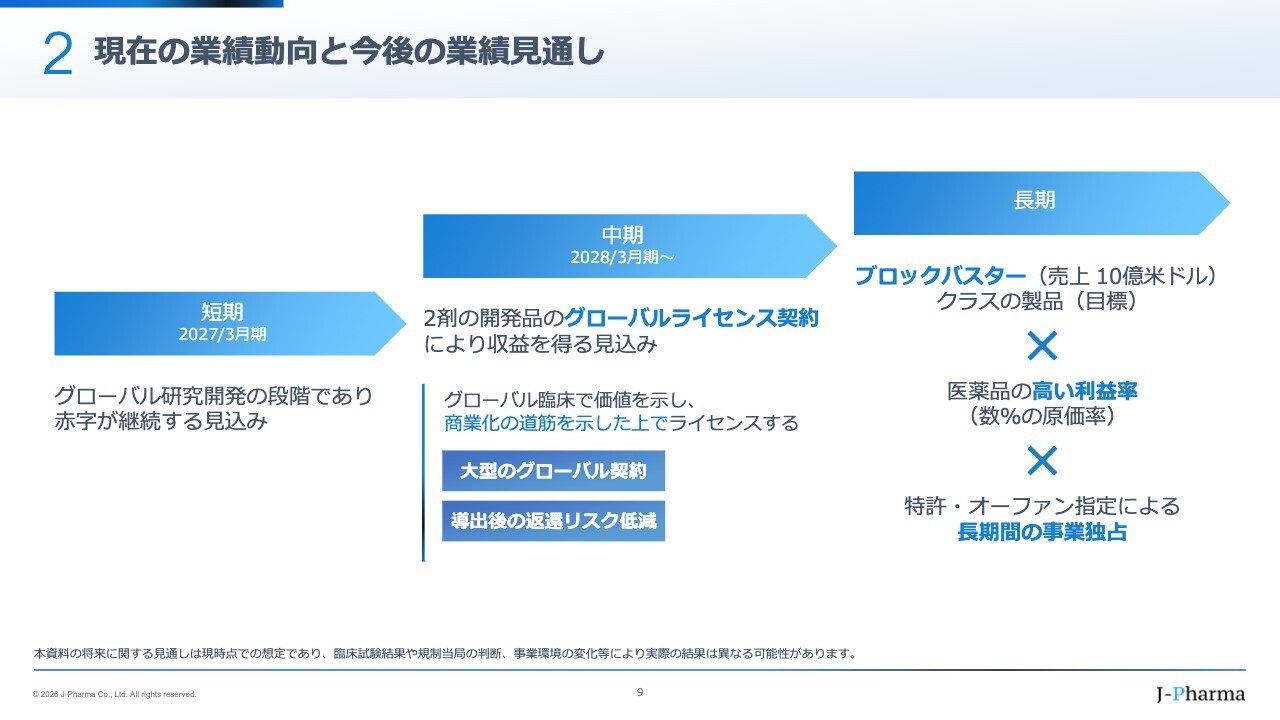
上場しましたので、業績についてお話しします。「バイオベンチャーは利益を上げにくく、評価が難しい」とよく言われます。ただし、私どもは今回の上場で調達した資金を活用し、今後2年間はグローバル試験を主軸に開発を進めていきます。
現在の手持ち資金と今回調達した資金を活用することで、市場から新たに資金を調達しなくても、グローバルフェーズを十分に推進できると考えています。
また、最後まで自力で進めるのではなく、確実に承認される目処が立つところまで自力で進める計画です。医薬品の開発では、自力で進めず他者に引き継いでも、最後まで育ててくれる保証はほとんどありません。特に欧米の企業では、途中で中断されるケースも多いのが実情です。
そのようなことがないように、「ここまで育てればビジネスになる」という段階まで自力で育て上げ、それをライセンスアウトしていきます。その上で、日米欧で開発を一緒に進めてくれるパートナーが見つかれば、ブロックバスターとなることも難しくないと考えています。
医薬品は非常に利益率が高く、特許で保護されている間は独占権を維持できます。そのため、中期から長期に移行する段階で会社を黒字化し、株主のみなさまに還元する体制を整えていきたいと考えています。
3 経営視点でのジェイファーマの強み - 日本発の革新的創薬をグローバル市場へ

当社の強みについてお話しします。1つ目は、LAT1阻害剤を手がけているのは世界で当社だけであることです。2つ目は、それを自社で独自に開発していることです。これにより、最終的にはグローバルでの承認を目指しています。
私が製薬会社に入社してから約40年が経ちますが、ビジネスのシステムはすっかり変わりました。
現在では、FDAやEMA(欧州医薬品庁:European Medicines Agency)が承認する医薬品の85パーセント以上が新興のバイオベンチャーにより開発され、大手企業がそれを育てるという時代になっています。しかし、日本のバイオベンチャーから出た独自の医薬品がそこまで育った例は1件もありません。
そのため、「日本のバイオベンチャーは信じられない」「日本のバイオエコシステムは動いていない」と言われることが多い状況です。私どもはなんとかこの潤滑油となり、勝てるニッチ分野に取り組み、独自のサイエンスで開発を進めていくという戦略をとっています。
世界トップレベルの研究者から、研究成果をグローバルに送り出す医薬品開発専門家にバトンタッチ

当社の創業者である杏林大学名誉教授の遠藤仁がLAT1という分子を発見し、「ナンブランラト」を合成できるところと一緒に作りました。先ほどお話ししたフェーズ1でキラリと光るダイヤモンドを1個見つけるまで、遠藤が独自に研究を進めました。
日本では、経済産業省が所管する国立研究開発法人新エネルギー・産業技術総合開発機構(NEDO)や国立研究開発法人日本医療研究開発機構(AMED)による橋渡し資金が非常に発達しています。
これらの資金を活用し、「キラリと光る」レベルまで来たところで私にバトンタッチされました。私は、これまでのグローバルでの医薬品開発経験を基に、グローバルでの開発経験を有する方々を採用しました。少し高齢の方々ですが、力を合わせ、7年の歳月を要してここまで会社を運営してきました。
当社のグローバル開発を支える世界最先端の大学・研究機関の医師・科学者
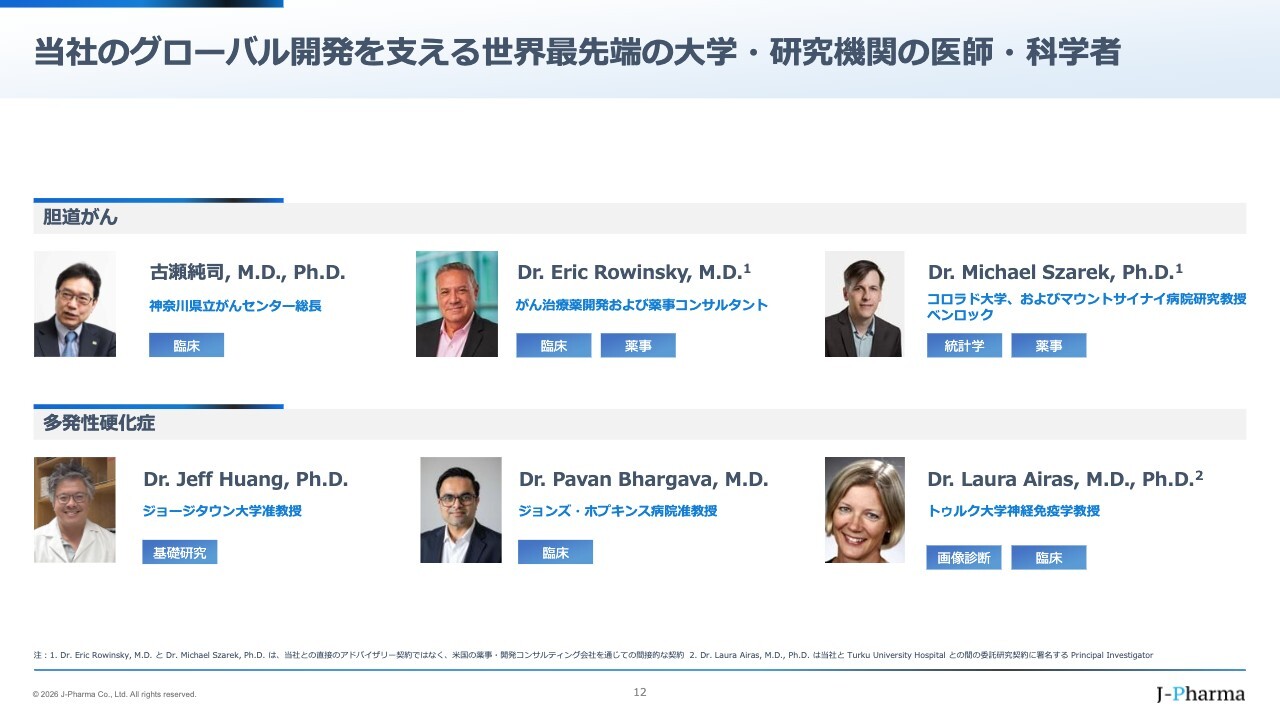
神奈川県立がんセンターの総長である古瀬純司先生は、胆道がんや膵臓がんの日本における一番の権威と言われています。古瀬先生にフェーズ1の日本のすべての試験を監督していただき、この方の紹介を通じて多くの先生方と知り合うことができました。
例えば、アメリカでの開発を担当していただいているEric Rowinsky氏と、マウントサイナイ病院研究教授で統計学を専門とするMichael Szarek氏の2人がFDAで私と共に協議を行いながら、モデルを構築してくれました。さらに、ジョージタウン大学やジョンズ・ホプキンス病院の先生方にも協力していただいています。
このように、新しいモノを作れば、世界のトップクラスの先生方が興味を持って一緒に働いてくれることを実証してきました。
4 今後のビジネス展開 - ニッチでアンメットニーズが高い疾患領域を狙う
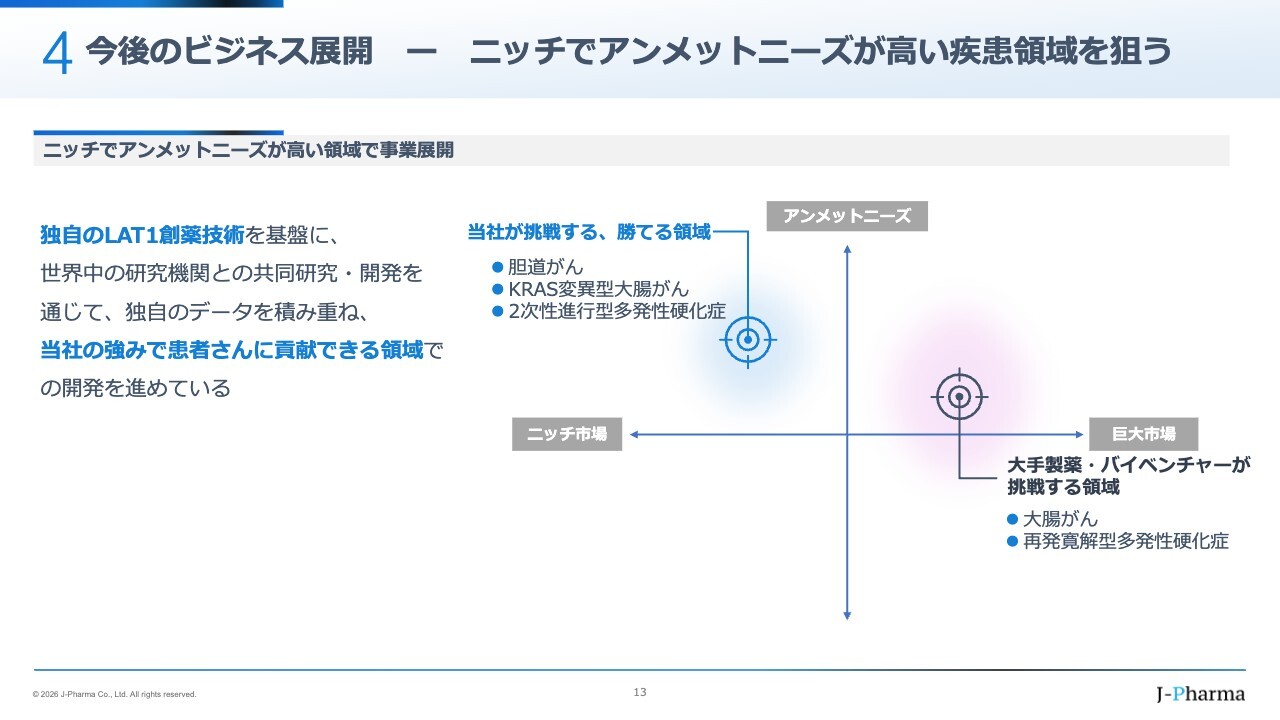
今後の展望についてです。私どもは勝ち筋が見えたニッチ分野に特化し、日本国内だけで展開するのではなく、早い段階からアメリカやヨーロッパといった薬事行政や専門家の評価が厳しいグローバル市場で育てることで強化し、ビジネスにつなげていく方針です。
胆道がんで目処が立つ状況に到達した場合、次はアメリカの著名な大学の先生から、医薬品が非常に効きにくいとされるKRASの遺伝子変異を持つ大腸がんの研究に一緒に取り組むことを3年間ずっと提案していただいています。
さらに、2次性進行型多発性硬化症については、有効な薬がほとんどないと言われています。この分野では、アメリカのジョージタウン大学の先生と7年間にわたって共同研究を進めてきました。その研究から生まれた薬が、今月アメリカで臨床試験を開始しています。
このように、独自で模倣されることのない技術やデータを持っていると、世界中のさまざまな方々が共に働いてくれるようになります。このように生まれた研究や技術の芽を大切に育て、それをビジネスにつなげながら、日本のバイオエコシステムを活性化させたいというのが、私たちの強い希望です。
質疑応答:「ナンブランラト」「JPH034」の開発資金について

質問者:この度は上場おめでとうございます。「手持ちの資金と今回の上場で調達した資金で、2剤の開発が可能」というお話がありました。現在、臨床試験が進んでいるのは「ナンブランラト」と、最近開始した「JPH034」です。
こちらは、一昨年から昨年4月にかけて調達したAMEDの資金を含む57億7,000万円と、今回の上場で調達された資金で、「ナンブランラト」のグローバルフェーズ3と「JPH034」のフェーズ1を完了できるという意味でしょうか?
𠮷武:実際に57億7,000万円を調達し、残っている手持ち資金に今回集めた26億円を加えることで、臨床プログラムを進める予定です。
フェーズ3に関しては、Part AとPart Bの2段階があります。Part Aでは、「日本人のデータだけでなくアメリカ人のデータも組み込んでほしい」というFDAのリクエストに基づき、アメリカ人に最適な用法・用量を比較検証します。こちらは、約120名の患者さまを対象に試験を行います。
日本ですでに100名以上の患者さまを対象に試験を実施していますので、アメリカでの120名分を加え、トータルで200名を超える患者さまによる試験で立証することになります。これにより、どのような製薬会社からみても信頼性が高く、「次に進むのではないか」と思っていただけます。
Part Bでは、日本、韓国、アメリカ、ヨーロッパの5ヶ国から6ヶ国で並行して試験を進める計画です。こちらでは、一緒に取り組みたいと考えていただいている製薬会社やバイオテクノロジー関連の会社と進めたいと考えており、すでに数社から手を挙げていただいています。
彼らもPart Aのデータを確認したいということで、並行して進めながら、秘密保持契約のもとで開示を進めていきます。このPart Aは、今回の資金計画に組み込まれています。
「JPH034」については、これまではAMEDの潤沢な資金ですべて賄ってきました。ここから今年の年末までにかかるフェーズ1の費用については、自社の資金で対応する予定です。
また、「ナンブランラト」は、免疫チェックポイント阻害剤と併用することで非常に高い相乗効果を発揮します。
これは当社のデータだけではなく、中国の研究者も発表しています。さらに、「大腸がんの研究を一緒に進めたい」と提案していただいているアメリカの先生も、まだ正式には発表していませんが、大腸がんの分野で効果を立証しています。
当社は横浜市鶴見区にいる中でも、声をかけていただくチャンスを得ることができました。通常の製薬会社で考えれば、約10分の1程度の経費でここまで来たと考えています。以前勤めていた会社で多額の資金を使えた頃と比べると、いろいろな研究者や日本およびアメリカの補助金制度の支援を受けつつ、限られた資金で進めてこられたと実感しています。
質疑応答:「JPH034」の導出時期について
質問者:MS(多発性硬化症)に対しても開発を進めていると思います。今回、AMEDやプレIPOでの資金調達により、フェーズ3のPart Aまで
新着ログ
「医薬品」のログ





