提供:オンコリスバイオファーマ株式会社 事業説明会
【QAあり】オンコリス、腫瘍溶解ウイルス内視鏡投与で特許取得 「OBP-301」は米国の臨床試験中間評価で食道がん完全奏効を確認
事業領域
浦田泰生氏(以下、浦田):オンコリスバイオファーマ代表取締役社長の浦田です。よろしくお願いします。ご多忙の中、当社の株主総会のみならず、毎年行っている事業説明会にもご参加いただき、誠にありがとうございます。
当社は創業21年を迎えて、ようやく手塩にかけてきた「テロメライシン(OBP-301)」がPMDAの審査にかかり、いよいよ発売するという我々のゴールが見えてきました。ただし、そのゴールを達成するためには、まだいくつもの山を越えなければならないと感じていますし、本日の株主総会においてもみなさまからたくさんのご質問をいただき、非常に身が引き締まる思いです。
この21年間、がんのウイルス療法と重症ウイルス感染症治療薬などのウイルス創薬を手がけてきました。このようなウイルス創薬を手がけている会社は世界を見ても非常にまれで、当社のみが行っている事業モデルです。
「テロメライシン」の第2世代である「OBP-702」もいよいよ臨床試験が近づいてきました。スライド右側にある「OBP-601」はもともと抗エイズ薬であったものが、ドラッグリプロファイリングという他の考え方によって、神経難病治療薬として開発されます。このように、ウイルス創薬がどんどん発展している状況です。
会社概要
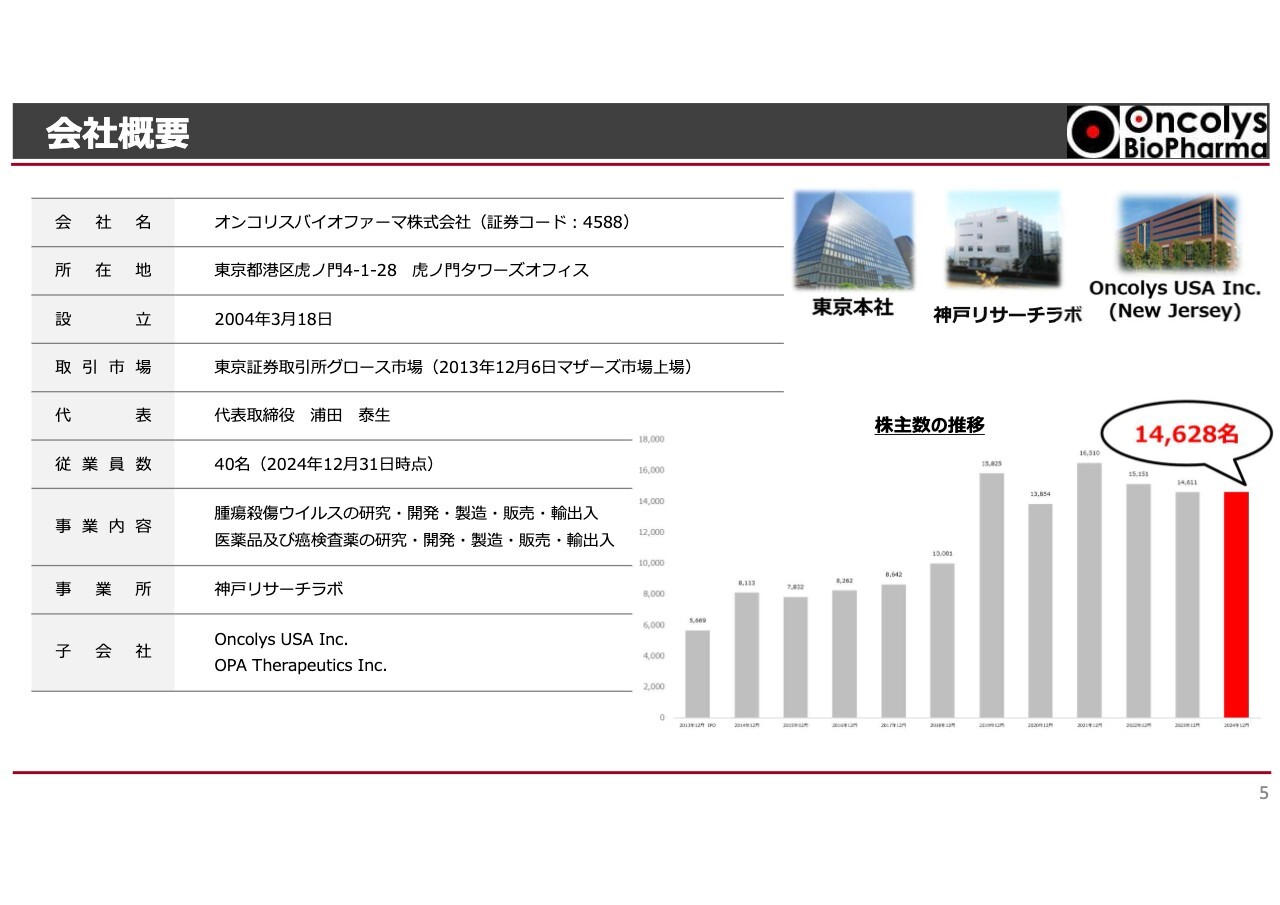
株主さまも現段階では1万5,000名弱と、大変多くの方にご支援いただいています。東京本社、神戸リサーチラボ、アメリカのニュージャージーにあるOncolys USAの3拠点で「テロメライシン」の価値を最大化するための活動を行っています。
ガバナンス体制

ガバナンス体制です。いろいろな能力を持った人材が当社に続々と集まってきています。その中で、執行役員をご紹介します。
久保田俊之氏:4月1日より生産調整・メディカルアフェアーズ担当執行役員に就任する久保田と申します。よろしくお願いします。
「テロメライシン」の承認申請に向けて、高品質なウイルス製剤の製造と安定供給ができる体制を整えることを第1の優先課題としています。そして市販後には「テロメライシン」の適正使用、価値向上を目指して、より一層準備を整えて邁進したいと思いますので、ご支援のほどよろしくお願いします。
田口めぐみ氏:人事担当執行役員を拝命する田口です。今期で4期目になります。現在、承認申請および承認申請後の事業領域拡大に向けて、組織体制の強化に取り組んでいます。
昨年は採用活動をベースに増員を見越した勤怠システムの入れ替え、社員の働き方改革に着手しました。本年度はそれらを継続しながら、人材育成の基盤作りやダイバーシティなどに力を入れていきます。引き続きご期待とご支援をいただきますようよろしくお願いします。
秦耕平氏:事業企画担当執行役員の秦です。「テロメライシン」の承認、販売開始に向けた活動について、株主のみなさまに十分にご理解いただけるよう発信していきたいと考えています。引き続きよろしくお願いします。
吹野晃一氏:メディカルサイエンス担当執行役員の吹野です。当社の創立記念日である3月18日に、いよいよ「テロメライシン」の先駆け総合評価相談を開始することができました。日頃より当社の活動にご理解、ご支援いただいている株主のみなさまに、あらためてご報告とお礼を申し上げます。
先ほどの株主総会では、実際にがんで苦しまれている患者さまの声を届けていただきました。1日も早く「テロメライシン」をがんの患者さまのもとへ届けられるよう、ラストスパートにさらに磨きをかけていきますので、引き続きご支援をいただけるよう、どうぞよろしくお願いします。
米尾哲治氏:経理・財務担当執行役員の米尾です。「テロメライシン」の承認申請によって一丸となって進んでいる当社を、裏側からしっかりと支えていきますのでよろしくお願いします。
浦田:このような体制で臨んでいきたいと考えています。当社は特に研究開発を重視してきましたが、これからも国際性豊かに、海外でのビジネス環境も含めて多様な人材で取り組んでいきたいと考えています。
パイプラインの状況
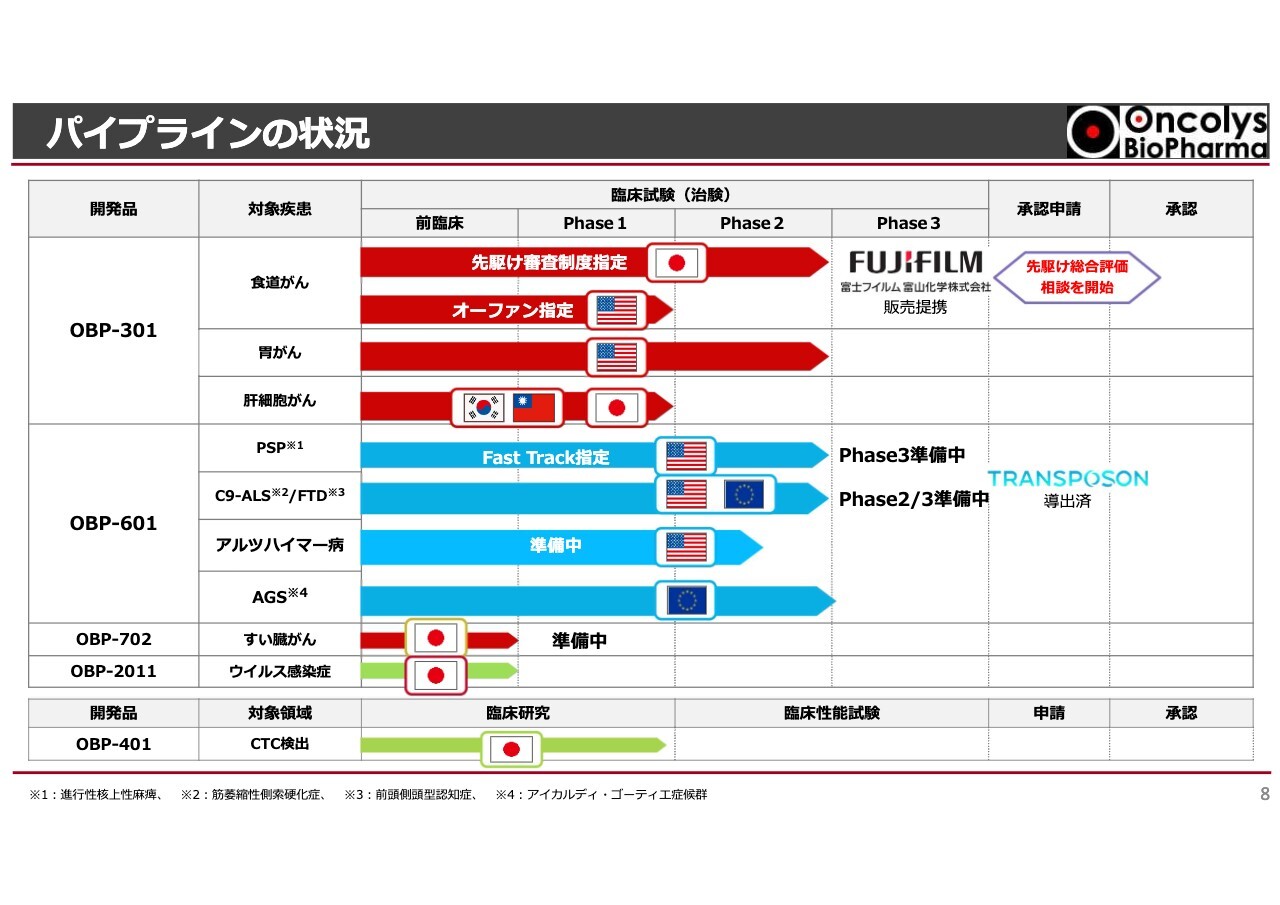
現在のパイプラインの状況です。みなさまもホームページなどでご覧になったと思いますが、スライド上部の赤いラインが「テロメライシン(OBP-301)」です。真ん中にあるブルーのラインは「OBP-601」を示しており、だいたいの開発品がPhase2まで近づいてきています。特に「テロメライシン」は日本国内で先駆け総合評価相談を開始しており、富士フイルム富山化学社と販売提携しています。今後、承認申請に向かって最善を尽くしていきます。
一方、後ほどご説明しますが、アメリカでは食道がんの臨床試験で非常に良い結果が出てきています。アメリカではすでにオーファン指定、要するに希少医薬品として指定されており、今後の臨床試験がどこまで進んでいくかという状況にきています。
「OBP-601」については、PSP(進行性核上性麻痺)という難治性の神経疾患やC9-ALS(筋萎縮性側索硬化症)などの病気で、Phase2、Phase3といった最終段階の臨床試験の計画が進んでいます。今回、アルツハイマー病という新しい適応にチャレンジするという情報がきており、こちらも臨床試験の準備中です。このように、当社のメインのパイプラインで、続々とステージが上がってきている状況です。
まだ小さいですが、「OBP-702」もいよいよ臨床試験が始められるという段階です。
腫瘍溶解ウイルスの競合状況
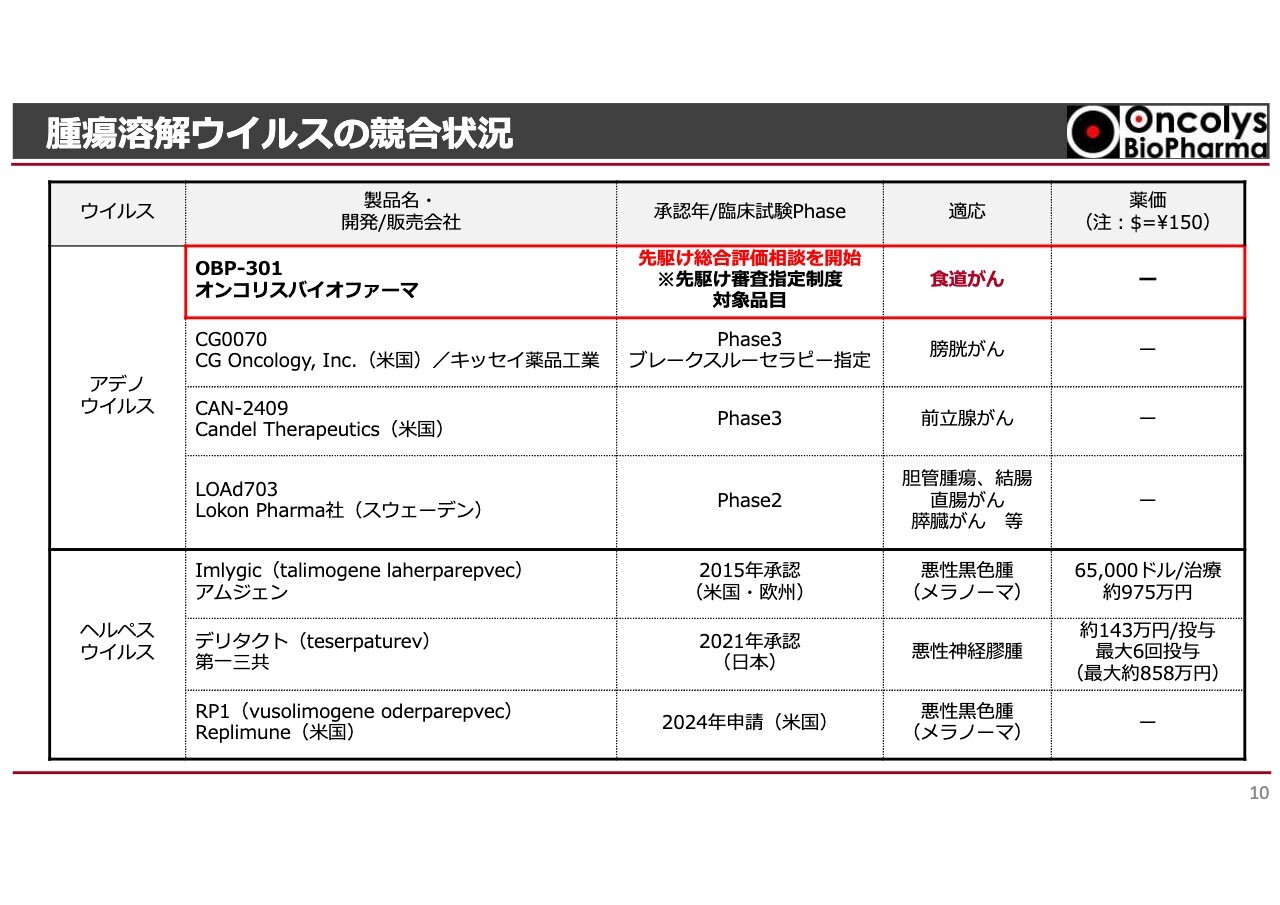
「テロメライシン」についてご説明します。「テロメライシン」の国際的な一般名は、少し難しいですが「スラタデノツレブ」です。現在、このような腫瘍溶解ウイルスは世界で40社から50社の会社が開発競争に入ってきています。特にスライド上段にあるアデノウイルスやヘルペスウイルスを使った開発が進んでいます。
最上段が当社です。2段目の「CG0070」という製品については、CG Oncology(旧Cold Genesys)社がキッセイ薬品工業社と組んで、膀胱がんに対して最終段階の臨床試験を行っており、アメリカではブレークスルーセラピー指定を受けています。
それ以外にも、Candel Therapeutics社、Lokon Pharma社などが、新しい技術を用いて前立腺がんや消化器系のがんに適応している製品を開発していますが、食道がんに適応する製品を開発している会社は、世界でも当社だけです。そのような意味では、オンリーワン、ナンバーワンを目指せる立ち位置にいると考えています。
またヘルペスウイルスが多く開発されていますが、アムジェン社の「Imlygic」という薬はすでにアメリカでメラノーマ(悪性黒色腫)の適応を取っており、日本では承認申請を諦めたのではないかという話を聞いています。第一三共社は「デリタクト」という薬を脳腫瘍の適応で2021年に販売しています。
今後、世界的にいろいろなウイルスが医薬品として登場してくる可能性がありますが、当社は食道がんに対して、まずは日本でナンバーワンを取り、世界でも唯一の食道がんの治療薬というポジションを目指していきたいと考えています。
101JP試験の概要 局所奏効率
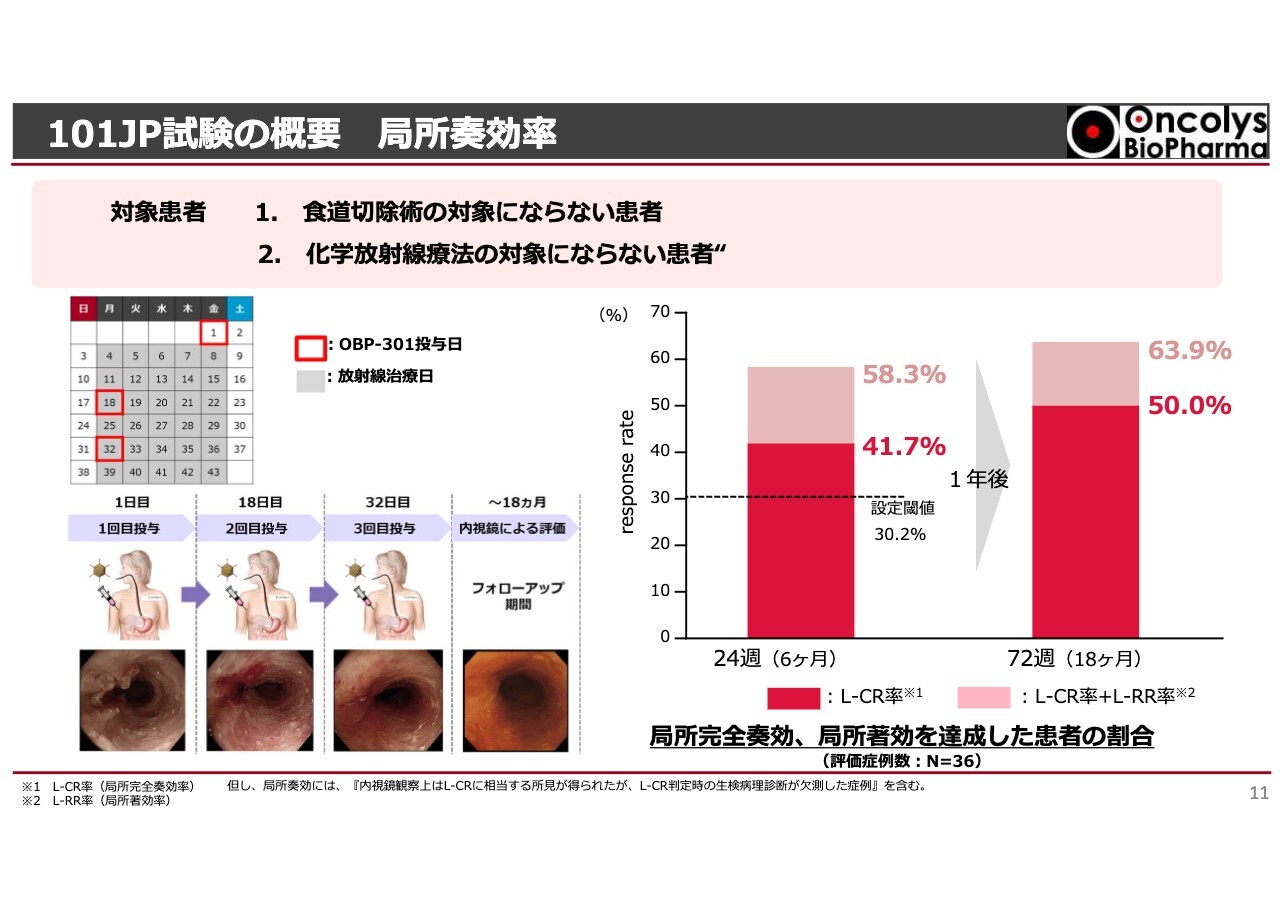
昨年もご説明したように、101JP試験は食道がんに対する局所治療として初めての臨床試験であり、放射線と併用します。特に化学療法が臓器障害があり受けられない方、あるいは術後の肝臓・腎臓の合併症が40パーセントぐらい出るような重いオペが受けられない高齢の方などに対して、「テロメライシン」を放射線治療と併用して、放射線治療を月曜日から金曜日まで毎日、テロメライシンは2週間おきに3回投与するという治療を行います。
治験開始から6ヶ月後の局所での完全治癒率は約42パーセントになりました。これは内視鏡ではつるつるで何も見えず、生検をしてもがん細胞が見当たらないという状態です。放射線を当ててがんが死滅し、その部分がケロイドのような瘢痕状態になっている人も含めると、だいたい6割がほぼ治っているという状況になっています。さらに、18ヶ月後の結果は局所の完全治癒率が50パーセント、少し瘢痕が残っている方も入れると約64パーセントの方が完全に治癒しています。
いろいろな文献や最近の調査によると、放射線単独治療での有効性は20パーセントから30パーセントだということがわかっていますので、「テロメライシン」を上乗せすると高い治癒率が得られて、広範囲な手術を避けることができ、重篤な副作用が出るような化学療法を受けなくてもいいという世界が作れるのではないかと考えています。
「テロメライシン」は内視鏡とカテーテルを使って、数分でがんの局所に少量ずつ、5箇所以上に注射して、そこにウイルスが局所で感染し、徐々にがんを殺していくという治療ですので、全身性の副作用はほとんど出ません。ただし、ウイルス感染はありますので、患者さまは投与されてから24時間ぐらいの間に、副作用として38度ぐらいまで発熱しますが、これは一過性で2日目、3日目ぐらいには普通の体温に戻ります。このようにほとんど副作用が出ないという大きなメリットも、治験からわかってきています。
臨床データの総括 生存率
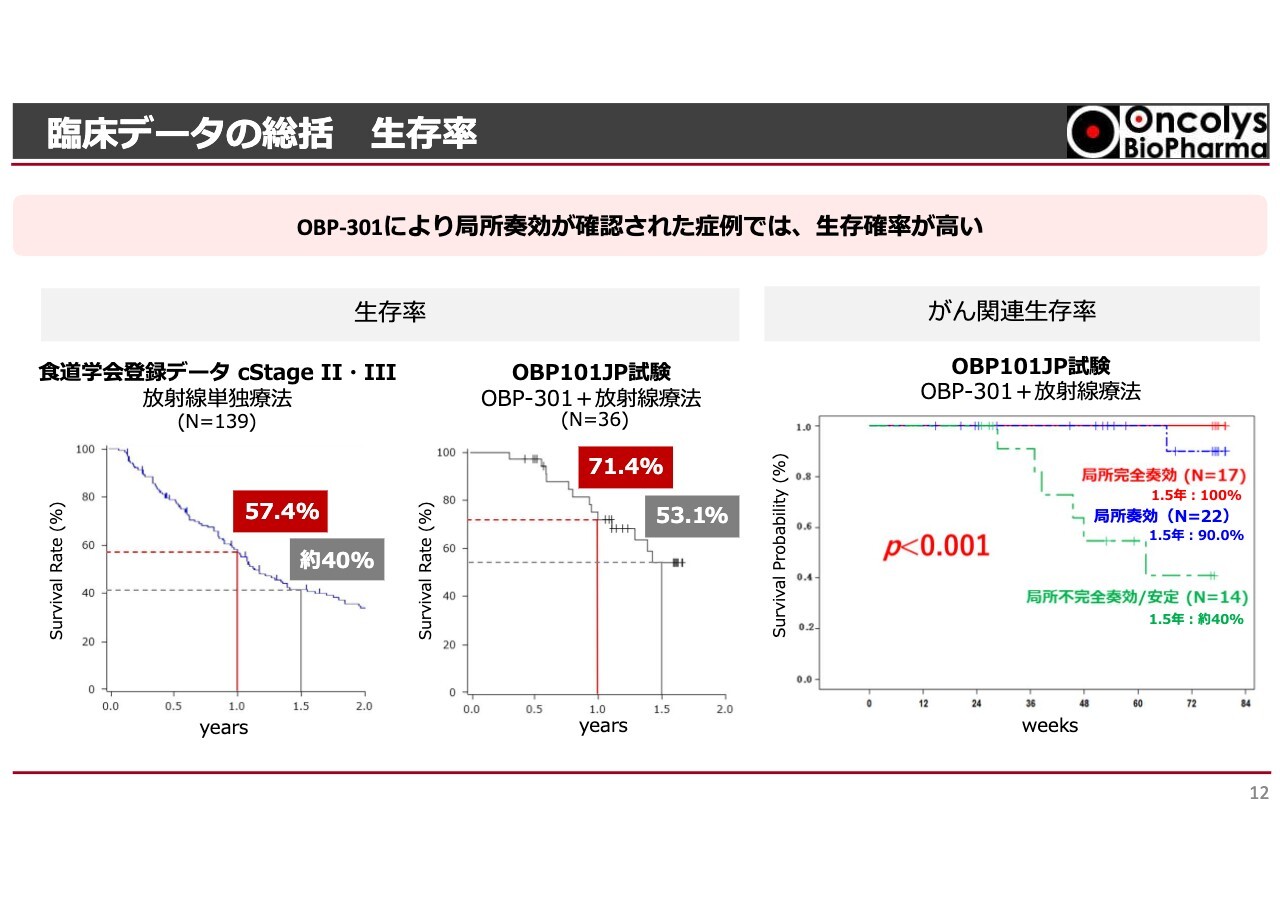
このような局所の治療が生存率に大きく影響するということは、食道学会でも認められています。スライド左側のグラフは、食道学会が20年ぐらい前に集めたステージⅡ、ステージⅢの食道がんの生存率曲線ですが、放射線単独では1年で約57パーセント、1.5年で約40パーセントの方が生存されています。逆に言えば、50パーセント、60パーセントの方が残念ながらお亡くなりになるという時代でした。
当社の「テロメライシン」を併用した放射線療法であるOBP101JP試験においては、全体の生存率は1年目に約71パーセント、1.5年後には約53パーセントという結果になっています。その中でも特に局所でよく効いた方で、例えば合併症や交通事故で亡くなる方を除いて、食道がんが転移して多臓器不全で亡くなるがん関連生存率の結果を検証すると、局所で治っている方は、1.5年後もほとんどが生存されています。
一方で、今回「テロメライシン」が残念ながらあまり効かなかったという例は、食道学会のデータと同じような生存率を示しているという結果が出ています。やはり「テロメライシン」で50パーセント以上の奏効された方は長期生存が見込まれるという良好な結果が得られた試験でした。今、この試験結果がPMDAで審査されています。
食道がん放射線Phase2試験の結論

スライドの内容は、ただいまご説明したとおりです。このような結果が1年以上前に出ており、PMDAとお話ししてきました。昨年、承認審査まで持っていきたかったのですが、残念ながら遅れました。その理由についてご説明します。
我々の「テロメライシン」は、再生医療等製品というカテゴリーに加えられています。厚生労働省から許可された再生医療等製品の中には、アンジェス社の遺伝子治療用製品(血管障害の治療薬)、テルモ社の「ハートシート」という心筋細胞を培養して心筋梗塞の部位に貼るという治療法がありますが、昨年の夏に、この2つの製品が相次いで市販後臨床試験で良い結果が出なかったというニュースが出ました。テルモ社は承認取り消し、アンジェス社は条件・期限付き承認を取り下げると判断したわけです。
このニュースが入ってきた時に、我々もちょうど審査を受けており、PMDAの姿勢が大変厳しくなって、今回の結果だけではなかなか次の段階に進めないというような話を何度もされました。ただ、過去の結果は非常に良かったですし、我々はこの臨床試験に携わった国内のいろいろな先生とPMDAに出掛けていき、「なぜこの結果が駄目なのか」という非常に激しい論争を繰り広げてきました。
最終的にわかったことは、PMDAは「治験の結果よりも、この治験が再現できるような、調査ではなく市販後の臨床試験計画書が必要だ」と伝えているということです。普通はこの段階でそこまで先の話をしないのですが、仮に承認した後に、どのような臨床試験があって、その臨床試験の方法が、PMDAが納得できるような試験計画なのかを先に審査したいという話が出てきました。
我々は至急先生方を集め、今回の臨床試験の反省点も含めて、どのような試験結果が良いのかを何度も話してきました。最終的に結論が出ましたので、3月18日に臨床試験の過去のすべてのデータおよび今後再検証する臨床試験、いわゆる市販後臨床試験計画をもってPMDAに書類を出し、ようやくそれが受け付けられて、先駆け総合評価相談に移行できました。
まだ審査結果待ちですので、今後いろいろな質問が出てくるのではないかと考えていますが、できる限り早いタイミングでPMDAに答えを出し、早く審査が進むように最善の努力をしていきたいと考えています。
CRT併用Phase1試験:ASCO-GIで発表
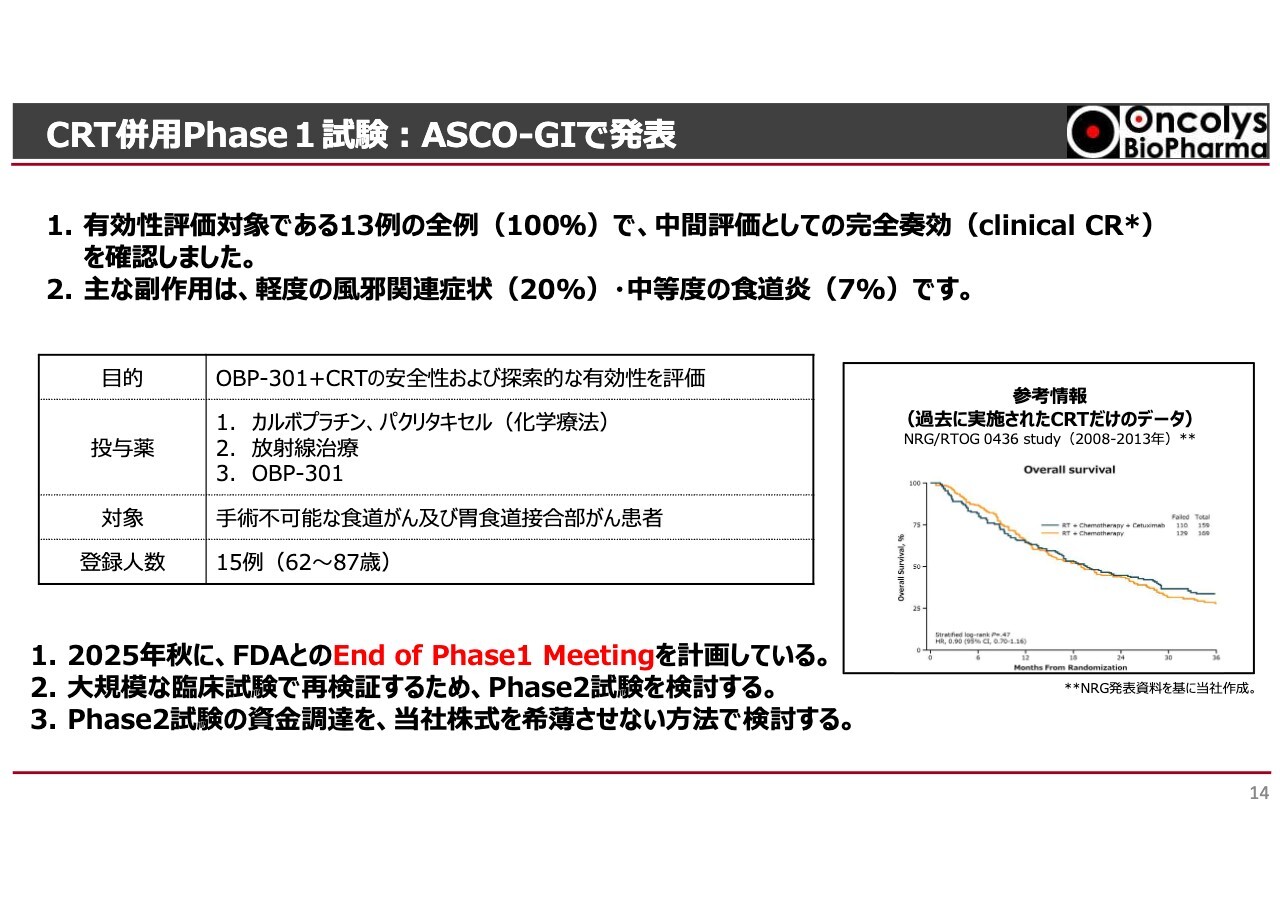
「テロメライシン」について、1つ明るいニュースが飛び込んできました。今年1月にサンフランシスコで行われた、アメリカのがん治療学会の消化器領域のASCO-GIという非常に有名な学会で、アメリカのNRG Oncologyグループというがん治療のプロトコルを作る有名なグループが、ニューヨークにあるスローン・キャタリングがんセンターを中心として「テロメライシン」の初めての放射線化学療法の臨床試験を行いました。これは食道がんが対象です。Phase1として主に安全性の確認を行いますが、実際は有効性も見ています。
評価対象は13例と少数例ですが、全症例で局所のがんが消えたという結果になっています。ケモラジ(放射線科学療法)の標準治療においては、50数パーセント、60パーセント未満の方が局所のがんが消えるのですが、今回の「テロメライシン」臨床試験結果は100パーセントということです。大規模試験でこれが再現できるかどうかはわかりませんが、大きなインパクトがあり、ぜひ今後の治験をさらに拡大して進めていきたいというのがNRG Oncologyグループというアメリカの臨床試験グループの考え方です。
中間的にはがんは消えたのですが、今年秋までに臨床試験の1年生存率の結果が出ます。その結果をもとにしてFDAとEnd of Phase1 Meetingを行って、次をPhase2にするのか、あるいは最終的な大規模試験に進めるかどうかを話し合う計画にしています。
スライドに示したのは、過去に化学放射線治療に対して「セツキシマブ」という抗体医薬を加えた臨床試験の参考資料です。生存率に差が出ない、難易度が非常に高い臨床試験ですが、今回の結果をもとにどのような治験ができるのかということは、我々も非常に興味深いところです。
本日の株主総会でもお話がありましたが、この試験を完遂させるためには、おそらく大きなお金が必要になります。スライドには資金調達と書いてありますが、我々はこの結果をもとに製薬メーカーを回っています。一緒に開発、あるいは完全ライセンスをして、許可まで持っていっていただけるような会社を見つけており、何社かに「非常に興味がある結果である」というお声をいただいています。できるだけ早く次の臨床試験に進めるように、大手の製薬メーカーと組んでいきたいと考えています。
米国2nd Lineのペムブロリズマブ併用胃がんPhase2臨床試験
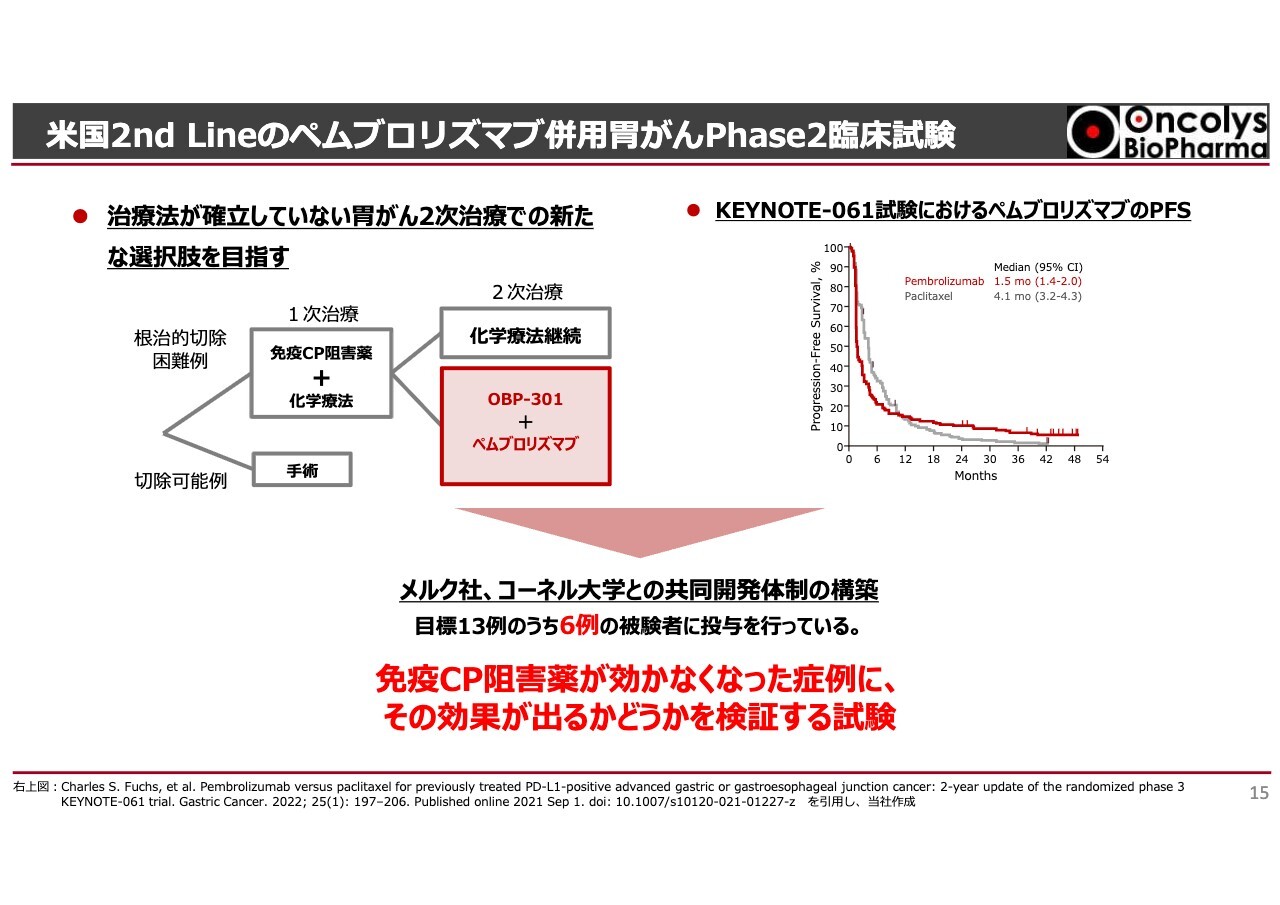
それ以外にもアメリカでは胃がんの臨床試験が進んでいます。今、「ペムブロリズマブ」というメルク社の免疫チェックポイント阻害薬との併用試験を行っています。免疫チェックポイント阻害薬は胃がんに対して、一時治療ではすでに許可をもらっているもので、アメリカでもこのような免疫チェックポイント阻害薬と化学療法の併用は行われています。ただ、スライド右側にあるように、胃がんのPhase3以降の患者さまがメインですが、非常に生存率が低く出ています。
8割、9割方の方は1次治療で効かないわけです。そのような方を対象にした2次治療という標準治療がまだアメリカでは十分に決まっていないということで、この2次治療に「テロメライシン」が上乗せされて、さらに生存率を上げることができるかという検証試験を行っています。
アメリカのメルク社、コーネル大学と組み、初期の探索試験で目標13例のうち6例の組み入れが終わっています。そのうち1例が部分奏効し良い状況に向かっていると聞いていますが、13例が終わってみないと何とも言えないところです。今後、この臨床試験の結果もみなさまにご報告できるのではないかと考えています。
2025年の臨床開発計画

それ以外の状況です。本年度の臨床開発計画としては、PMDAに先駆け総合評価の市販後臨床試験計画を提出しています。まだ考えなければならないところがあるのですが、今後、PMDAからの照会事項に応答していきます。
また、我々が今狙っている食道がんは放射線単独療法の方々です。毎年2万5,000人程度の方が食道がんに罹患するわけですが、その中で放射線治療しかできないという患者さまは10パーセント程度です。
そのような方々に「テロメライシン」が使われるのですが、アメリカで良い結果が出たケモラジとの併用を日本国内で検討したいと思っています。食道がん領域で、今は放射線と併用して3回しか投与できないのですが、さらに4回投与、5回投与はどうなるかというようなことも含めて、消化器領域に関する「テロメライシン」の研究会を発足させ、さらに大きなマーケットを狙っていきたいと考えています。
食道がん以外でも、本日ご出席の株主さまから株主総会の質疑応答で「肺がんではどうか」というお話も出たのですが、どのような領域で拡大できるのかを考えています。「テロメライシン」では、現段階では口腔がんを狙えるのかどうか、あるいは非常にニッチな領域ですが、直腸よりもさらに下の肛門のがんなどに使えるかどうかということも、できるだけ早く検討して臨床試験を開始したいと考えています。
肺がんについては「テロメライシン」でもいいのですが、さらに強力な第2世代の「テロメライシン」も考えていきたいと思っています。
商用製造の状況
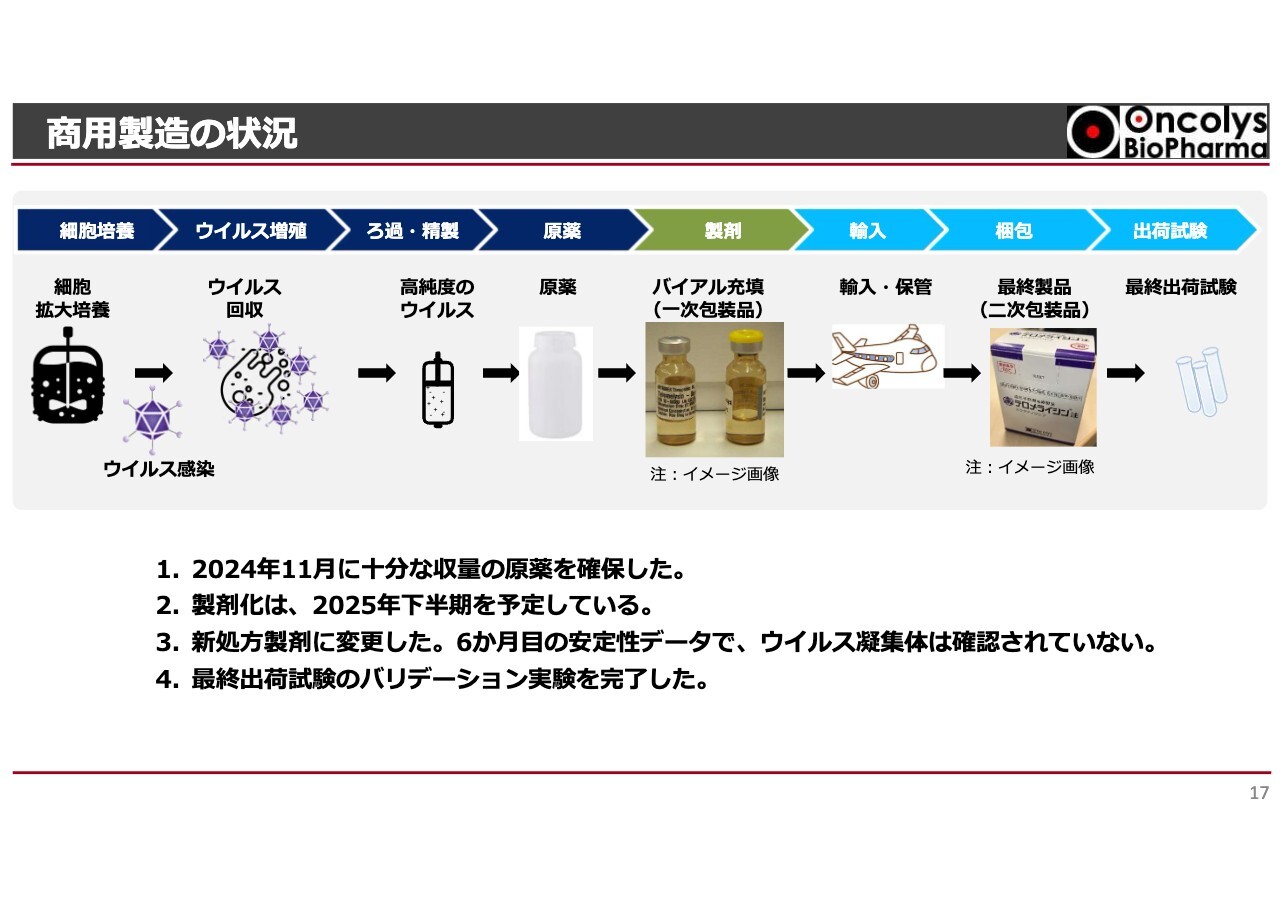
今後、当社にとって非常に重要になるのが商用製造です。PMDA、厚生労働省から許可をもらっても、製品が出なければマーケットは満足できないわけです。特に我々の業界では、細胞治療を行うある会社の「許可はもらったが、製品の出荷がままならない」という状況を厚生労働省はずっとつついています。やはり安定した高品質の製品をマーケットに出すことが、これからの我々の使命になっていきます。
「テロメライシン」の製造はご説明したとおりの状況です。
我々はヒーラ細胞、子宮頸がんの「セルライン」を使って細胞培養をして、それに「テロメライシン」を感染させてウイルスを増殖させた後、液体クロマトグラフィーなどで高純度のウイルスを作ってフィルターにかけて、薬をまだ瓶詰めする前の状態の大きなボトルで保管する原薬をベルギーのヘノジェン社で作っています。
その後バイアルと呼ばれる瓶に詰めて、シールを貼って封入し、日本国内に持ってきて、さらに箱詰めをして出荷するという非常に長い工程を経ていきます。原薬については、2024年11月の段階で十分なものができるという状況になってきています。最終製剤化については何度も試行錯誤を行っており、今年の下半期に出来上がる予定です。
もう1つ、透明な液が少し濁ってくるウイルスの凝集体を回避するために、我々は旧来の製剤に独自の改良を加えて、ウイルスの凝集体ができないような製剤を作ってきました。現段階では6ヶ月目までの安定性試験のデータで濁りが出ないことを確認しています。年内には12ヶ月、発売するまでには18ヶ月目ぐらいまでの安全性データが出るのではないかと考えています。
さらに、最終出荷試験のバリデーションについては、きちんとした製剤ができているか、中身だけではなくシールが貼られているか、箱が包装できているかなども厳密にチェックした上で出荷する過程がなかなか一筋縄ではいかない状況ですが、三井倉庫ホールディングス社や富士フイルム富山化学社と、とにかく良いものを出していきたいと考えています。
商用製造の課題
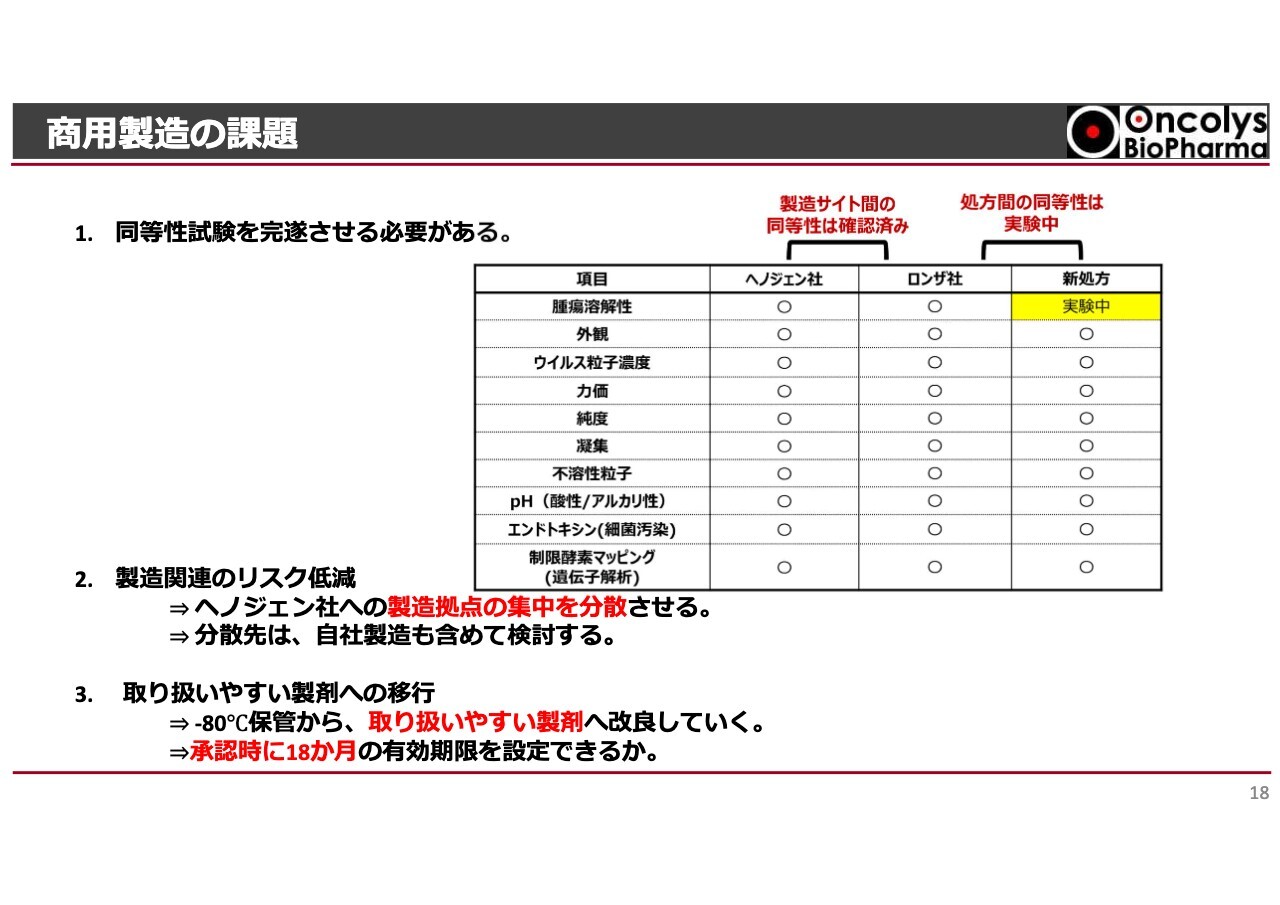
商用製造については、まだいろいろな課題があります。1つは同等性試験の完遂です。治験を行った際に使用したアメリカのロンザ社で作った製剤と、新処方にした最終製剤が同等かどうかというデータが厚生労働省から厳しく求められるのですが、少なくともロンザ社で作ったものとヘノジェン社で作ったものは、いろいろな項目において同等であったということを確認しています。
さらに、この新処方製剤で出来上がった製剤の中のウイルスが本当にがんを殺すかというような最後のチェックを行って、治験で使用した製剤と新処方の製剤が同等であるという結果が出ると、同等性は保てるということになります。こちらも近い将来に結果が出る予定です。
2つ目は、製造関連のリスク低減です。今後はヘノジェン社のあるベルギーで製造しますが、我々も適応拡大の治験をしなければならず、商用としても十分な量を確保しなければいけません。ヘノジェン社1社だけで製造するのは将来的に厳しいため、自社製造も含めて製造拠点を分散させることを検討しなければならない状況です。
3つ目は、取り扱いやすい製剤への移行です。現段階の製剤はマイナス80度で保管しなければならないため、例えば普通の冷蔵庫でも保存できるような取り扱いやすい製剤に対応していく必要があります。また、承認時期は来年半ば以降と考えているのですが、承認時期には最低限でも18ヶ月の安定性データが出ているように努力しなければならないと考えています。
製造販売体制の構築
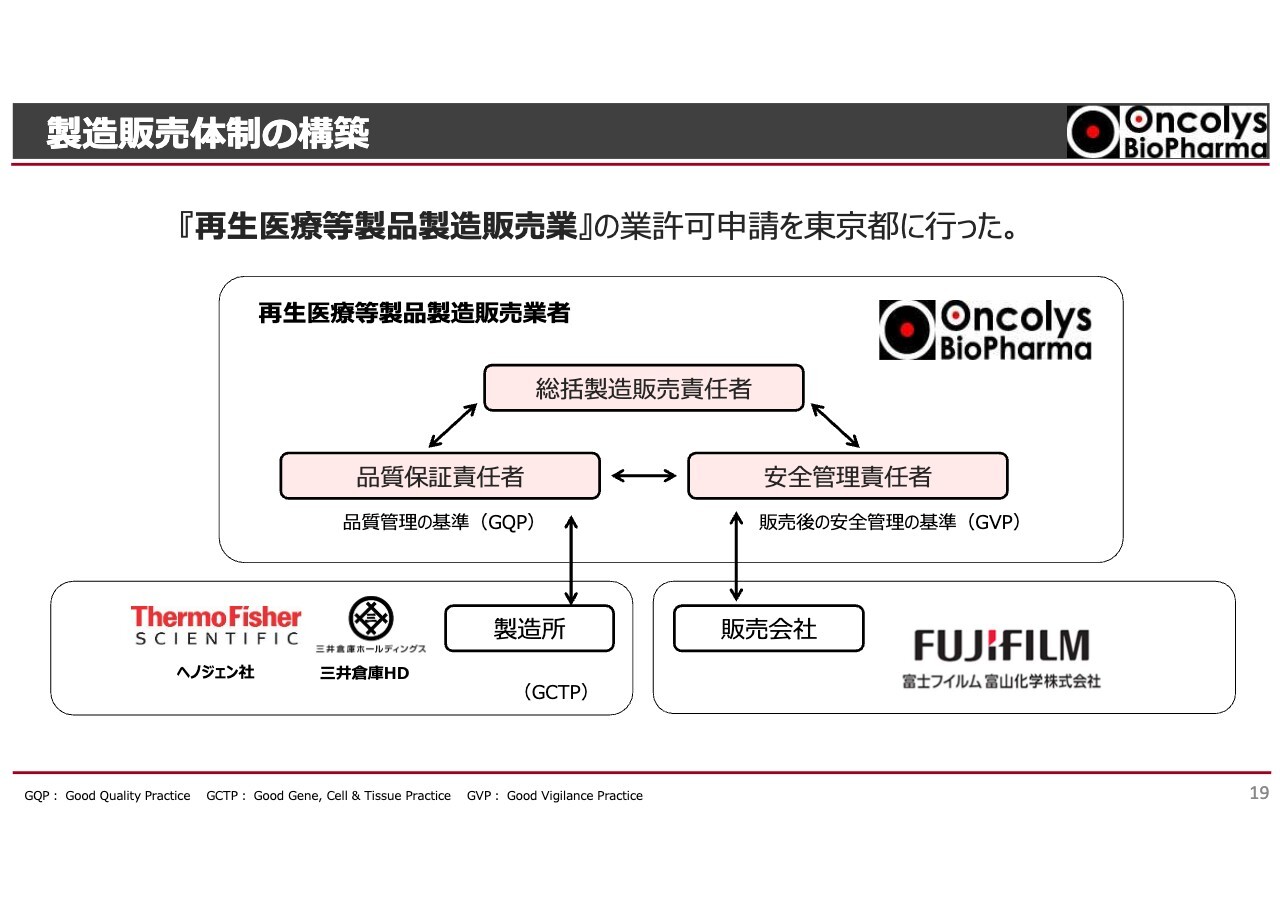
株主総会でもご質問があった、製販販売体制についてです。東京都には業許可申請を出しているのですが、審査に少し時間がかかっているようです。審査の結果が出たらご報告します。
スライドにあるように、総括製造販売責任者のもとに、品質保証責任者と安全管理責任者の三角形が成立しており、今は業務品質を一定に保つための指示書であるSOPなどを決めている状況です。GCTP体制についても製造所を含めて、十分に流通できるような体制を取るようにしており、業許可が出れば前に進んでいけると考えています。ただし、人材確保に関しては少し苦労しています。
サプライチェーンの整備
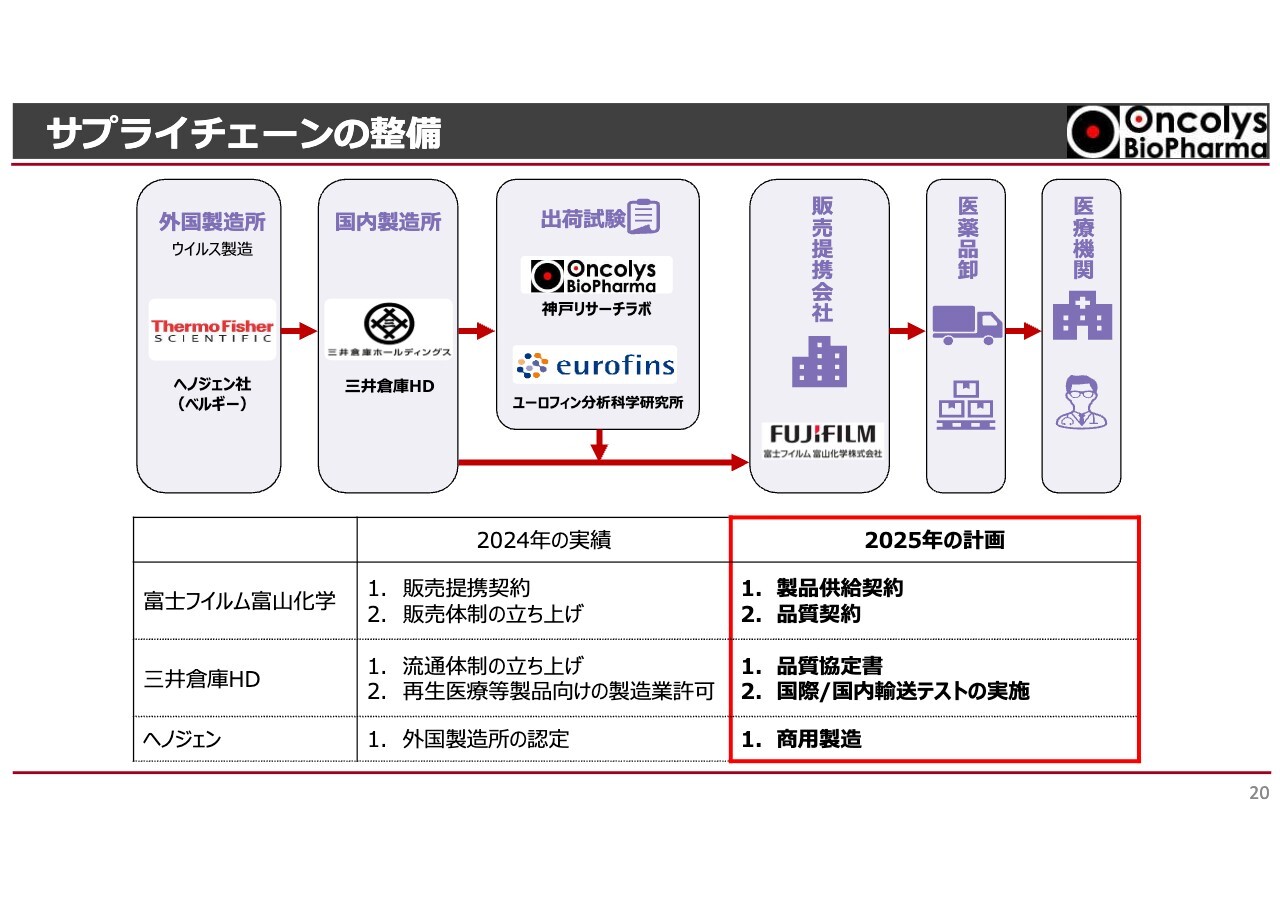
サプライチェーンの問題です。先ほどは商用製造までをご説明しましたが、その後どのようにマーケットまで流通していくかというところです。
ベルギーのヘノジェン社から送られてきたサンプルを、神戸にある三井倉庫ホールディングス社で箱詰めするという工程は、バリデーションを行っているところです。このような状況が整った後に、主に京都にあるユーロフィン分析科学研究所で品質チェックを行い、ようやく出荷となります。その後、富士フイルム富山化学社の提携している卸会社が製品を各医療機関へ届けていきます。
富士フイルム富山化学社とは昨年、販売提携契約を行っており、今年はさらに製品の製品供給契約と品質契約を結んでいく計画です。
三井倉庫ホールディングス社は昨年、再生医療等製品向けの製造業許可を取っており、今年は品質協定書を結び、国際/国内輸送テストを実施するという作業が残っています。
ヘノジェン社には商用製造を進めていただくにあたって、サプライに関する契約が少し残っています。
OBP-301承認申請の状況
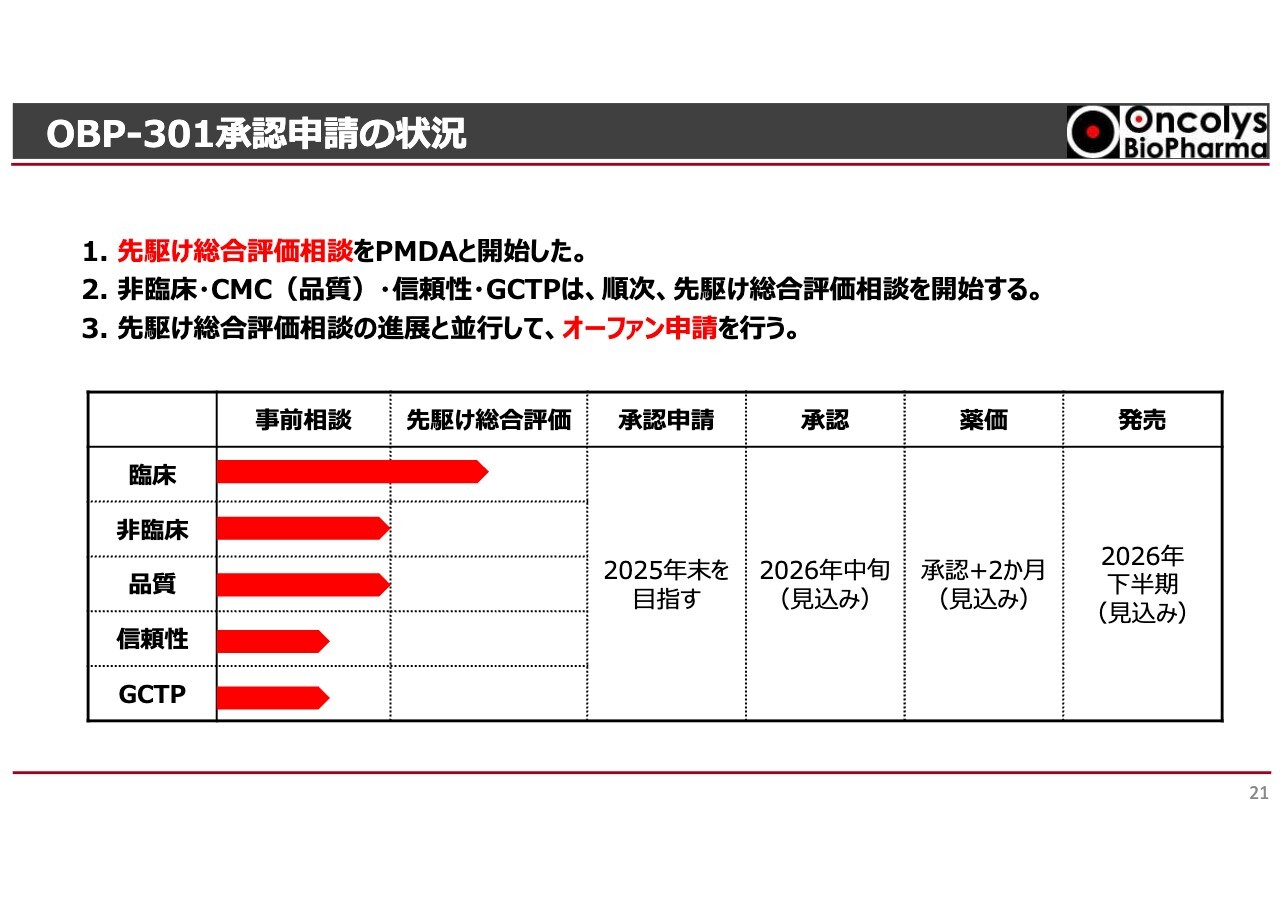
当社はいよいよ、非常に大きな資料をもとにして「テロメライシン」の承認申請を行います。それに向けてPMDAと事前相談を行い、我々も疑問に思っていることをぶつけてきましたが、ようやく先駆け総合評価という段階に入りました。大変複雑で業界の方以外はわかりにくいかもしれませんが、これが終わった後にようやく承認申請が下り、承認されると今度は薬価を交渉しなければいけません。薬価がついた後に、ようやく販売となります。
現段階では臨床の先駆け総合評価が始まったところで、その後、非臨床、品質、信頼性、GCTPとたくさんの資料を持ち込まなければいけないのですが、年末までの承認申請を目指していきたいと思います。これがかなうと半年ぐらいで承認される可能性があり、そこから薬価の交渉に入ってプラス2ヶ月かかります。発売は来年の下半期ではないかと考えており、まだ長い道のりが待っています。
ただし、この期間中にきちんと評価が進んでいれば、オーファン申請も行っていく予定です。オーファンは「みなしご」という意味で、非常に患者さまの数が少ない病気が対象になります。
食道がん治療ニーズ

「テロメライシン」は、現段階では食道がんの局所治療薬、将来的にはより幅広い局所治療薬を目指します。患者数が少なく、大手製薬メーカーが手をつけないようなアンメットメディカルニーズ領域を、我々が狙っていきたいと考えています。
食道がんは、長時間の非常に大きなオペをしなければなりません。また、食道を切ってしまうと喉からすぐに胃に入って逆流が起こるなど、いろいろな副作用が起こるのですが、「テロメライシン」の治療を行うと食道が温存できるということは、患者さまにとって大きなメリットになるのではないかと考えています。がんを切らずに治療するという、まだ満たされていないニーズを満たしていきたいと思います。
OBP-301の知的財産権の強化

食道がんにおいて、我々は世界的に確固たる地位を築きたいと思っているのですが、特許庁から連絡があり、「腫瘍溶解アデノウイルスの内視鏡投与に関する特許」が成立しました。これは「テロメライシン(OBP-301)」だけではなく、「OBP-702」や他社の腫瘍溶解アデノウイルスも対象になっていますので、他社が我々のまねをして食道がんに使うということも特許によりブロックできる可能性が出てきました。
投与箇所は食道がんに限定されず、胃がんや頭頸部がん、肛門がんなども対象になります。このようながんに対して内視鏡を使って投与するということに関しては、日本では当社が非常に強い立場になりました。特許が残り15年以上ありますので、食道がん領域は我々が独占できる可能性が高くなってきました。
ヨーロッパやアメリカに関してはまだ審査中ですので、成立したらみなさまにご報告したいと思います。
海外展開に関する状況及び今後の進め方

「テロメライシン」のビジネス状況です。まずは昨年、台湾のメディジェン社に商業化権を許諾しました。メディジェン社とは、2008年からコストシェア・プロフィットシェアの契約のもとに開発を進めてきました。これによって、彼らは台湾当局と話し合い、「テロメライシン」が台湾でも発売できる状況を作っていくことになると思います。当社から商品を買って、当社にロイヤリティが入ってくるというかたちが出来上がってきました。
台湾だけではなく、一部のアジア諸国においては、日本できちんとした許可が取れていれば臨床試験をしなくても商品を発売できる制度があります。このような国に対しても、我々が単独で行うかもしれませんし、メディジェン社と組んでアジア戦略を考えていく可能性もあります。
先ほどご説明したように、ケモラジ試験、大規模な臨床試験を完遂するために、政府、企業との提携交渉も進めています。
ヨーロッパ諸国では、放射線単独での食道がん治療が行われているようです。あまり大きなマーケットは期待できないかもしれませんが、「テロメライシン」の世界戦略の中に、そのようなヨーロッパの政府、企業を含めてビジネス交渉をしていきたいと考えています。
OBP-301の売上予測(国内)

このような状況を踏まえて、当社は承認取得後にマーケットを拡大していきたいと考えています。薬価がなかなか決まらず、ヘルペスウイルスで脳腫瘍領域の許可を取っている第一三共の「デリタクト」の価格が140万円ぐらいですので、現段階では我々もこのぐらいの薬価になる可能性が高いと踏んでいます。
当然、我々はこれより高い薬価を目指しているわけですが、仮に140万円だったとした場合、2週間おきに内視鏡で3回投与すると考えると、発売後5年間で累積売上高が最低でも48億円、うまくいけば135億円を達成すると見込んでおり、できる限り早く単年度黒字を達成したいと考えています。その後、投与方法の拡大や他のがんへの適応拡大を行って、6年目から10年目、2035年に向けて、年間売上高100億円以上を目指したいと考えています。
いろいろな経費を引くと100億円そのものが収益になるわけではありませんが、少なくとも我々が「テロメライシン」で食っていけるという状況をできるだけ早く作っていきたいと考えています。
トランスポゾン社へライセンスするまでの経緯
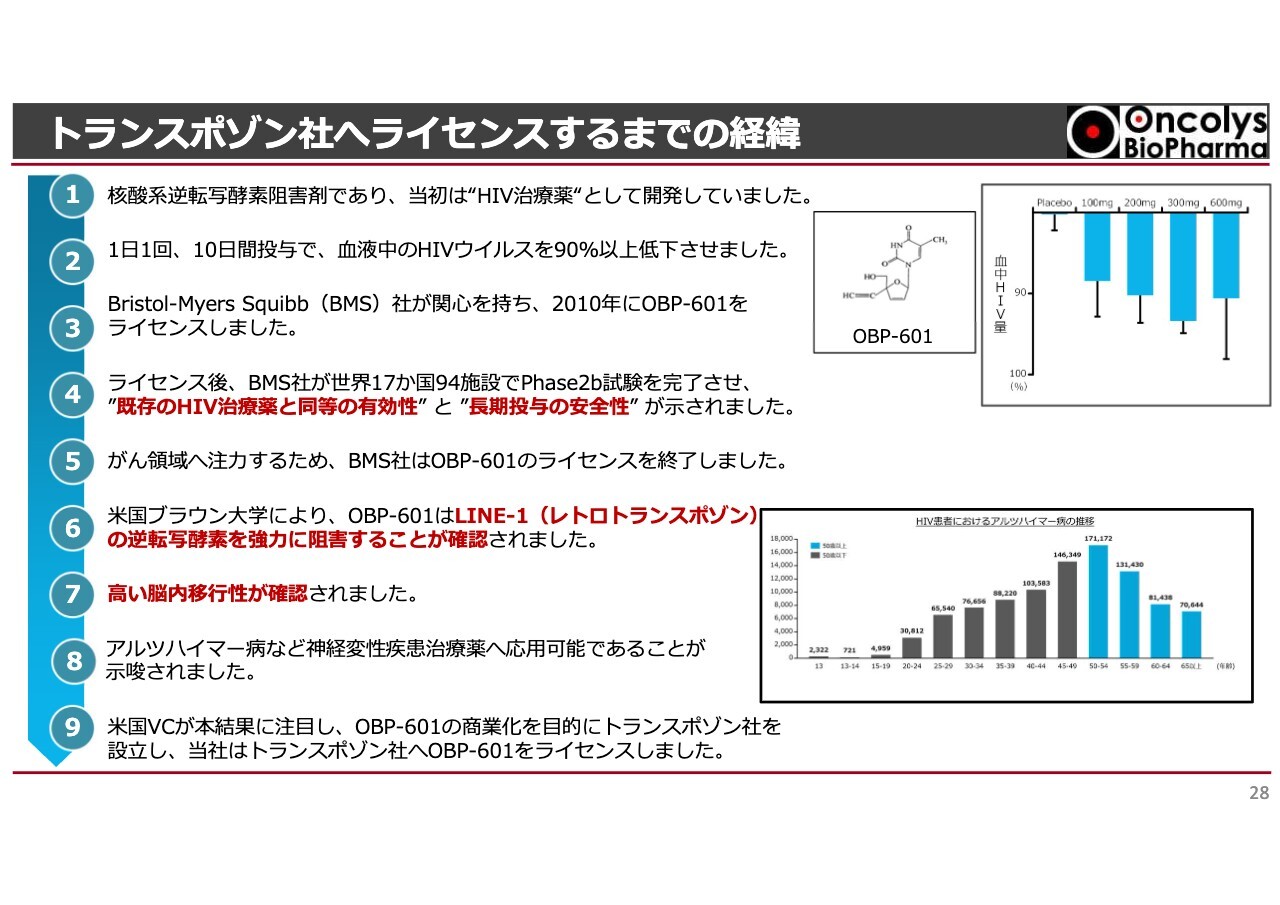
「OBP-601 censavudine」についてです。トランスポゾン社の開発番号は「TPN-101」となっています。
もともとは抗エイズ薬で、1週間飲むだけで血液中のエイズウイルスが90パーセント以上低下するという結果を受けて、2010年にはBristol Myers Squibb(以下、BMS)社がライセンスしました。
残念ながら、BMS社が「オプジーボ」という免疫チェックポイント阻害薬の開発に注力するということで、抗エイズ薬を開発したり売ったりすることをやめたため、我々はそのライセンス契約を切られてしまった時代がありました。その後「OBP-601」がアメリカのブラウン大学の目にとまり、新しい使い方ができるのではないかという報告が我々に上がってきたわけです。
スライドのグラフについても昨年の株主総会でご説明しましたが、HIVウイルスに感染した50歳以上の方は、アルツハイマー病になる確率が減っています。普通は、高齢者になるほどアルツハイマー病になる可能性が高くなるのですが、抗エイズ薬を飲んでいる人は、なぜかアルツハイマー病に罹患しないという結果が得られました。
研究の結果、「OBP-601」あるいは抗エイズ薬が、レトロトランスポゾンの中のLINE-1という遺伝子の活性を抑制していることが推察されました。実験した結果、非常に良い結果が得られて、他の抗エイズ薬と比較して「OBP-601」が断トツで良いということがわかったわけです。その結果をもとにしてトランスポゾン社が設立されたという経緯があります。
OBP-601:トランスポゾン社の紹介

トランスポゾン社の所在地はコネチカット州で、創業者はエッカード・ウェバーという方です。この方と今年3月にアメリカで会って、今後の臨床試験の方法やビジネスの考え方をお話ししてきました。社員数は35名で、当社と規模はあまり変わりません。臨床試験も非常に緻密に、しかも時間厳守で行っている非常に優秀な会社だと考えています。
エッカードさんは世界で発売される抗菌剤などの新薬を創出した方で、2020年に会社を創業していただき、大変心強く思っています。すでに7年のお付き合いですが、いろいろな情報を交換しています。
神経変性疾患治療薬としての開発着眼点
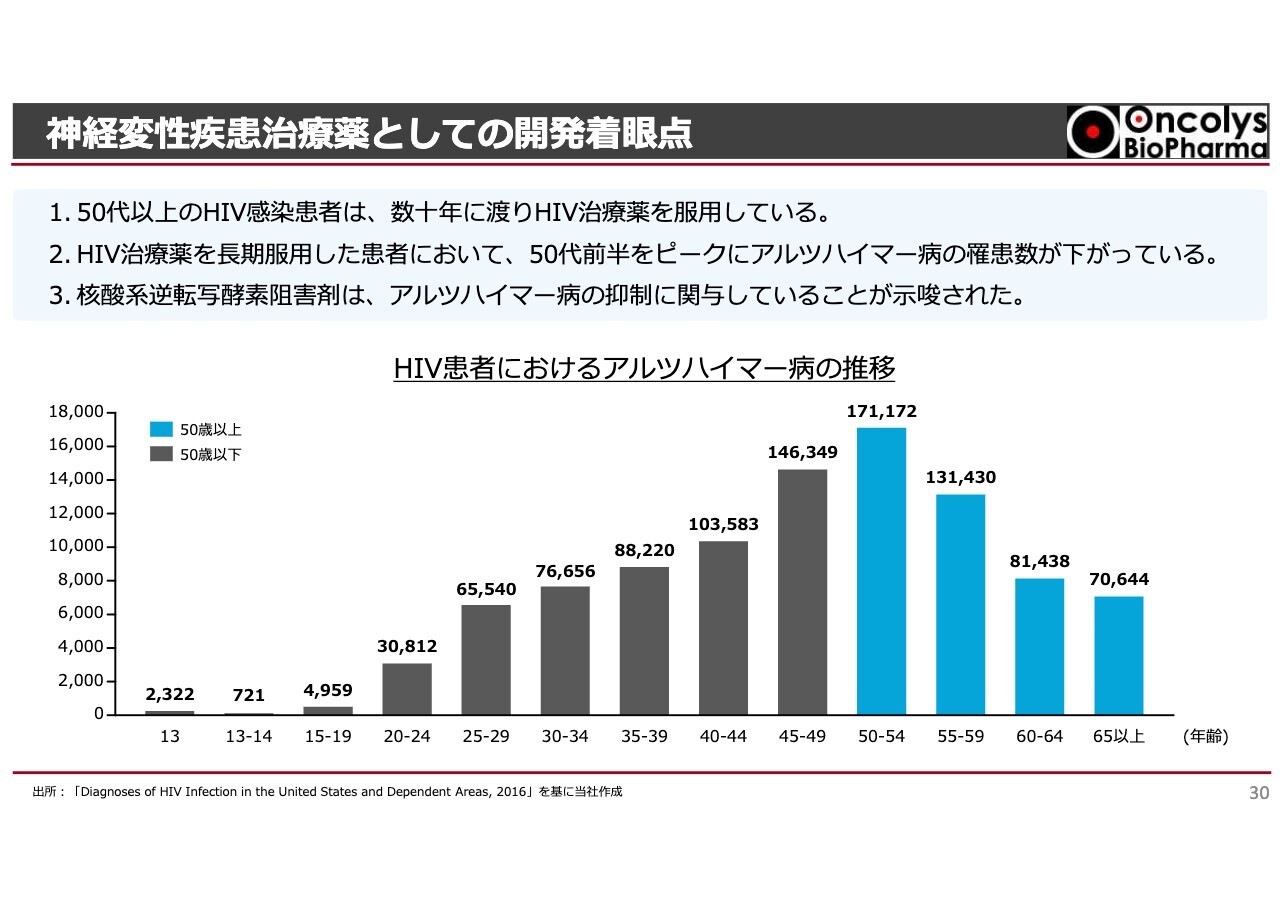
こちらの内容は先ほどご説明したとおりです。
OBP-601の新規メカニズム
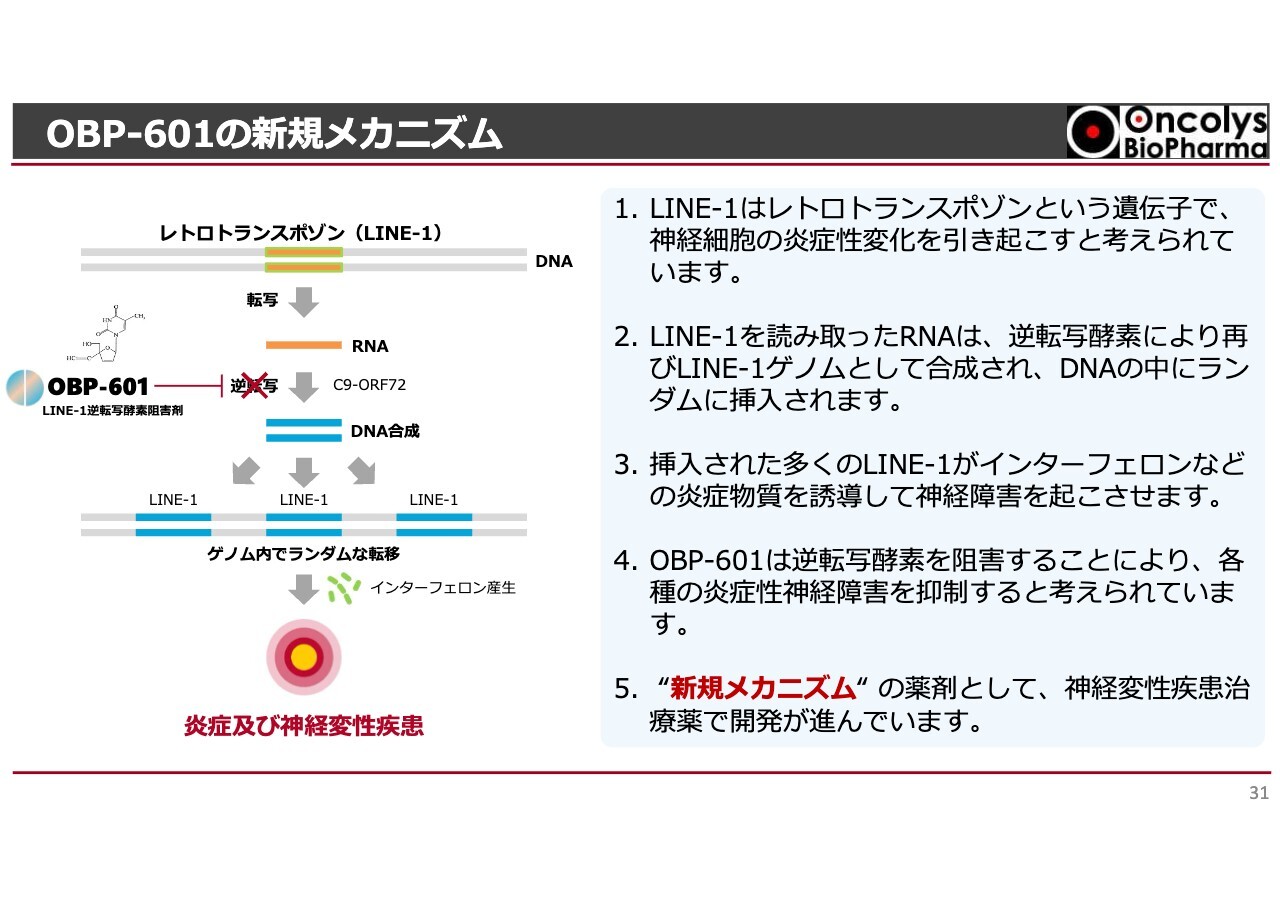
メカニズムについてです。難しい話ですが、ヒトの二重らせんの遺伝子の中に、このレトロトランスポゾンという遺伝子が40パーセントぐらい分布しています。何をしているかはよくわかりません。特にLINE-1という名前のついた遺伝子が、病気によってはあちこちに飛んでいます。飛ぶことによって遺伝子の働き方がおかしくなっていき、神経付近でインターフェロンを出して、神経の炎症を起こすというのが簡単なメカニズムです。
これを「OBP-601」が強力に抑えており、なおかつ「OBP-601」は脳の中に非常に入りやすい化合物であるということがわかってきました。
強力なLINE-1の抑制
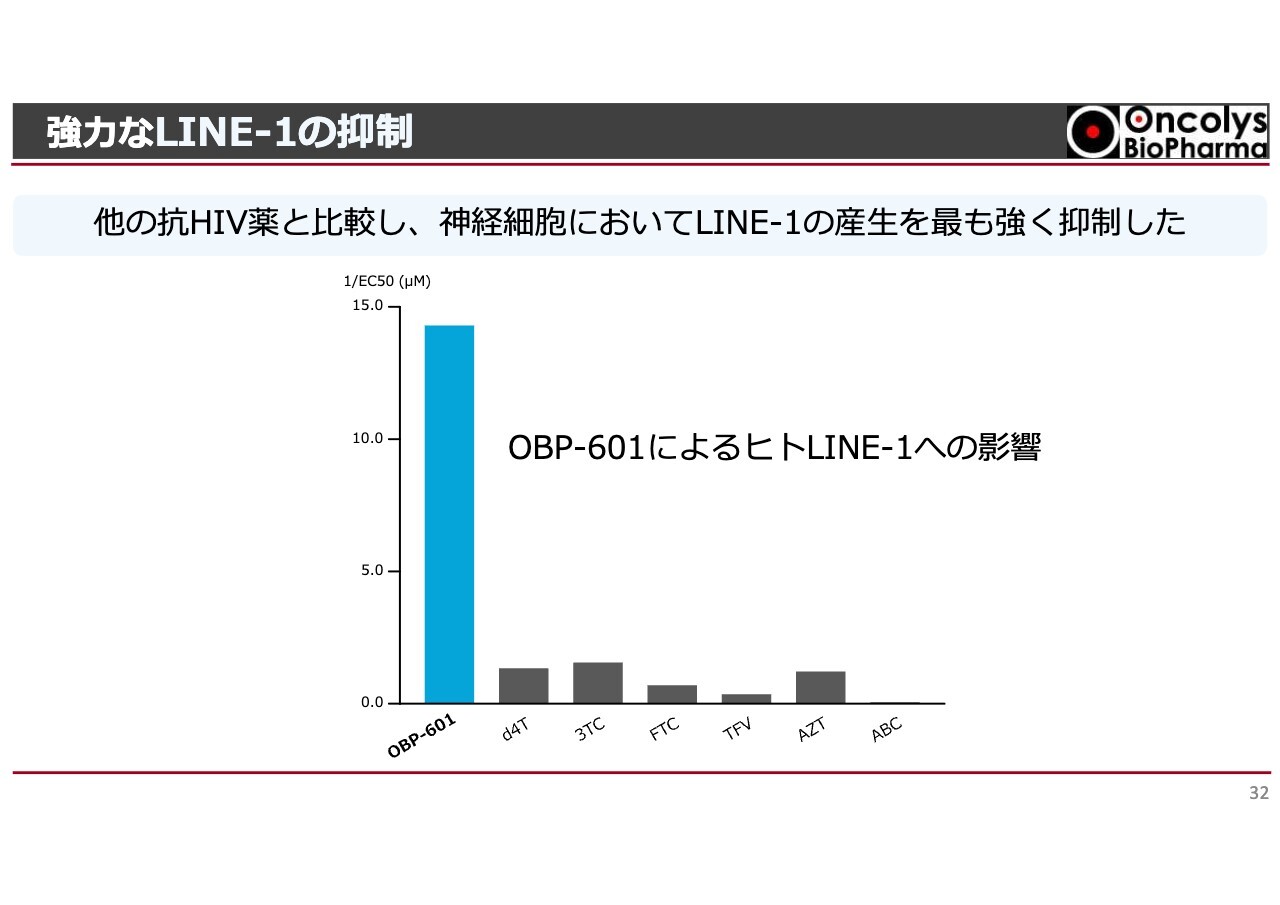
スライドはブラウン大学のLINE-1の逆転写酵素阻害の結果で、グラフ横軸にある「d4T」「3TC」などは現在世界中で使われている抗エイズ薬です。このような薬も多少効果はあるのですが、「OBP-601」だけがトランスポゾンの抑制活性が断トツで高く、このような観点から開発が始まりました。
OBP-601の特長

エッカードさんとお話ししたところ、現段階では全く競合薬が開発されていないということです。このような意味では、世界唯一のLINE-1の逆転写酵素阻害薬であるという確固たる地位を築けており、現在はいろいろな神経疾患で開発が進められています。
PSP(進行性核上性麻痺)という病気は、パーキンソン病と非常によく似ていて体が震え、普通に歩いていても突然転んで倒れたりするという症状がよく起こります。この病気が進んでいくと、認知機能も障害を受けるという特徴があります。日本でも数千人が罹患している病気です。
PSP(進行性核上性麻痺)Phase2

OBP-601は、アメリカで昨年5月にPSPに対するファストトラックに指定されています。昨年の結果ですが、脳脊髄液中のNfLという神経マーカーは神経が壊れると脊髄中にたまってくるのですが、この上昇を抑制させました。炎症性神経変性のバイオマーカーであるIL-6も、「OBP-601」を投与すると低下します。安全性も担保されているという結果が並び、昨年7月にFDAとEnd of Phase2 Meetingを行っています。
この結果として、FDAからはPhase3の内容と計画については良いという同意が得られています。そして今後、Type C Meetingを行う予定です。これはどういうマーカーを取ればいいのかを検討するミーティングなのですが、迅速承認に向けたものであり、FDAはPSPの結果を非常に前向きに捉えているという結果が得られています。
ALS(筋萎縮性側索硬化症)/ FTD(前頭側頭型認知症)Phase2

2024年に報告があったALS(筋萎縮性側索硬化症)、FTD(前頭側頭型認知症)という2つの領域でPhase2の臨床試験を行っています。
この結果、ALSには効果が認められました。スライドにC9-ALSと記載していますが、これはある遺伝子変異が起こっている、特にLINE-1が悪さをしているようなALSです。C9-ALS患者は、筋肉が委縮するため、最終的には呼吸ができなくなって亡くなります。臨床試験の結果、たった1年の投与でしたが、この病気の患者の死亡率と相関する肺活量低下において、約50パーセント進行を抑制したという結果が出ています。
全体の病態の進行も抑制して、なおかつPSPと同じように主要なバイオマーカーの低下も示しました。このようにALSに対しては非常に良い結果だったのですが、残念ながらFTDに関しては、選択した症例が良くなかったのかもしれませんが、一定の変化が認められませんでした。現段階では、ALSに集中しようと考えているところです。
こちらについては、すでに2025年1月に最終臨床試験に向けたEnd of Phase2 MeetingをFDAと行っています。最終的な試験に向かうための計画にFDAは非常に興味を持っており、今後もディスカッションしていく予定です。どのように行うか、どのような施設で実施するか、どうすれば優先審査にかけられるかを、もう少しFDAと話し合っていく段階です。少なくとも非常にポジティブであることは確かです。
トランスポゾン社の今後の展開

Phase2で非常に良い結果が出たPSPとALSの領域については、トランスポゾン社はできるだけ早くPhase3を始めようと考えています。これに対して、トランスポゾン社も資金調達の活動を行っています。当然このようなパートナリングになりますが、一緒に取り組んでいただける製薬会社をいくつか絞り始めています。
トランスポゾン社のエッカード・ウェバーCEOといろいろ話したのですが、彼らとしてはこれだけ良い結果が出たものを現段階で安い価格でライセンスをするよりは、自分たちでここまで持ってきたのだから、できるだけPhase3は自分たちで行いたい、あるいは仮に大手企業が来てくれたとしても、いきなりライセンスではなくてパートナリングなどのかたちでPhase3を進めたいというようなビジネス展開を彼らは考えています。
今後どうなるかはまだ教えてもらっていませんが、少なくとも年内には、どのようにPhase3を始めるかについてお伝えできるのではないかと考えています。
トランスポゾン社は、それにも増して新たな治療薬のアルツハイマー病に対する展開について非常に意欲を燃やしていますし、彼らが話してきたいろいろな製薬メーカーも、この治療薬がアルツハイマー病に効くかどうかを非常に気にしています。Phase3という大きな試験を始めることも重要ですが、一刻も早くアルツハイマー病に対しての治験を始める計画です。治験計画についても、今話し合いをしていてほぼ固まっており、Phase2をこれから始める準備を迅速に進めていると聞いています。
なお、治験が進んで良い結果が出た場合に、スライドに「再ライセンス」とあるとおり、我々からライセンスしたものをトランスポゾン社がまたさらにライセンスをするということも考えています。当然良い結果が出ればM&Aなども考えていますし、さらに場合によってはIPOして、アメリカだと相当大きな額でIPOできると思うのですが、自分たちで開発を進めていくことも考えています。
いずれにしても我々にはお金が入ってくる契約を結んでいるため、とにかく彼らに臨床試験を早く始めていただき、当社にマイルストーンが入ってくることを期待しています。
神経難病領域におけるディールサイズ
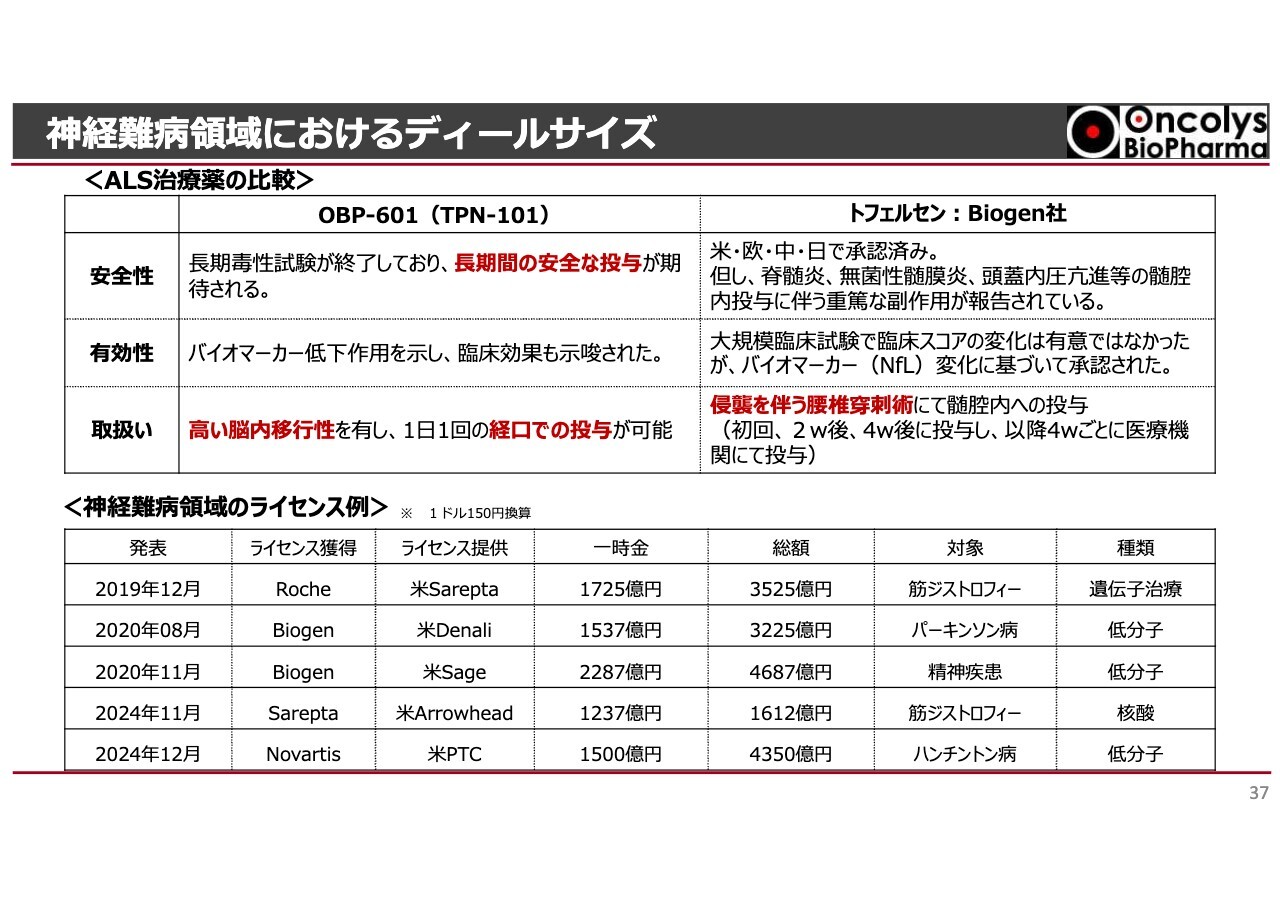
神経難病、特にALSに対しては、トランスポゾン社も非常に力を入れています。2024年までにアメリカあるいは日本で許可になった、Biogen社の「トフェルセン」という核酸医薬があります。この薬は、臨床試験ではなかなか差は出なかったものの、人によってはバイオマーカーがある程度変化したため、ほかの薬がないこともあり、許可を取っています。
ただし「トフェルセン」は脳内に入れなければならない薬です。侵襲を非常に伴う腰椎穿刺術による、いわゆる髄腔内投与となります。背中から背骨に穴を開けて、そこから2週間ごと、あるいは4週間ごとに薬を投与しなければならないという、非常に継続しづらい投与方法で許可を取っています。
一方で、「OBP-601」は1日1回の経口投与が可能です。加えて脳内移行性も非常に高く、バイオマーカーもきちんと動いていて、臨床症状にも効果が出ています。すでに抗エイズ薬の段階で長期毒性試験は終わっており、長期投与において重篤な副作用がないことも確認されています。したがって、ALSでも優先審査のもとにとにかく早く許可を取ってもらえればと考えています。
スライド下部の表は、神経難病領域でのライセンス例です。上の3つについては、前回の株主総会でもお話ししたのですが、表の一番下に記載しているように、2024年12月にNovartis社がPTCという会社からハンチントン病の薬を導入し、総額4,350億円、一時金1,500億円を受け取っています。
下から2番目のSarepta社も、2024年から筋ジストロフィーの薬を入れており、もちろん各ステージにはよりますが、大変大きなディールがまだアメリカで行われているという状況です。このような中に、近い将来「OBP-601」も入ると良いと考えています。
アルツハイマー病(AD)への適応について
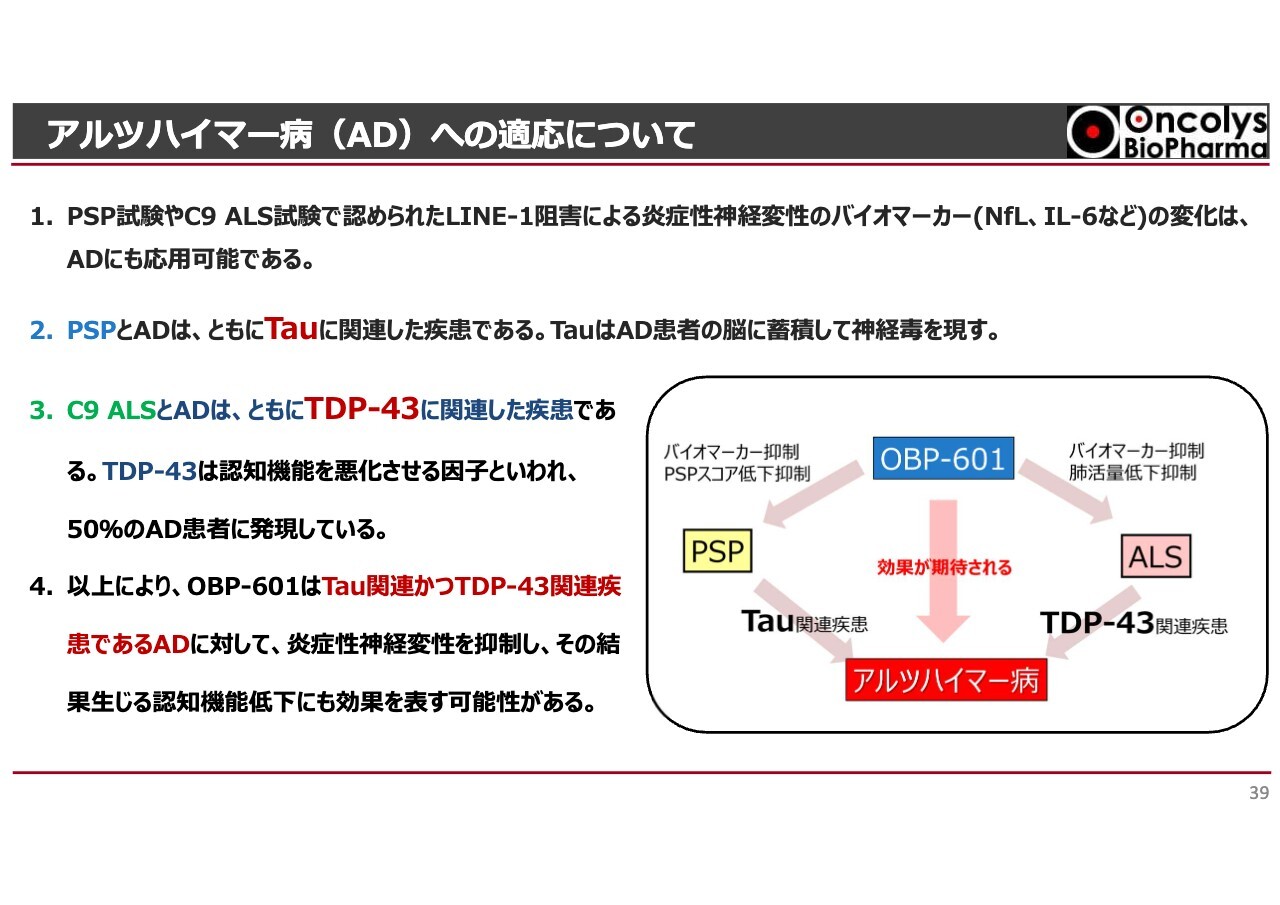
アルツハイマー病の開発といっても、無計画に狙っているわけではありません。簡単にいうと、PSPという病気は、Tauというタンパク質が神経に蓄積して神経損傷が起こり、認知機能が悪くなるというもので、Tau関連疾患の1つです。すでにTauに注目した抗アルツハイマー薬が開発されているところであり、「OBP-601」はこのようなTau関連疾患に効果があります。
さらに、TDP-43というタンパク質があります。C9-ALSとアルツハイマー病は、ともにTDP-43に関連した疾患なのですが、このような病気にも「OBP-601」が効きます。
このように、Tau関連疾患であるPSP、TDP-43関連疾患であるC9-ALSにおける「DBP-601」の効果を考えると、Tau関連疾患でもあり、TDP-43関連疾患でもあるアルツハイマー病にも当然効くであろうと考えられます。その大きな仮定のもとに、トランスポゾン社は次の段階に進んでいこうとしており、FDAもこの考え方は認めているようです。
早くアルツハイマー病の結果が出ることを見たいと思いますし、まったくこれまでと違う、世界で唯一のメカニズムを持ったアルツハイマー治療薬に育てていければよいと考えています。これらが期末の状況です。
OBP-702の特長
「OBP-702」についてご説明します。先日プレスリリースもしましたが、「OBP-702」の臨床研究に、AMEDという機関の科研費が出るということになりました。3年間で合計3億円程度の助成金が入ることとなり、その資金をもとに、岡山大学の研究グループですい臓がん患者を対象とした「OBP-702」の臨床試験を考えています。
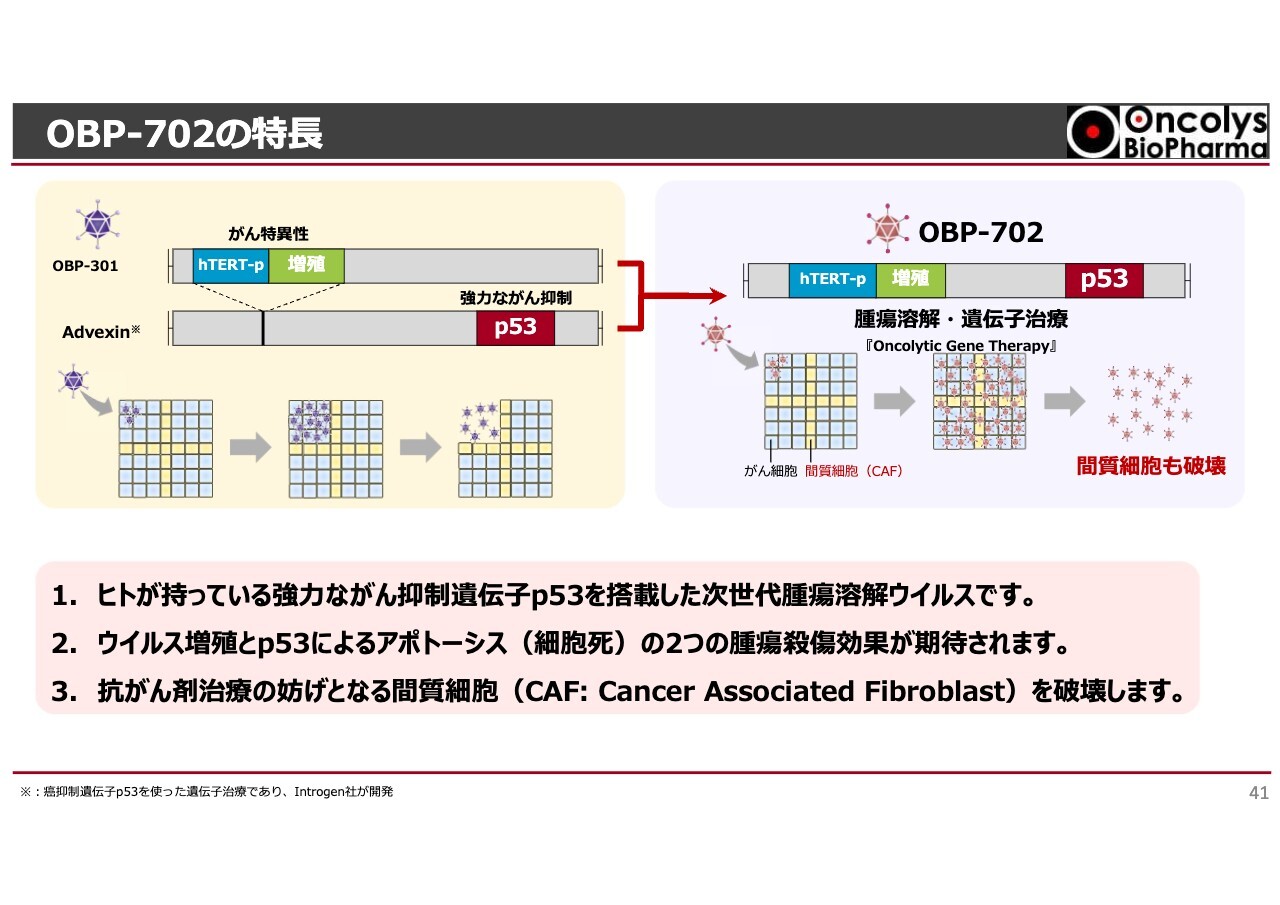
「OBP-702」とは「テロメライシン」の遺伝子に、ヒトが持っている非常に強力ながん抑制遺伝子であるp53を搭載した次世代腫瘍溶解ウイルスです。
「OBP-702」は、がん細胞の中でウイルス増殖してがんを殺すという「テロメライシン」の特徴に加え、がん抑制遺伝子p53をがん細胞の中で作り、より強力にがんを殺すという性質を持っています。
難治性がん治療の課題とCAF破壊への期待
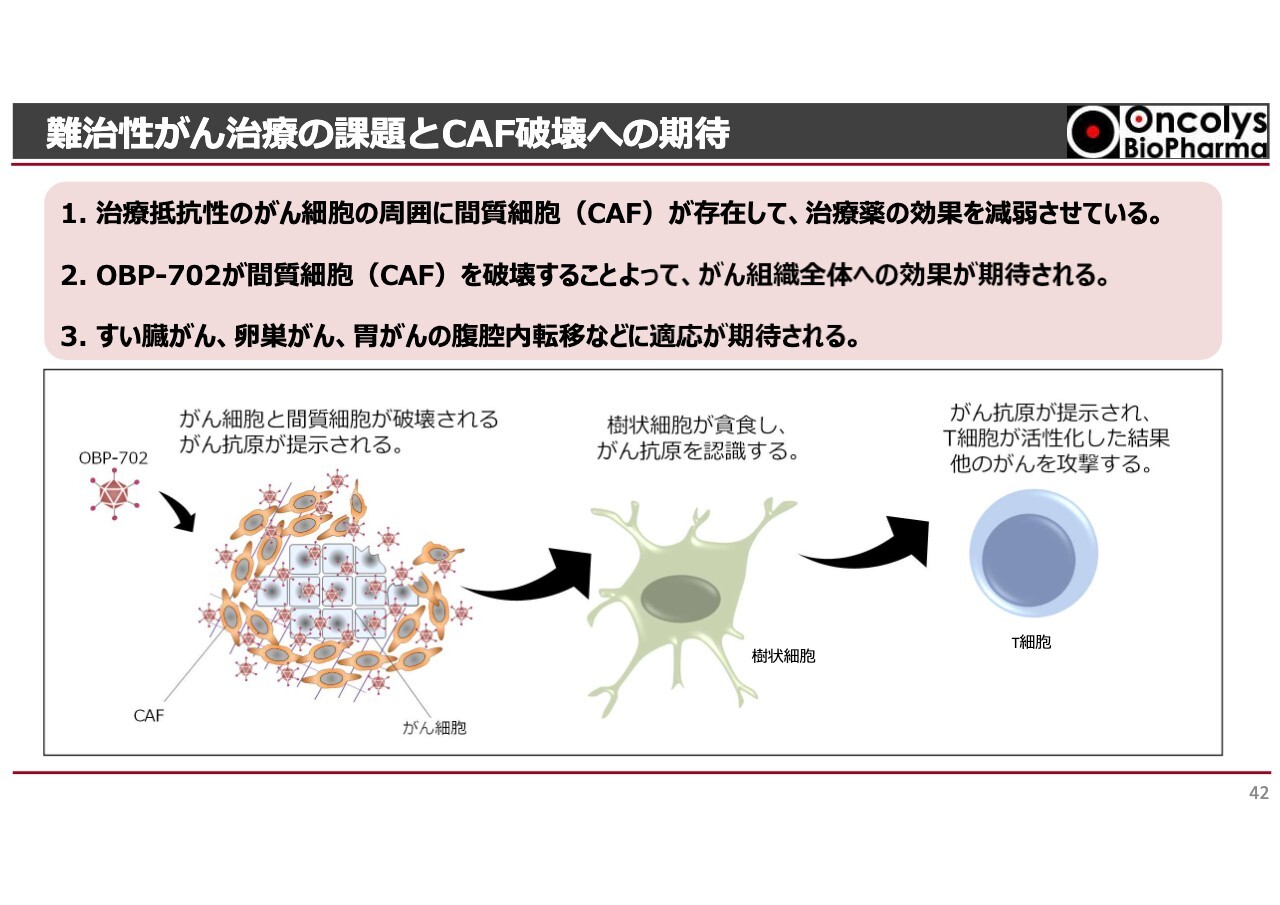
「OBP-702」は、「テロメライシン」と比較して、抗がん活性が約10倍から約30倍強いという特性を持っています。なおかつ期待できる話も出てきています。がん組織を包む繊維芽細胞であるCancer Associated Fibroblast(CAF)というものがあります。このCAFという間質細胞が、がん細胞を取り巻いて保護し、いろいろな抗がん剤の効果を低下させていきます。しかし最近の研究により、特にすい臓がんにおいて、CAFに対しても「OBP-702」が効果を示すという結果が出ています。
すい臓がんについては多くの大手製薬メーカーも臨床試験ですべて失敗しているため、我々もどうなるかわかりませんが、岡山大学の結果をもとにしてよく効くようであれば、当社としても世界で初めてのすい臓がん局所治療薬に育て上げたいと考えています。
すい臓がんの特徴
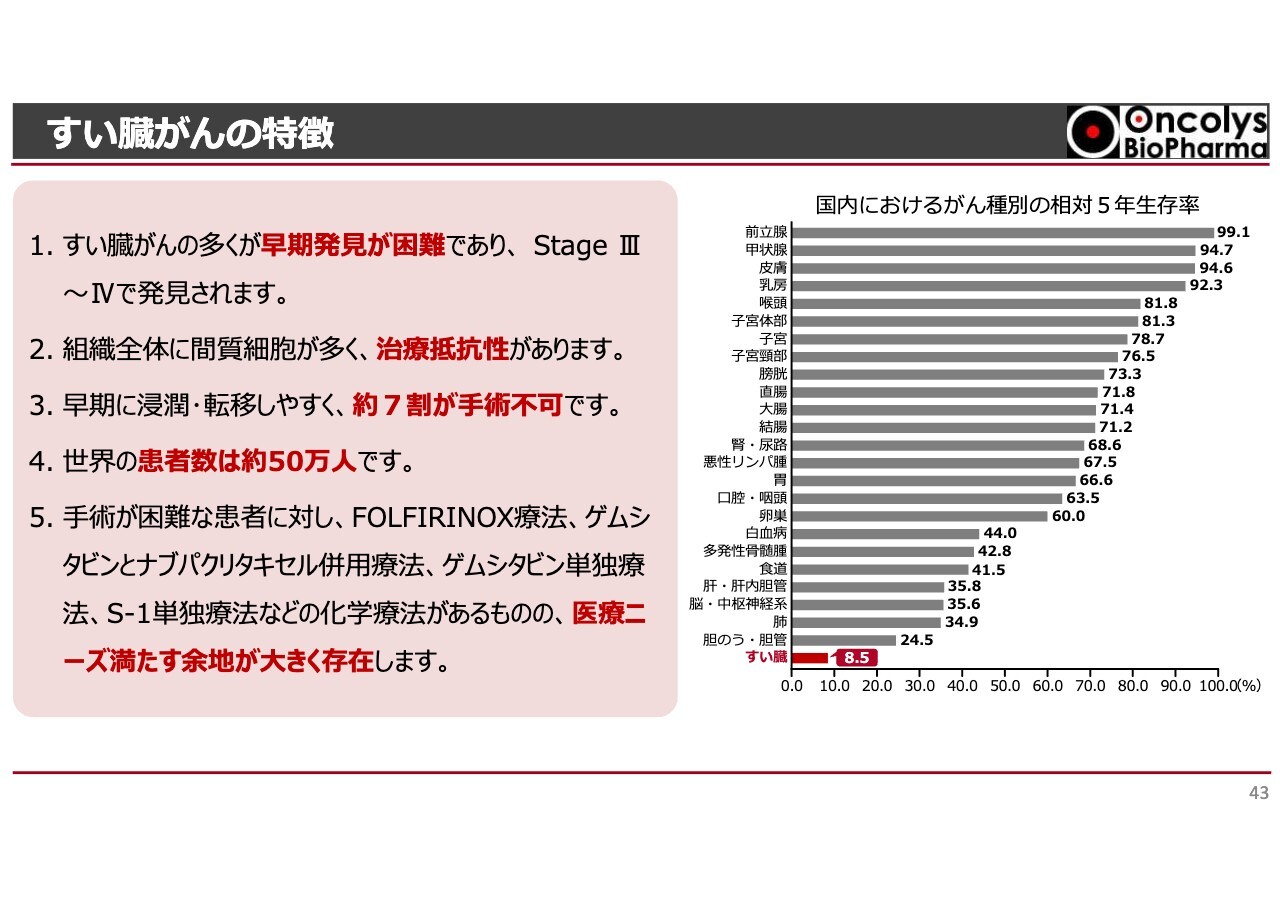
すい臓がんは早期発見が大変困難で、ステージ3からステージ4で初めて見つかることが多いです。そして多くの薬が効かない、手術もなかなかできない、一方で罹患患者が増えているという特徴があります。スライド右側の5年生存率のグラフの一番下に位置しているように、がんの中でも5年生存率が非常に低いです。
OBP-702の効果
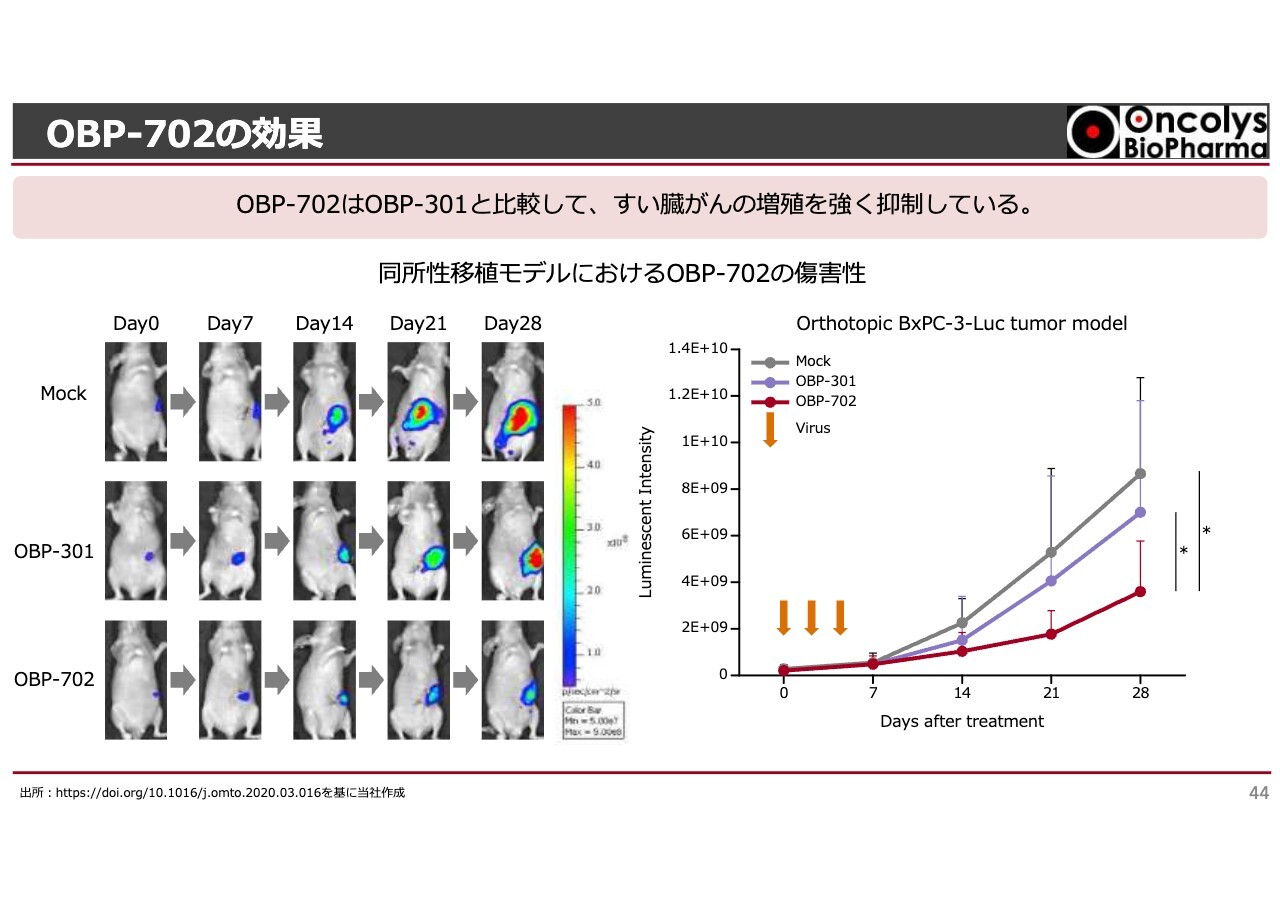
岡山大学の研究グループにおいて、ネズミのすい臓にヒトのすい臓がんを植えて、ネズミの中にヒトのすい臓がんを作り、その局所に「OBP-702」を投与すると、非常によく効き生存率も高まっているという結果が得られています。
OBP-702の開発方針
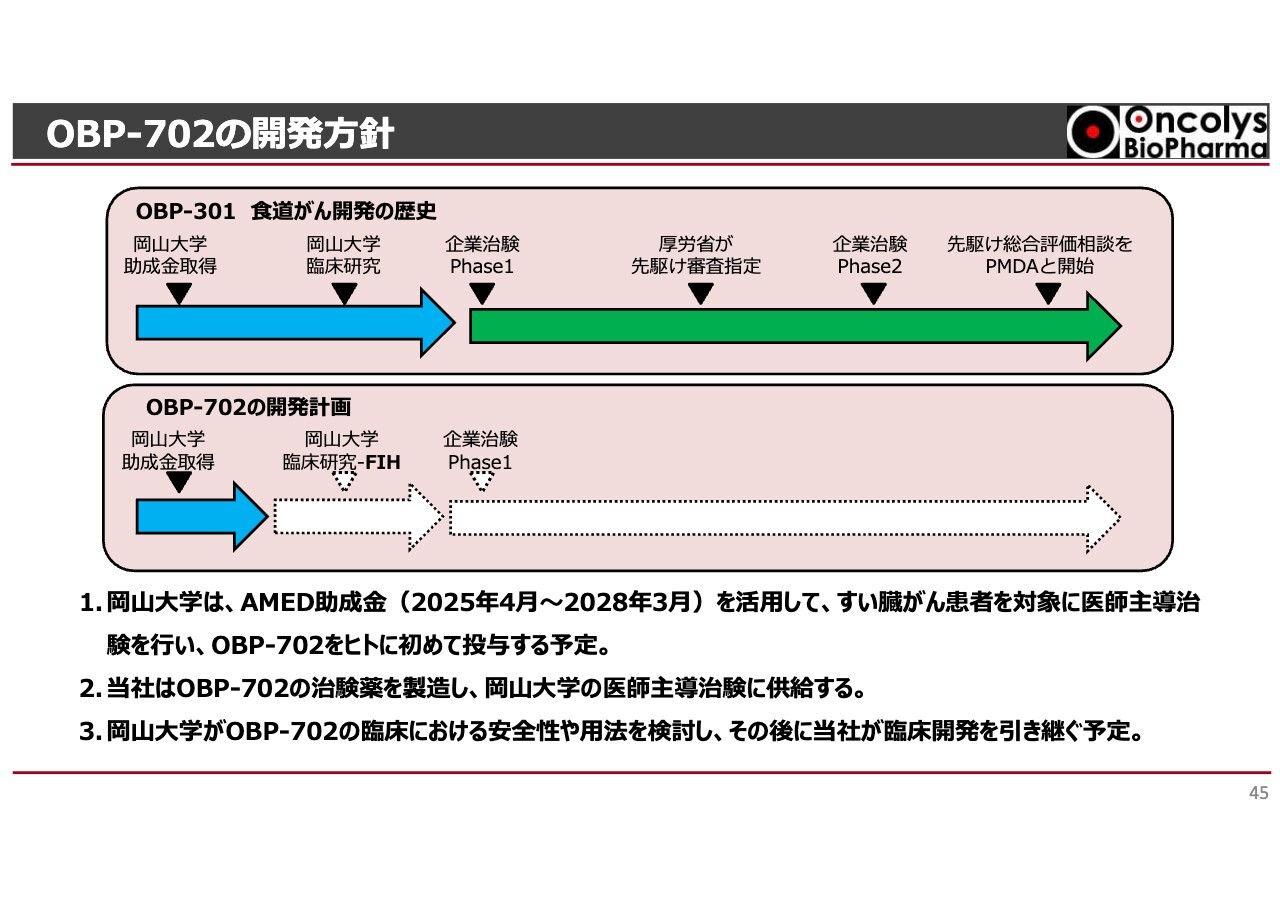
「OBP-702」についての開発計画も、「テロメライシン」の開発と同様の流れをとりたいと考えています。「テロメライシン」の食道がんにおける開発の際も、まず岡山大学で臨床研究を行っていただき、良い結果が出たら我々の企業治験に切り替えて、厚生労働省に持っていくという流れで行いました。このような流れが一番効果的な開発方針なのではないかと思っています。
最初から我々がお金を出して行うよりは、岡山大学の助成金の中で支援を行い、良い結果が出れば我々が引き継ぐというかたちでこれから取り組んでいきたいと考えています。
岡山大学の消化器外科の研究グループであるため、AMED助成事業では現在すい臓がんを対象にしていますが、我々としても、それ以外にどのようながんに領域を広げられるかについて、これから詳細に検討していきたいと考えます。
2025年にご期待頂きたい事項

2025年にご期待いただきたい8つの事項をスライドに記載しています。
まず「OBP-301」に関する①から⑥の事項についてご説明します。
「①先駆け総合評価相談を開始」は、すでに達成しています。
「②国内承認申請」は、年内に実施予定です。
「③国内オーファン申請」はきちんと行っていきます。
「④再生医療等製品 製造販売業の業許可取得」も、現在は待っている状況ではありますが、通っていきたいと考えています。
「⑤新製剤での12か月安定性試験をクリア」は、少なくとも年内には12ヶ月の安定であるという結果を出していきたいと考えています。来年には、さらにこれを延長させて18ヶ月まで安定なものを作っていきたいと考えます。
「⑥内視鏡投与に関する知的財産権の獲得」は、先ほどお話ししたように、国内においては達成できました。
「OBP-601」に関する⑦⑧の事項についてご説明します。
「⑦ピボタル試験の開始とマイルストーン受領」とは、要するにPhase3の臨床試験開始のマイルストーンをトランスポゾン社から受領したいと考えています。
「⑧アルツハイマー病で新たな試験を開始」は、我々がみなさまにご期待いただきたく挙げています。
2025年12月末のパイプラインの見通し
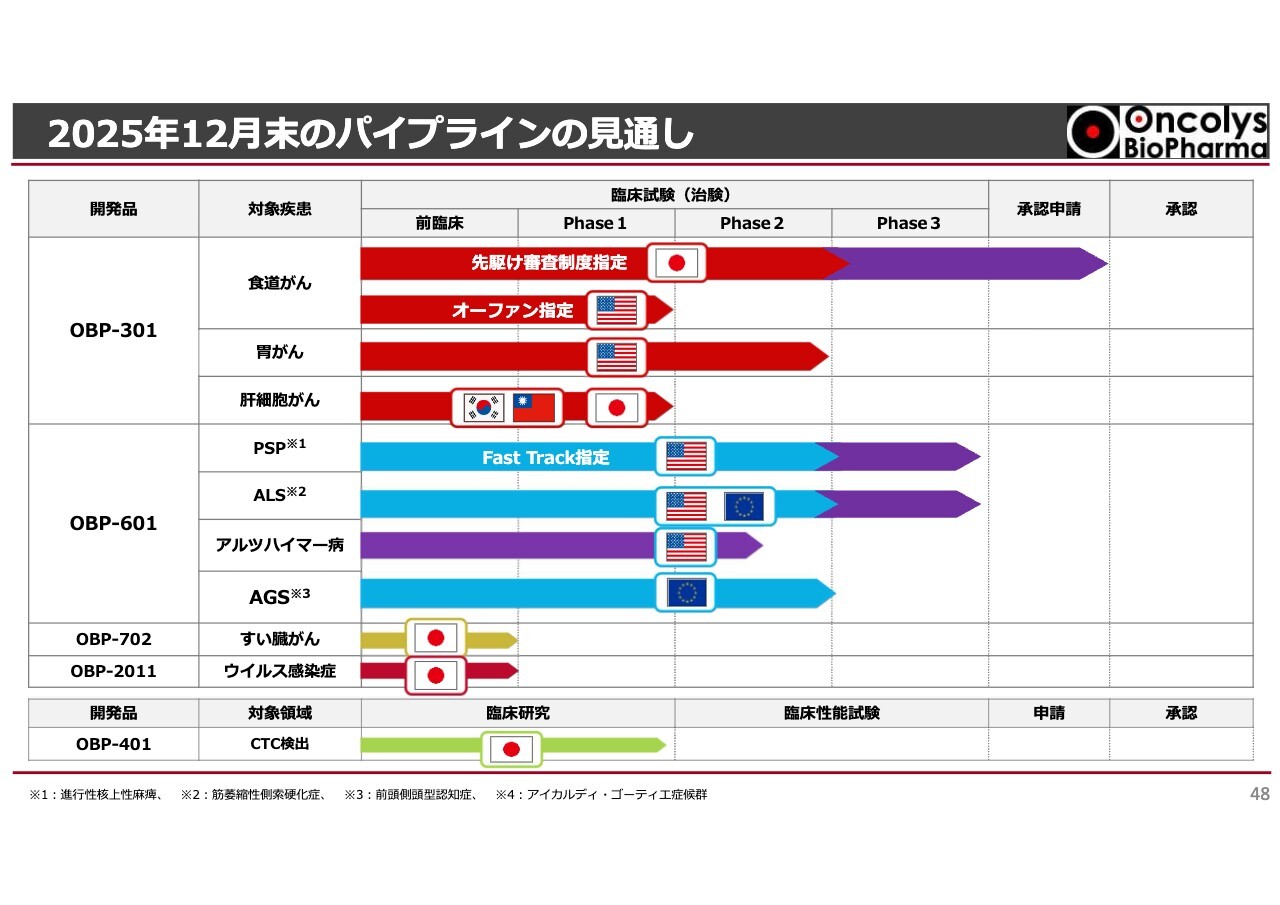
2025年12月末のパイプラインの見通しを示しています。今年末においては、承認申請を行い、「OBP-601」が最終臨床試験に入っている、アルツハイマー病で新たな試験が進んでいるなど、このような状況をみなさまにご報告できるように、最善を尽くしていきたいと考えています。
経営戦略

当社はこれまで、研究開発をし、それをライセンスしてお金を受け取るという「ライセンス型事業モデル」でしたが、それだけではなく、今後は製造販売等ができて、自分たちで製品の利益を得ることができるような「製薬会社型事業モデル」にしていきたいと考えています。そのようなハイブリッド型の会社を目指して邁進していきます。
質疑応答:同等性について
質問者:「商用製造の課題」の話が出ました。昨年の事業説明会で私が同じ質問を行った際、浦田社長はゲノム解析により同等性、同一性が証明できると回答されたのですが、先ほどのお話はゲノム解析なのですか?
浦田:昨年お話ししたのは、「テロメライシン」の特徴的なテロメラーゼプロモーターとIRESという遺伝子の組み合わせについてです。「テロメライシン」の特徴的な構造について、重要なポイントできちんとゲノム解析を行い、同じものであると確認しています。
それだけではなくて、不純物はどうか、ヒトのがん細胞で作っているため微量のタンパク質や遺伝子が入っていないかなど、製剤全体でいろいろなことを調べます。その中にはゲノム解析も入っています。
質疑応答:「キイトルーダ」の特許期限切れが近づく中での動きについて
質問者:コーネル大学で、メルク社の「キイトルーダ」と併用して治験中ですが、「キイトルーダ」の特許期限が2028年で、あと3年しかありません。メルク社以外とのアライアンスの可能性はありますか?
浦田:メルク社の特許については我々も調べています。2028年頃に特許が切れるのですが、メルク社はおそらく「キイトルーダ」を守るために相当多くの特許を出しています。2028年に後発品は出てくるでしょうが、それがすべての病気で使えるということにはならないと思います。胃がんに後発品が出てくる時期はもう少し後になると想定しています。
現在メルク社がどこまで力を入れているのかは、我々にもわからない部分があります。少なくとも試験が始まる2024年の段階で、メルク社がただでサンプルを出して一緒に実施していくと決定したということは、決して後ろ向きで行っているわけではないと思っています。この試験だけではなく、先ほどお話しした「化学放射線療法の試験で、がんがなくなる」という結果をもとにして、いろいろな大手製薬会社とも話し合いをしています。
このようなことを踏まえて、どのように取り組んでいくかを考えています。
質疑応答:トランスポゾン社の資金調達について
質問者:浦田社長が訪米してトランスポゾン社の首脳とお会いになったとい
新着ログ
「医薬品」のログ





