サスメド株式会社 2023年6月期第2四半期決算説明
サスメド、不眠障害治療用アプリの製造販売は正式承認待ち 他のパイプラインでも開発が進捗
ビジョン

上野太郎氏(以下、上野):みなさま、お集まりいただきましてありがとうございます。サスメドの上野でございます。よろしくお願いいたします。2023年6月期第2四半期の決算説明資料に沿ってご説明いたします。
私どもは「ICTの活用で『持続可能な医療』を目指す」をビジョンに掲げており、「SUStainable MEDicine」を略して、サスメドと称しています。
このビジョンを達成するための具体的な取り組みを2つご説明します。1つは治療用アプリのDTx(Digital Therapeutics)で、各疾患に対してDTxのプロダクトを開発し、医薬品や医療機器と同様に患者・医療従事者向けにプロダクトを提供しています。
もう1つはDTxプラットフォーム事業です。製薬企業の方々が臨床試験を行う際に、効率よく治験のレギュレーションを担保しながら実施できるような取り組みや、機械学習のデータ分析などをBtoBで実施しています。
事業領域概要
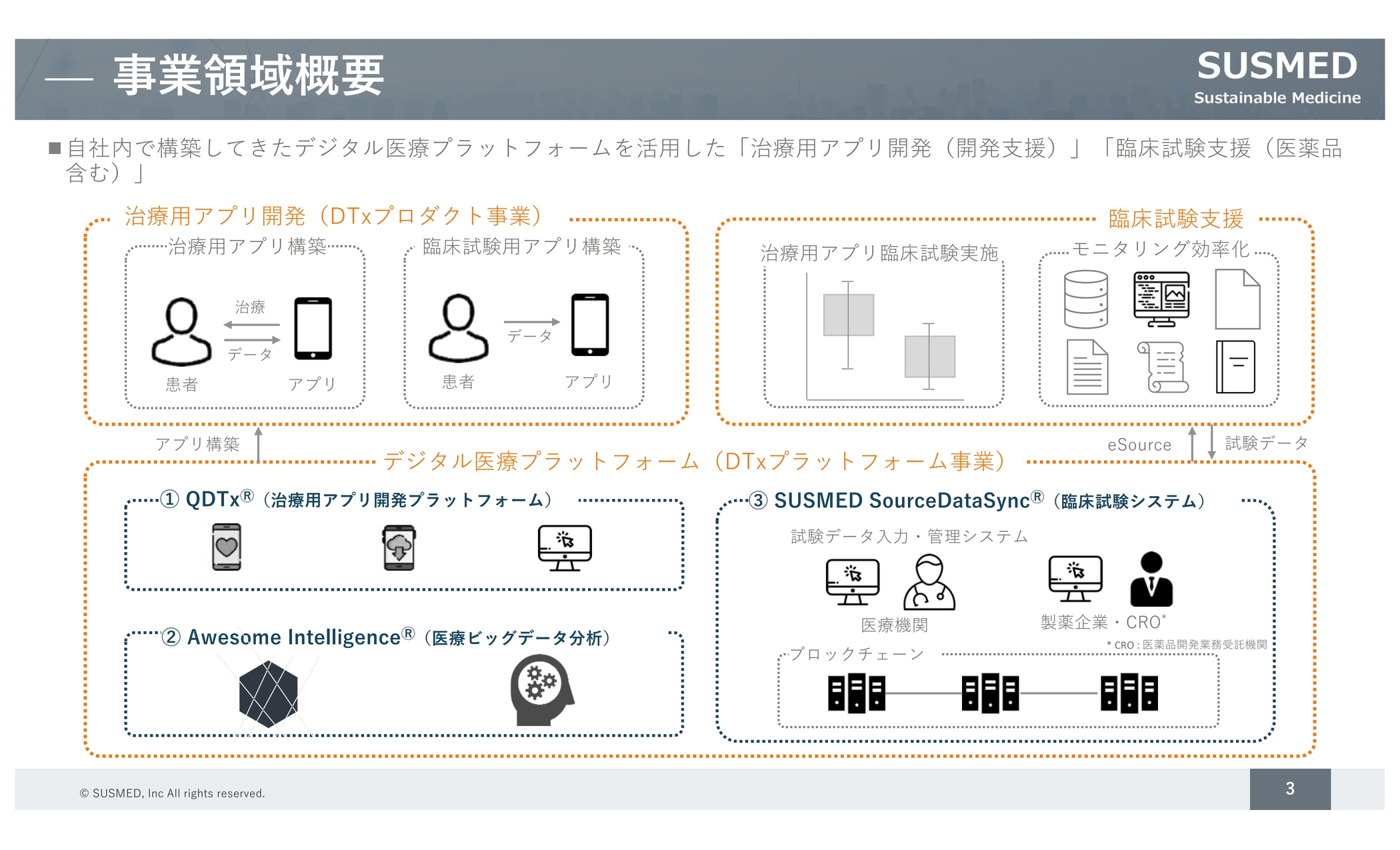
スライドには実際の取り組みの全体像を記載しており、大きく分けて2つの取り組みがあります。1つは治療用アプリの開発、もう1つは、治療用アプリに限らず医薬品やハードウェアの医療機器も含め、臨床試験の効率化を図る取り組みです。
これらの事業を進める上で私どもの強みになるのが、スライドの下部に記載しているデジタル医療プラットフォームです。具体的には3つの取り組みがあります。1つ目が「QDTx」で、治療用のアプリを効率よく開発するためのプラットフォームです。こちらを活用することで、初期段階の治療用アプリのPOCを迅速に取得できる仕組みになっています。
2つ目は「Awesome Intelligence」です。このような治療用のアプリが世の中に出てくると、デジタルデータや医療データが日々生み出されるようになるため、そのデータの利活用を見越し、機械学習による医療データ分析のプラットフォームを構築しています。現在、こちらの基盤を使って医薬品の医療ビッグデータを分析し、製薬企業など向けに事業展開をしています。
3つ目は「SUSMED SourceDataSync」です。特に臨床試験支援に関わる部分ですが、臨床試験を効率よく実施するための基盤システムとなっています。特徴として、当社は医療分野にブロックチェーン技術を用いるという知財・特許を持っているため、これを用いることにより規制が求めているデータの信頼性と効率性を両立させることができます。
治療用アプリの提供の流れ
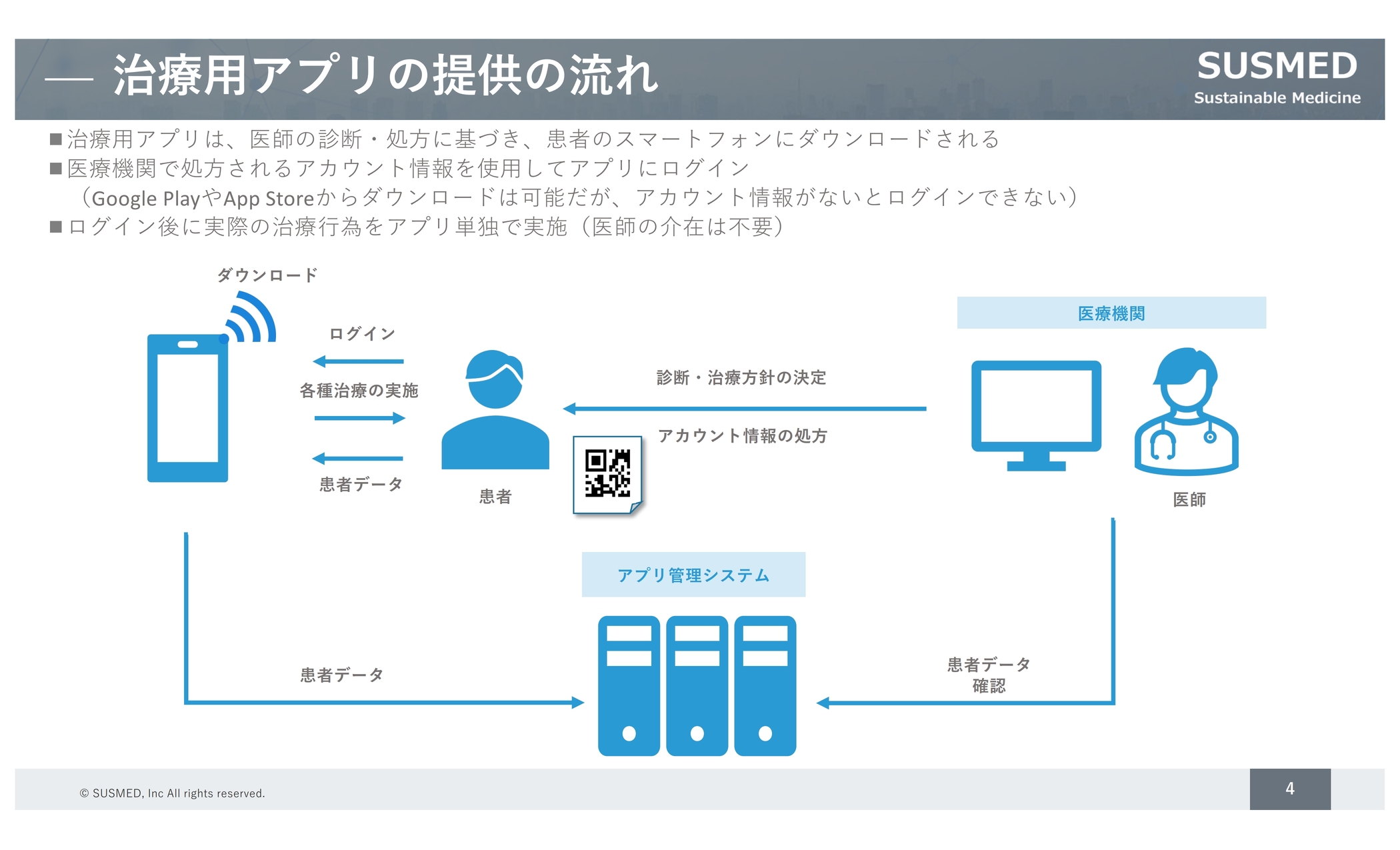
最初に、治療用アプリからご説明します。治療用アプリは医療機器に該当します。そのため、通常の医薬品やハードウェアの医療機器と同じように、医師の診断・処方に基づき、患者が使えるものになっています。これまで医薬品は医師が処方していましたが、この治療用アプリにログインするためのアカウント情報を処方して、初めて患者が使えるという仕組みです。
治療用アプリは、遠隔診療とは異なりアルゴリズムで提供されるため、裏側に医師が必要なわけではなく、医師はアカウント情報を処方するだけで治療が行えます。その後の治療介入については、スタンドアローンで実施できるところが大きなポイントになります。
また、日々スマートフォン経由で患者のデータがサーバーに集まってくるため、医療ビッグデータを活用していくことも新たなポイントですし、データを医師が確認することで、治療方針の最適化が図れることも新しい分野になっていくと考えています。
ヘルスケアアプリと治療用アプリの違い

世の中にはコンシューマー向けのヘルスケアアプリが多数ありますが、それらとの大きな違いについてご説明します。既存のヘルスケアアプリはあくまで健康増進が目的ですので、健常者が健康管理や健康増進のために用います。例えば、歩数や血圧の記録などが主眼になっており、治療を行うことはできません。
一方、私どもの治療用アプリは医療機器に該当し、治療を行うものですので、他の医薬品や医療機器と同じように治験を実施して、エビデンスをもとに厚生労働省による承認を受ける必要があります。
また、日本には国民皆保険制度がありますので、保険を活用することで患者は一部を費用負担すれば使用することができます。医師が処方を行うため、医師に対してのマーケティングが非常に重要になってきます。
開発パイプライン①(2023年2月10日現在)
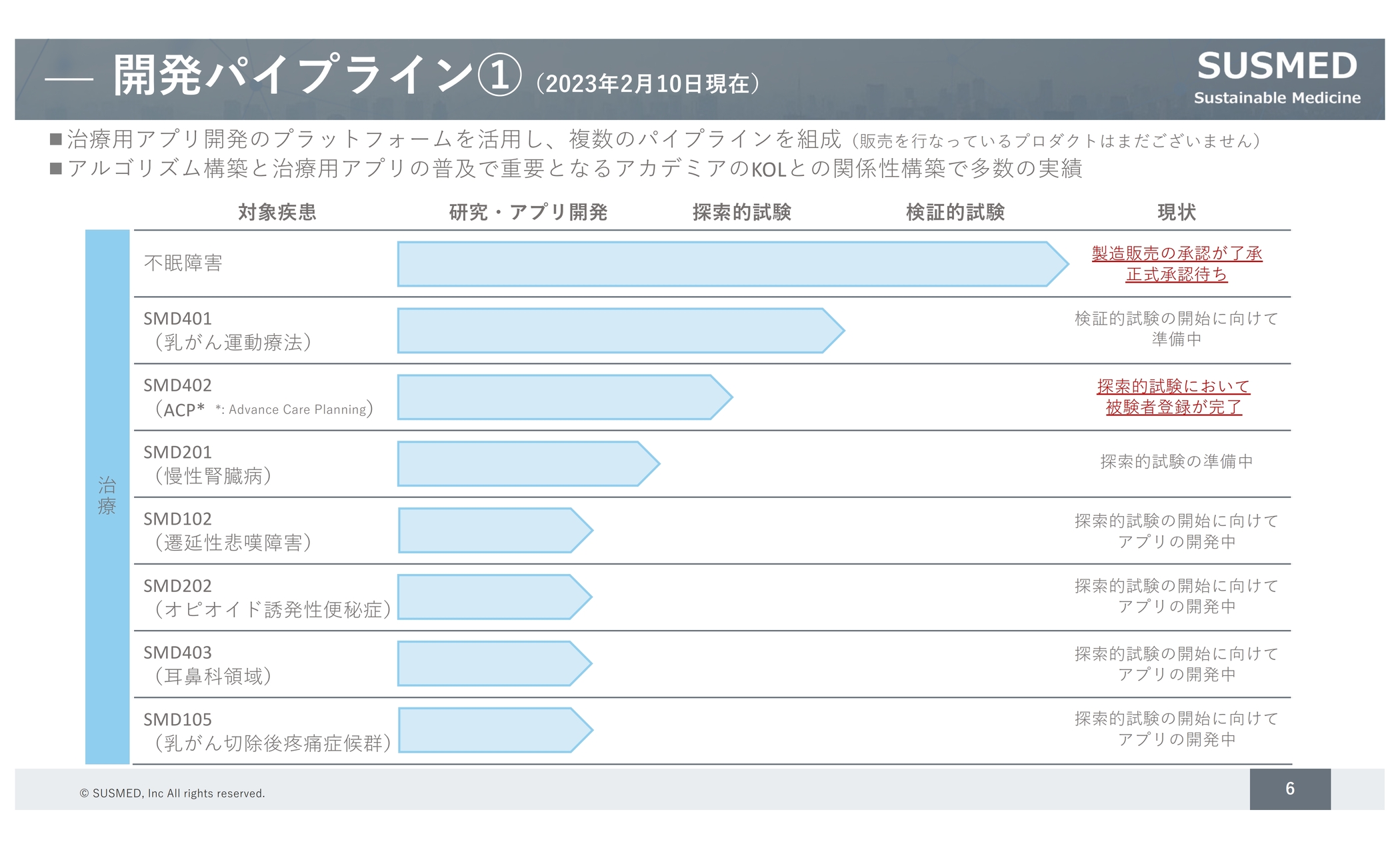
私どもは治療用アプリのパイプラインを多数保有しています。不眠障害治療⽤アプリについては、昨年2月1日に承認申請し、12月に承認の了承を受けている状況です。
また、今回アップデートがあったのは、「SMD402」というプロジェクトコードで呼んでいる「ACP(Advance Care Planning)」のアプリで、末期がん患者に対して治療方針の策定を行うものです。これまで探索的試験を実施していましたが、アップデートした点として、被験者登録が完了しました。それ以外の治療用アプリのパイプラインについても、それぞれ研究開発を進めている状況です。
開発パイプライン②(2023年2月10日現在)
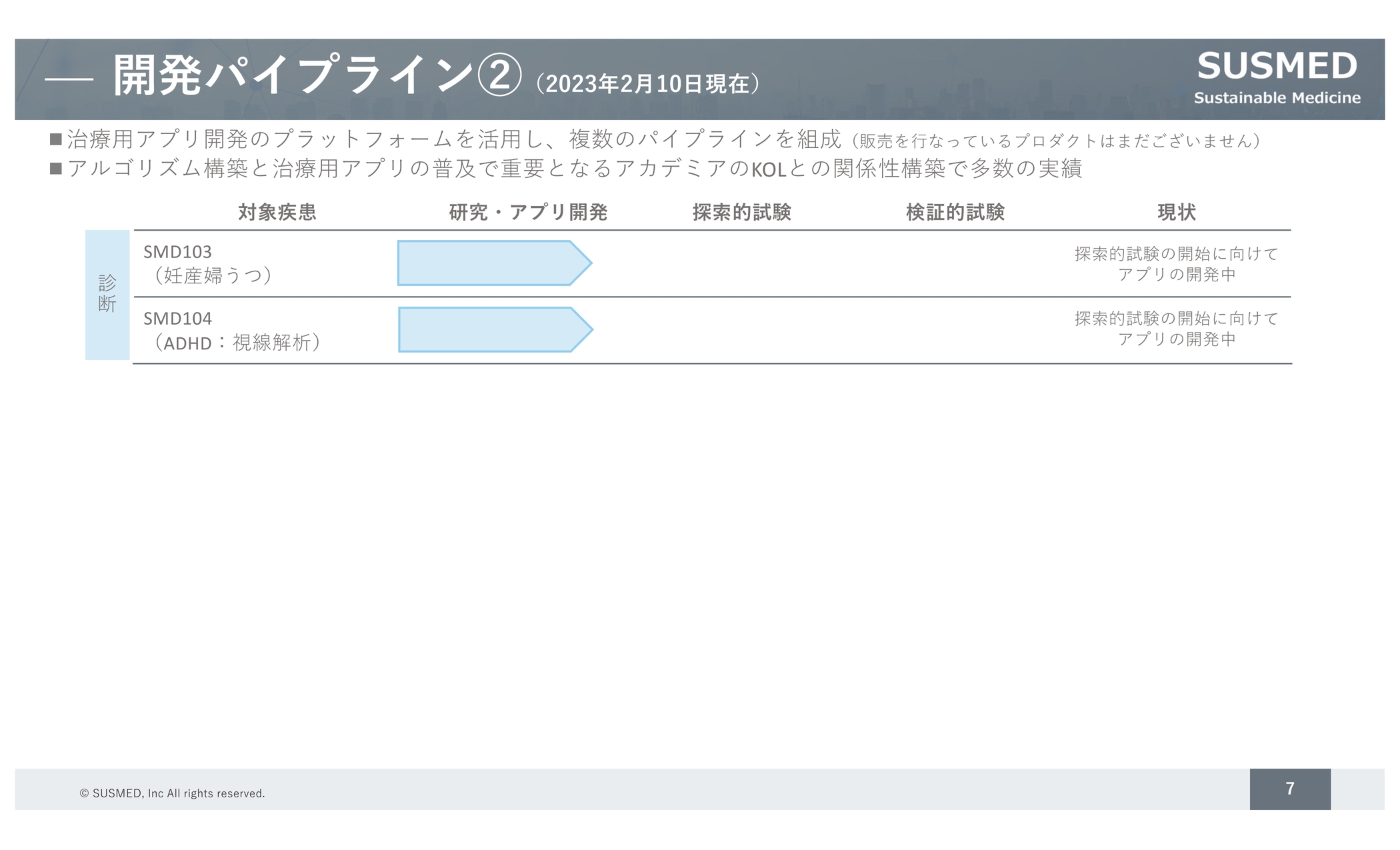
診断用のアプリのパイプラインです。こちらもそれぞれ研究開発を進めています。
汎用臨床試験システム:SUSMED SourceDataSync

DTxプラットフォーム事業についてです。「SUSMED SourceDataSync」という臨床試験を効率化するためのシステムでは、ブロックチェーン技術の活用により、治験で求められる臨床試験データのモニタリング業務を行っています。通常では、CRO企業(医薬品開発業務受託機関)のモニターと呼ばれる方が実地でダブルチェックを行っていますが、私どものブロックチェーンの技術でその業務を代替できるシステムになっています。
ブロックチェーン技術の実装による効率化
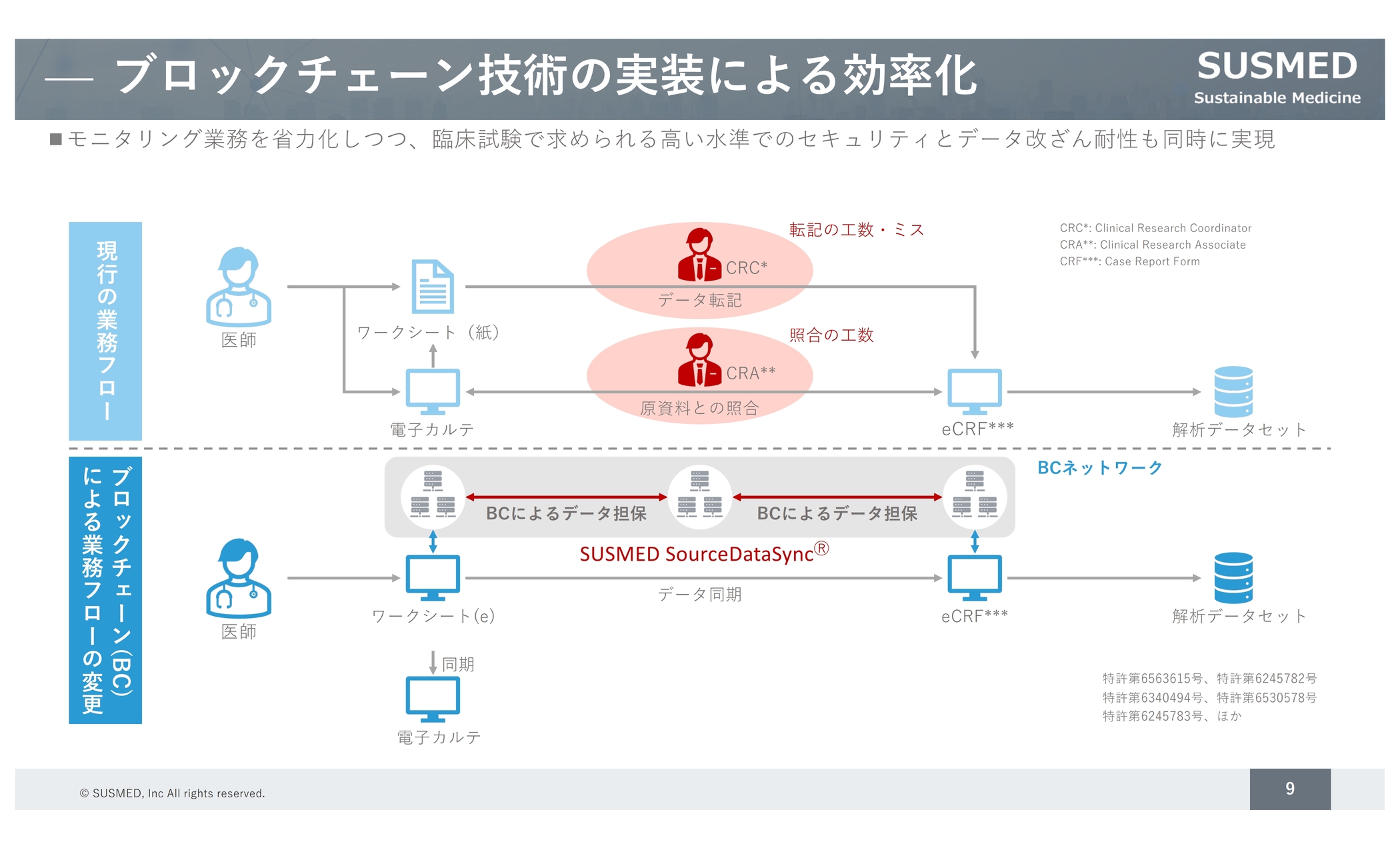
このような技術による効率化の仕組みをスライドに記載しています。治験業務は、医師が電子カルテに医療データを入力したあとに、CRCという職種の方がデータの転記作業を行い、製薬企業などの依頼者が承認申請をするための症例報告書である「eCRF」を作成します。このデータの真正性を担保する必要があり、GCP省令というレギュレーションがあります。
これまでの業務フローでは、このレギュレーションの担保のために、CRO企業から派遣されたCRAという職種の方が医療機関を訪問し、医療機関のカルテ情報である原資料データとの照合作業を実地で行っていました。
それに対して、ブロックチェーンを使うと、医療機関の原資料をブロックチェーン経由で「eCRF」に繋ぎこむことができます。ブロックチェーンにはデータ改ざんを防ぐことができるという特性があるため、原資料との照合は不要という規制当局の通知が出ており、その通知をもとに、業務が効率化できる仕組みになっています。
機械学習自動分析システム:Awesome Intelligence
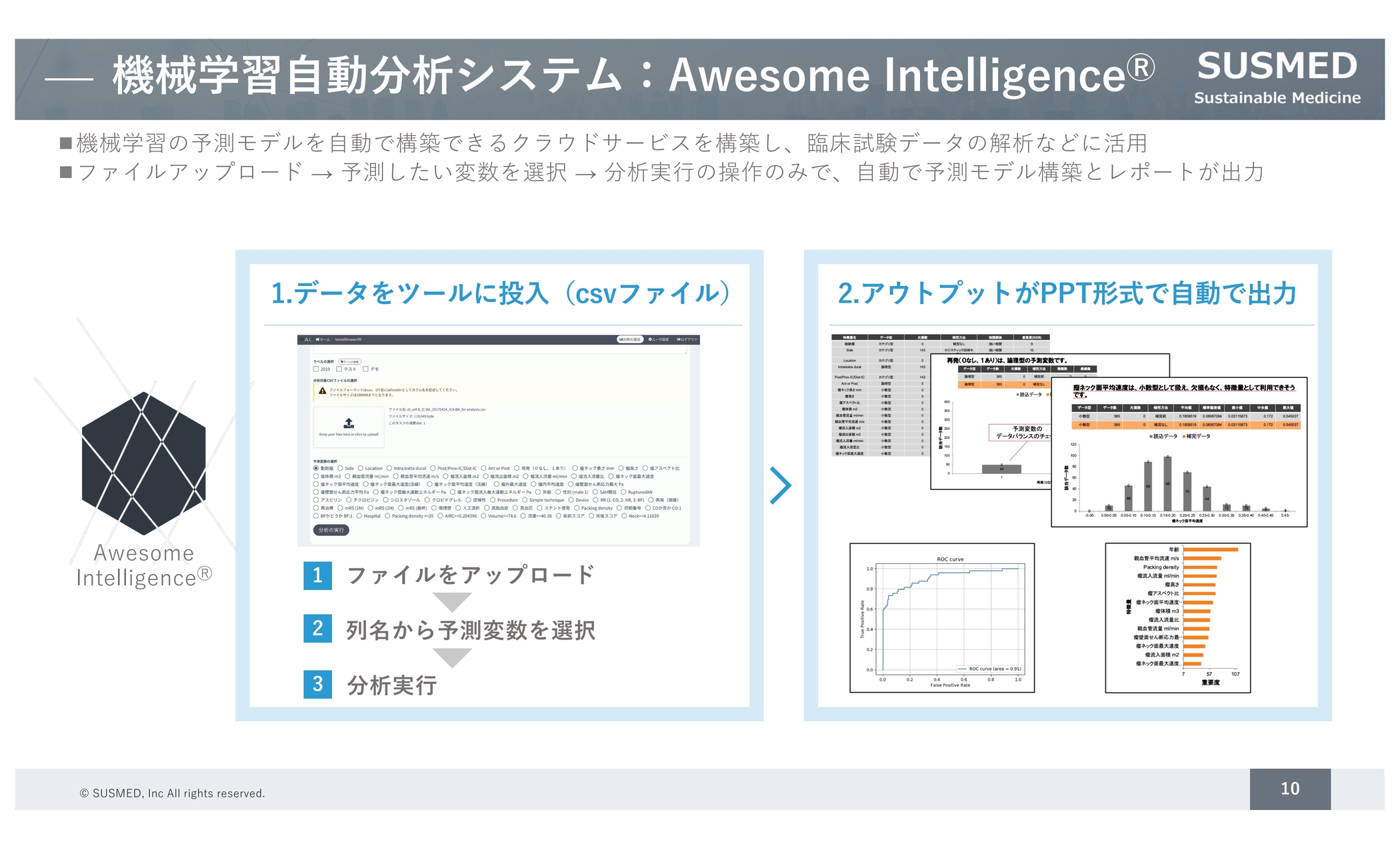
機械学習自動分析システムについてです。データサイエンティストが張り付くことなくクラウドサービスとして機械学習が実施できるサービスとしてSaaSのシステムを構築しており、製薬企業や医療機関など、企業との共同の取り組みで活用を進めているところです。
2023年6月期 重点施策

期初に掲げていた4点の重点施策を具体的にご説明します。不眠障害治療用アプリについては、製造販売承認を取得します。また、後続のパイプラインについては、「SMD402」「SMD201」の被験者登録を完了させることを目標に掲げています。
ブロックチェーンシステムについては、承認申請のための企業治験での稼働や、さらに治験から領域を広げ、レジストリなど治験以外の医療データにまで広げることを掲げています。
重点施策① 不眠障害治療用アプリの製造販売承認取得
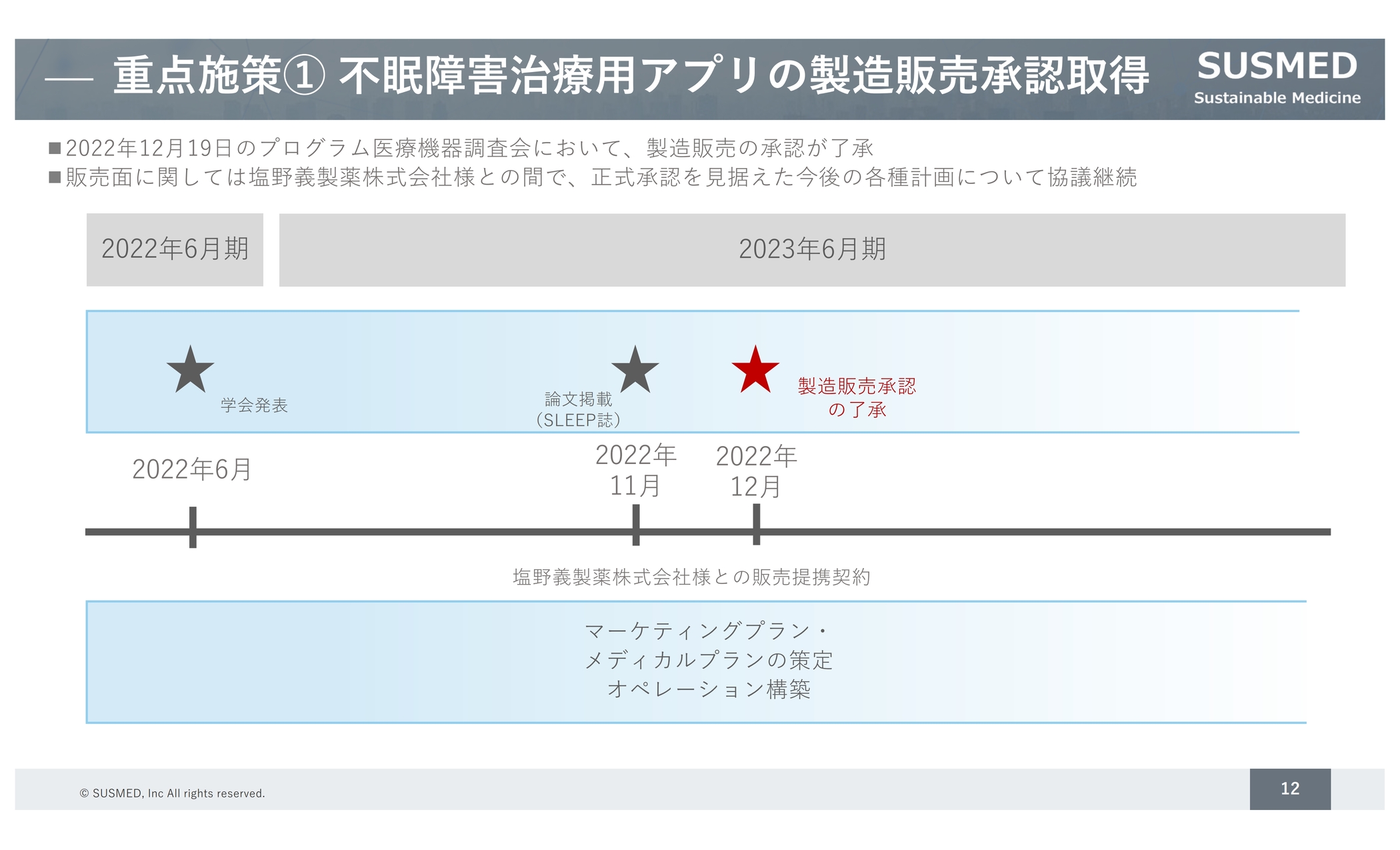
1点目の不眠障害治療用アプリの製造販売承認取得についての進捗です。非常に大きなポイントとして、昨年12月19日の部会の審議において、製造販売の承認について了承されています。年末年始を挟んだため、手続きに少し時間がかかっているとのことですが、承認の了承もされていますので、現在、正式承認を待っている状況です。また、『SLEEP』というこの分野のトップジャーナルで、論文が掲載されています。
その他、正式承認後の販売のところの準備を進めています。塩野義製薬とマーケティングプランの策定とオペレーションの構築を行い、全国の医療機関にくまなく届けるための協議を進めている状況です。
重点施策② SMD402の臨床試験の進捗
2点目のパイプラインの進捗についてです。国立がん研究センターとの共同研究として、「ACP」用プログラムの医療機器を開発しています。こちらは、厚⽣労働科学研究にも採択いただき、厚生労働省とコミュニケーションをとりながら臨床研究を進めてきました。
現在被験者の登録が完了し、介入期間と観察期間に入っている状況ですので、終了次第、結果の取りまとめができればと考えています。「ACP」用プログラム医療機器に期待している効果は、終末期の患者における不安や抑うつ症状を改善できるという先行研究があるため、それをアプリで実現できるかということです。
また、死亡直前の抗がん剤の投与が国としても大きな問題になっています。死亡直前まで副作用や医療費が問題になる抗がん剤を投与するのではなく、早期の緩和ケアを実現することが目的になっています。
また、診療報酬についても、「ACP」分野の診療報酬が令和4年度の診療報酬改定で確定されています。がん患者指導管理料という保険点数がついているため、そちらを活用していければと考えています。
重点施策③ 企業治験での臨床試験システムの稼働開始

3つ目の臨床試験システムの企業治験での稼働についてです。初めてのブロックチェーン治験として、ナルコレプシーの患者に対してのフェーズⅢの治験をアキュリスファーマと共同で開始していました。これに続いて、睡眠時無呼吸症候群に対しての治験についても新たに開始しています。
これまで2つの企業治験において、ブロックチェーンを使った臨床試験システムが稼働している状況になっています。
治験の対象はリアルな医薬品であるヒスタミンH3受容体拮抗薬で、逆作動薬でもある「Pitolisant」です。この医薬品は、海外ではすでに承認されていますが、国内における承認を取るためのフェーズⅢの治験にブロックチェーンを使ったシステムが現在動いている状況になっています。
先ほどその効果についてご紹介しましたが、この仕組みを使うことにより、データ入力や照合作業に関わる工数を削減し、効率よく治験が実施できます。また、治験データの信頼性をより向上させる取り組みになります。
2023年6月期 重点施策の現在地(2Q時点)

第2四半期における各重点施策の進捗です。不眠障害治療用アプリについては、製造販売の承認が了承されていますので、正式な承認通知を待っている状況です。パイプラインについては、「SMD402」の被験者登録が完了しました。引き続き「SMD201」のリクルートを進めています。
企業治験については2つ同時に動いています。ブロックチェーンの治験以外では、レジストリでの活用があります。こちらも今年度からAMED(国立研究開発法人日本医療研究開発機構)の事業が新しく始まっていますので、活用に向けて協議を進めています。
業績ハイライト
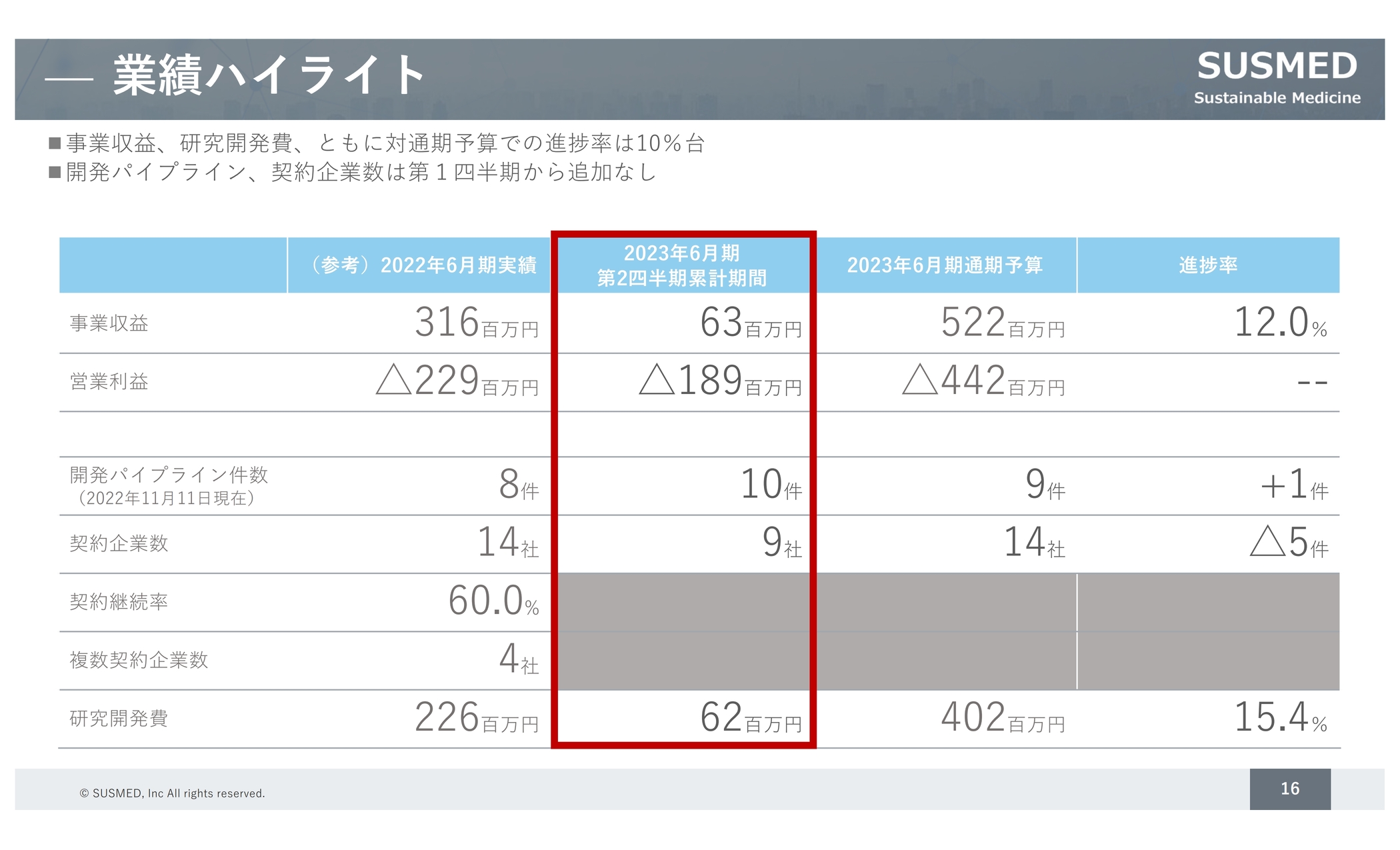
業績についてです。スライドの赤い囲みの部分が第2四半期累計の実績となっています。事業収益の進捗は12パーセントですが、変更はしない予定です。
開発パイプライン件数は、第1四半期の時点で杏林製薬とのパイプラインが1件追加されました。また、名古屋市立大学との取り組みがアカデミアとの取り組みに追加されたため、今期の予定を1件超過している状況ですが、こちらについても変更ありません。
契約企業数は、通期予算に対してプラス5件を予定しています。研究開発費は、通期予算4億円に対し6,200万円となっています。
セグメント業績
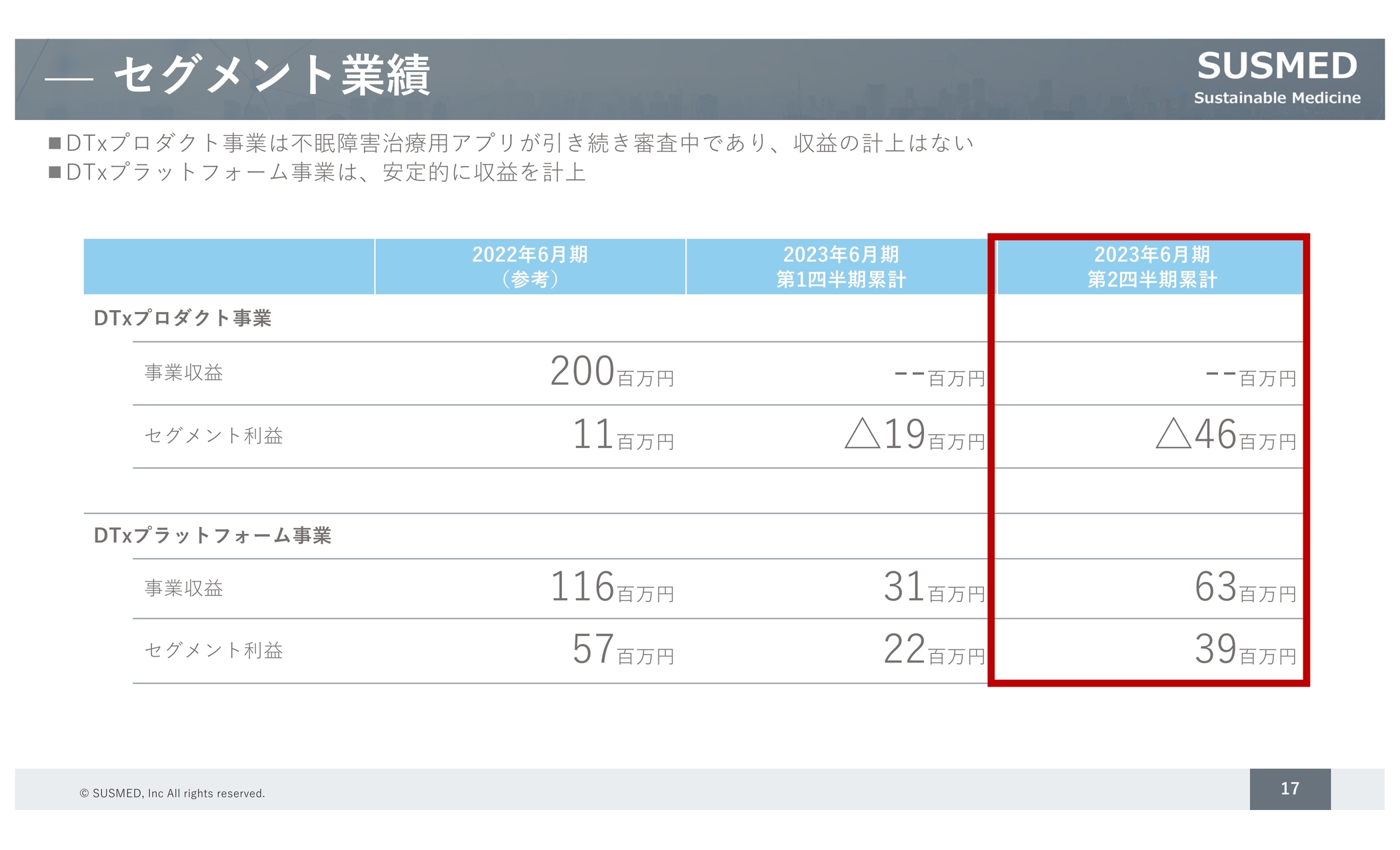
各セグメントの業績になります。DTxプロダクト事業については、前期に塩野義製薬との販売提携契約で2億円計上していますが、今期の第2四半期時点では計上はありません。
また、DTxプラットフォーム事業については、安定的に収益が上がっている状況です。第1四半期と比べても第2四半期は事業収益が伸びています。
財務状況
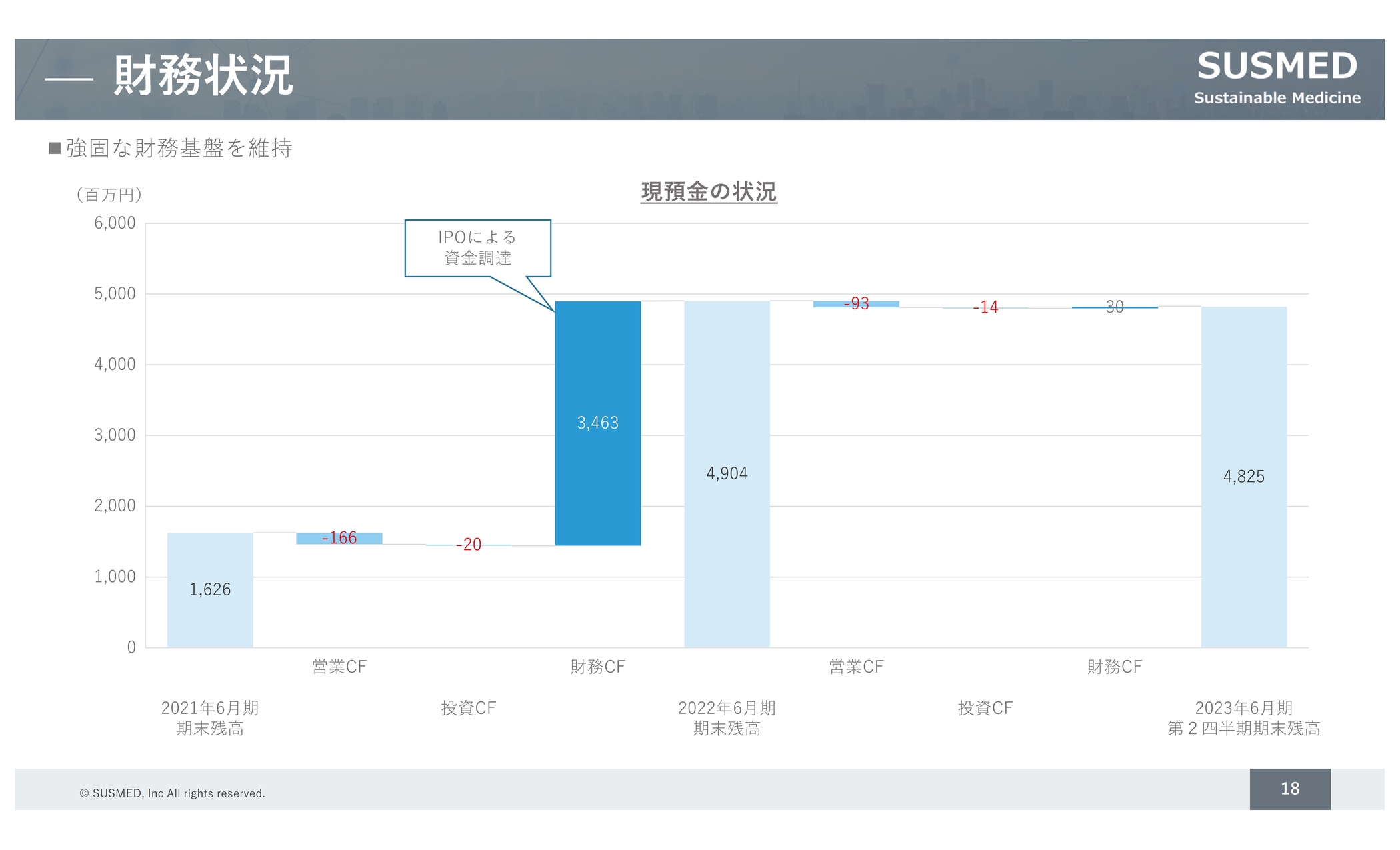
財務状況についてです。IPOで資金調達を行ったため、前期末時点で49億円現預金がありました。第2四半期の状況としては48億円の資金があるため、強固な財務基盤が維持されています。
2023年6月期業績予想の見直し
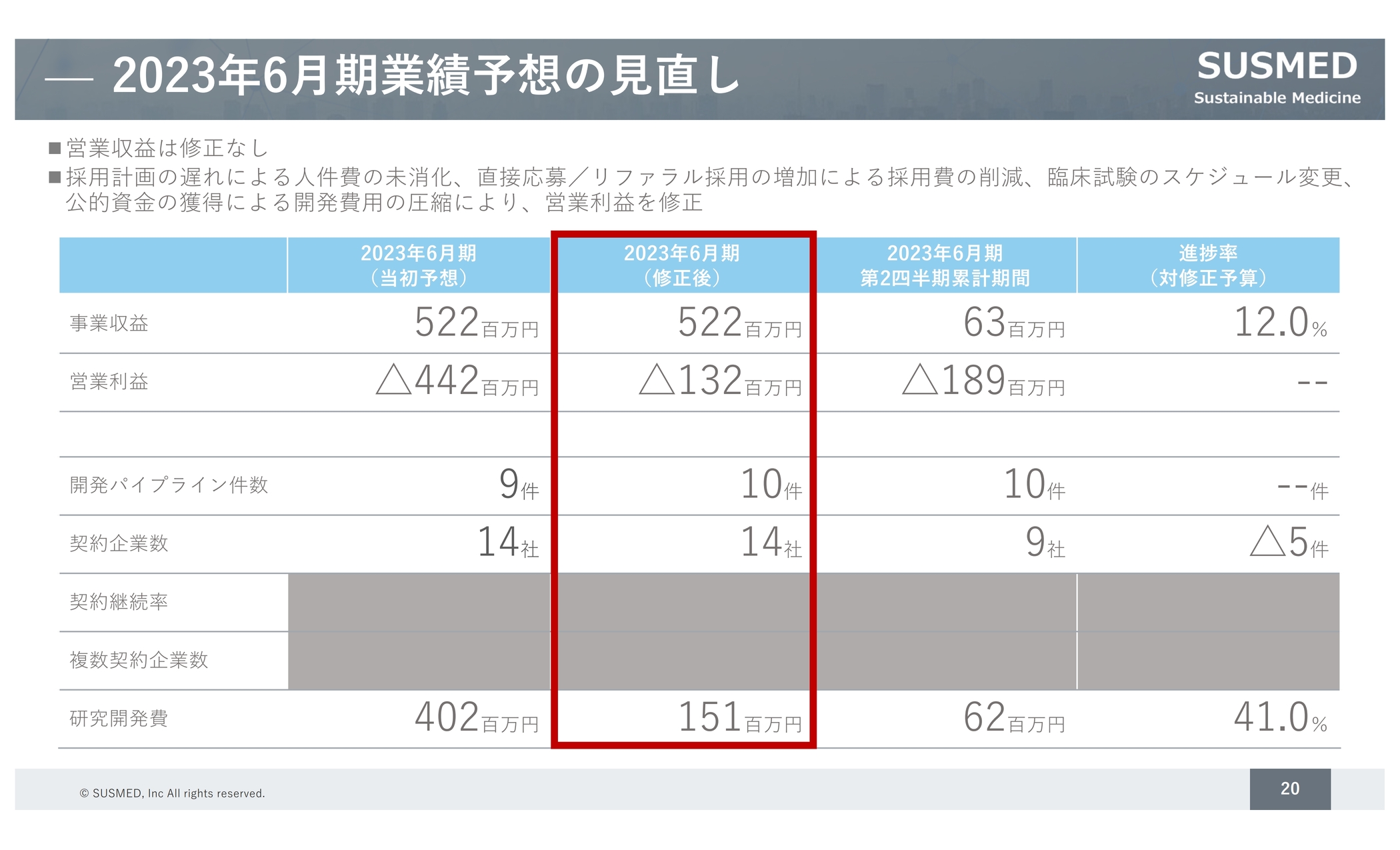
業績予想の修正について説明します。事業収益は当初の予算どおりの見込みです。一方、営業利益は当初マイナス4億円の赤字を見込んでいましたが、販管費が圧縮できる見込みになったため、マイナス1.3億円を見込んでいます。
特に大きいのは人件費の部分で、リファラル採用などにより採用費が削減できた実績があります。また、期中でもいくつかリリースしていますが、複数採択いただいた公的資金の獲得により研究開発費が圧縮できる見込みとなり、営業利益を上方修正したかたちになっています。
質疑応答:不眠障害治療用アプリについて
質問者:不眠障害治療用アプリについて、可能な限り詳細を教えてください。無事に部会を通過し、我々を含め株式市場は承認の通知を待っているところですが、今業界誌などでいろいろな憶測が出回っています。
現状は、トラブルや書類のキャッチボールの遅れなどではなく、単に年末年始を挟んだことで業務のタイミングが1ヶ月をオーバーしたためで、現在ボールは相手方にあると理解してもよいですか?
上野:本当に私どもも純粋に待っているところです。なにか遅れや支障があるとは認識していません。担当者の話では、年末年始を挟んだ影響により、通常より少し時間かかっているとご連絡はいただいています。
書類の不備や支障になるものについては、特段何も言われていません。基本的には当局側にボールを持っていただいています。そのため、本当に毎日待っている状況です。
質問者:正式な承認の通知が出ていないためコメントしづらいと思うのですが、不眠障害治療用アプリの適用患者に制限が入るのではないかという憶測が業界誌などを通じてあります。
我々は部会でどのような議論があったのかわかりませんが、一般的にこのフェーズⅢの組み入れ基準が踏襲されると理解しています。適用患者や医師の使用要件で制限がつくなどの議論があったのか確認させてください。
上野:適用の部分については、私どもも制限がかかるとは認識していません。治験自体もそのような通常の不眠症治療におけるプロトコルで行っているため、これを制限することはないと思っています。
おそらく補助や支援などの文言の追加について業界誌などに掲載されているため、憶測を呼んでいると思います。こちらについて先方とのやり取りの中では、前例に従い補助や支援の言葉を入れるように言われています。
プログラム医療機器としてすでに承認されているものが2品目ありますが、そちらのほうで補助をつけていることが前例としてあります。部会の議論では、その前例に従うというご指摘をいただいたと聞いています。しかしながら、それが適用患者や使用要件に制限を加えるものではないと認識しています。
質疑応答:ブロックチェーン技術について
質問者:ブロックチェーン技術についてお伺いします。企業治験が2つスタートし、堅調だと思います。企業治験が始まった場合、基本的に月々の収益になると理解してよいですか? また、アキュリスファーマ以外の企業からの引き合いはありますか?
これが始まると収益構造も徐々に変わってくると思います。現状の引き合いなど、もしコメントできることがあれば教えてください。
上野:こちらのシステムについては臨床試験の実施期間で按分して計上していくかたちのため、始まった時点で一括計上はされない認識です。引き合いについては、いろいろといただいているところもあり、先日リリースしたようにCRO企業との取り組み等も行っています。
今回、CRO企業のリニカル、ClinChoiceと業務提携しており、彼らが製薬企業に提案するという機会も増えています。また、実際に当社に対して「御社の試験システムを使って、効率的に臨床試験を行いたい」と直接お声掛けいただく機会も、かなり増えている状況です。
質疑応答:今期の契約企業数の見通しについて
質問者:今期の契約企業数の見通しについて、プラス5件を予定しているとお話があったと思います。残り4ヶ月で5件となると、ハイペースで契約しないと達成できないのではないかと思いますが、こちらの状況や引き合いなど、ご説明できることがあればお願いします。
上野:おっしゃるとおり、リードタイムがそれなりに長い分野です。すでに契約している企業以外でも、これまで継続的にコミュニケーションをとっている企業がありますので、そのようなところが積み上がって、期末で予定の契約企業数を達成できればと考えています。
先ほどお話ししたように、引き合いや相談はいただいていますので、数字の達成に向けてしっかりと進めたいと考えています。
質疑応答:2023年6月期業績予想の見直しについて

質問者:今期の業績予想修正について、営業利益の損失幅が従前より3.1億円ほど縮小するというのは、研究開発費が2.5億円圧縮されたことが大きいと思っています。公的資金の獲得というお話もありましたし、スケジュール変更も影響しているのかなと思います。
第2四半期累計の助成金収入は129万円としていますが、公的資金の獲得について、これ以外にも第3四半期、第4四半期でいろいろと見込みがあり、圧縮されているのでしょうか? この部分のみであるならば、むしろスケジュール変更のほうが研究開発費の圧縮に大きくはたらくと思います。このあたりについて、もう少し詳しく教えていただきたいです。
上野:公的資金の採択については、私ども単独ではなくアカデミアや医療機関も含めたかたちでの採択となっていて、当社が外部に支払う予定としていた開発費用も含めて圧縮できています。資金以外の部分でも、プロジェクトを進める上でのインパクトはそれなりにあると思っていますし、このような公的資金を獲得することで、プロジェクトとして前進しやすくなっていると考えています。
また、今期に見込んでいた臨床試験の開始費用については、臨床試験自体を来期以降に実施する計画になったことも影響しています。

質問者:今期の重点施策2つ目に「SMD402」「SMD201」の被検者登録完了とありましたが、「SMD201」のほうが少し遅れているのでしょうか? 研究開発費の圧縮はこれが原因でしょうか?もしくはそれ以外でしょうか?
上野:おっしゃるとおり、フェーズが先に進めば進むほど、実際の試験プロトコルを固める部分などで議論が発生するため、その部分で当初見込んでいた予算の消化がないというのが、今期の状況だと思います。
質問者:予算の消化状況について、案件ごとに提示していただくのは難しいでしょうか?
上野:個別の案件については開示していません。
質疑応答:不眠障害治療用アプリを使用できる医師について
質問者:不眠障害治療用アプリについて、承認取得前でコメントは難しいとは思いますが、もし可能であればお願いします。
メディアの文言の中に「不眠障害に関連する十分な知識を有する医師が行う」という内容があり、あたかも日本睡眠学会に所属する医師のみなど、処方できる医師が限られるようなニュアンスも連想させるのですが、そのようなことではないと認識してもよいでしょうか? どのような医師でも使えるものなのか、教えてください。
上野:私どももどのような医師でも処方できるものと認識していますし、実際の治験自体もそのようなかたちで実施しています。いわゆる一般のクリニックなどで治験を実施しており、学会の専門医でなければ使えないという設定ではありません。そのため、特定の医師のみが使えるわけではなく、不眠症の患者の治療において、広くこのプロダクトが使えると認識しています。
質疑応答:不眠障害治療用アプリの手離れのよさについて
質問者:不眠障害治療用アプリについて、どのくらい手離れが効くものなのでしょうか? あくまでも補助という文言が加わっただけで、患者が自宅で入力できるといった手離れのよさは、元々の想定と変わらないイメージでしょうか?
上野:おっしゃるとおり、医師が対面で時間をかけて行わなければならない認知行動療法を、アプリのアカウントを処方するだけで完了できるというコンセプトで治験を行っていますし、実際にそのようなかたちで結果が出ているため、医師に負担がかかるようなことはまったく想定していません。
質疑応答:杏林製薬からの契約一時金について
質問者:杏林製薬からの契約一時金について、確か1億円だったと思います。貸借対照表を見る限り、契約負債の部分に1億2,000万円ありますが、こちらがそれに該当するのでしょうか?
上野:そのとおりです。
質問者:これを来期の事業収益に振り替えるということですか?
小原隆幸氏(以下、小原):来期「以降」です。来期以降の適切なタイミングで振り替えます。
質疑応答:契約企業数について
質問者:開示している契約企業数について、2022年6月期が14社、足元が9社、今期予想が14社だと思います。アプリの提携契約企業では、1年間の中でこのように大きく上下するのが普通というか、契約期間としては短く設定しているというイメージでよいでしょうか?
小原:契約企業数に関しては、大半がプラットフォーム側の分析やシステム利用の契約になっています。例えば、杏林製薬のような共同開発・共同研究というよりも、プラットフォーム側でのプロジェクト型の契約のほうがはるかに多くなっています。
そのため、おっしゃるように1年未満で契約が終了する案件も多々あり、年内・期中で数字が大きく変動するかたちになっています。
質疑応答:不眠障害治療用アプリのリリースについて
質問者:不眠障害治療用アプリについて、今後、正式承認が出た際に、その中に詳細要件などリリースの文言があるわけではないと思います。普通に正式承認されて、薬だと用法・用量や薬効などが出てくると思いますが、そのようなかたちで発表されるイメージでしょうか?
上野:おっしゃるとおりで、おそらく目的や用法が出てきて、それとともにリリースするかたちになると思います。
新着ログ
「情報・通信業」のログ



