ソレイジア・ファーマ株式会社 2018年12月期決算説明会
ソレイジア・ファーマ 通期損益はマイナス24億円で赤字幅拡大 今期も赤字幅は横ばいの見通し
2018年12月期 連結業績(国際会計基準IFRS)①
荒井好裕氏:ソレイジアの代表取締役社長の荒井でございます。本日はご多用のところ、当社の決算説明会にご参席いただきまして誠にありがとうございます。
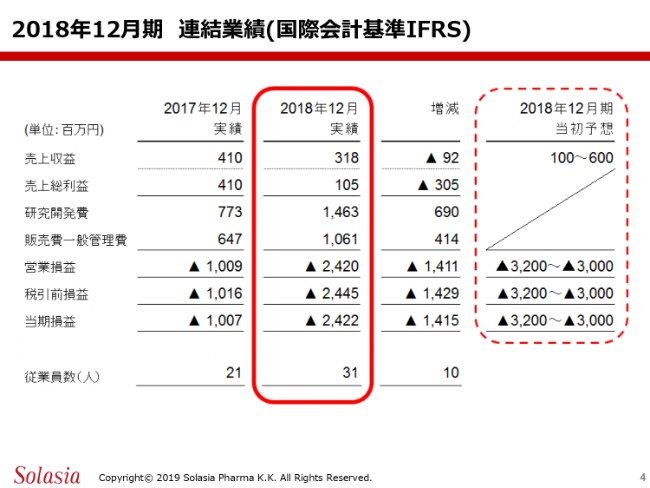
まず最初に、2018年12月期の連結業績の概要につきまして、ご報告申し上げます。2018年12月期の実績でございます。スライドでお示ししている赤い枠で囲っているところになりますが、売上収益は3億1,800万円で着地いたしました。当初の予想は、1億~6億円の範囲ということでございましたので、その枠の中に着地したということでございます。
また、売上総利益は1億500万円であります。その他、研究開発費が14億6,300万円。販売費、一般管理費が10億6,100万円であります。営業損益はマイナス24億2,000万円。税引前損益が24億4,500万円。そして、当期の損益はマイナス24億2,200万円で着地いたしました。
また従業員に関しましては、一昨年の21名から増えて、2018年は31名ということになっております。なお、営業損益、税引前損益、当期損益につきましては、当初の予想よりも少し低くなっております。
2018年12月期 連結業績(国際会計基準IFRS)②

もう少し詳しい情報について、ご報告申し上げます。売上収益でございますけれども、当初の予想は1億~6億円という範囲でございましたけれども、実績としては3億1,800万円で着地しております。
売上原価は、当初の予想が5,000万~4億円という予想でございましたけれども、実績は2億1,300万円ということで着地しております。この内容といたしましては、SP-01の中国向け製品の販売等によるものであります。
またもう1つは、SP-03の日本向け製品の販売等で占められております。また、研究開発費でございますけれども、当初の予想は13億~14億5,000万円という想定でございましたが、実績としては14億6,300万円ということで、ほぼ予想の範囲ということが言えるかと思います。
内容といたしましては、代理用製品であるSP-02のアジア共同第Ⅱ相臨床試験……これは最終試験でございますが、こちらの費用およびSP-04の国際共同第Ⅲ相臨床試験で、こちらも最終の試験でありますけれども、この2つの臨床試験の実施費用として使用しております。
また、販売費および一般管理費は、当初予想を18億~19億円と予想しておりましたけれども、実績としては10億6,100万円で着地いたしました。この内容ですが、まず中国のマーケティングの活動費で、実際にはSP-01とSP-03の販売開始の準備にかかる費用であります。
また、中国のセールス体制の構築ということで、こちらの費用であります。さらに、当社全体の体制の維持費にも費やしております。
さらにこの中には、無形資産の償却を開始しておりますので、この額として1億4,800万円が含まれているということになります。
2018年12月期 連結財政状態(国際会計基準IFRS)

次に、2018年12月期の連結の財政状況です。これもIFRS会計でございますけれども、こちらについてご報告申し上げます。2018年12月期の現預金は40億4,600万円です。また、棚卸資産は1億2,200万円。無形資産は31億円2,300万円で、その他資産としては4億3,600万円。合計で77億2,800万円というかたちです。
またこれらは、2017年12月期に比べて増加しております。負債としては、6億4,100万円で、資本金、資本剰余金の合計額が151億1,500万円であります。利益剰余金等につきましては、79億7,500万円のマイナスで、自己株式としてマイナス4,800万円を計上しております。
内訳ですが、現預金が増えた内容については、昨年9月に実施いたしました公募増資による資金調達で、32億8,600万円を調達したことが原因です。棚卸資産におきましては、SP-01の中国販売開始に備えた製品ということになります。
無形資産でございますけれども、これまでSP-01、03の開発にかけた累計額およびSP-01、02、03、04の導入に至る契約金、およびマイルストーンの支払いの累計額等で構成されております。
またSP-03の日本、またSP-01の中国の無形資産については、償却を開始しております。自己株式に関しましては、従業員向けの報酬として「J-ESOP」を昨年導入いたしましたので、こちらのためのものであります。
これに加えまして、銀行融資枠として35億円を保有しております。これは、三井住友銀行さま、みずほ銀行さまからの20億円、および15億円の合計額であります。こちらにつきましては、SP-01、02、03の運転資金のバックアップとして使用する可能性がございます。
2019年12月期 連結業績予想(国際会計基準IFRS)

次に、2019年12月期の連結業績予想について、ご報告申し上げます。こちらも同じく、国際会計基準IFRS会計でございますが、売上収益に関しましては5億~17億円と予想しております。また、売上原価は2億~3億円と予想しております。
この売上収益の内容でございますけれども、SP-01の中国での製品販売による収益や、SP-03の日本および中国での製品販売による収益、さらに権利の導出による収益……具体的には、SP-02、04などの権利の導出に際しての一時金としての収益をここで計上しております。
また研究開発費は、15億円と予想しております。この内容といたしましては、SP-02で、今は末梢性T細胞リンパ腫を中心に臨床試験を実施しておりますけれども、このアジア第Ⅱ相臨床試験の費用に充当ということです。
この試験は、年内の終了を予定しております。また同じくSP-02については、将来の適応拡大の中の開発費用として、一部を使用することを想定しております。SP-04に関しましては、第Ⅲ相国際共同臨床試験の費用に充当することを考えており、この試験も最終試験になります。
一方、販売費、一般管理費ですが、18億~19億円を想定しております。この内容といたしましては、SP-01、03の中国での自販およびマーケティング活動費でありまして、これには市販後の調査も含んでおります。
また、中国のセールスマーケティングを含む体制の運営費にも充当する予定であります。さらにこの中には、SP-01、03の無形資産の償却比が4億5,000万円ほど入っているということを注記しておきたいと思います。
営業損益ですけれども、予想としては20億~30億円の赤字になると想定しておりますけれども、いわゆる研究開発費を除いた営業損益に関しましては、およそマイナス5億円~マイナス15億円を想定している次第であります。
製品/開発パイプライン(2019年2月13日現在)
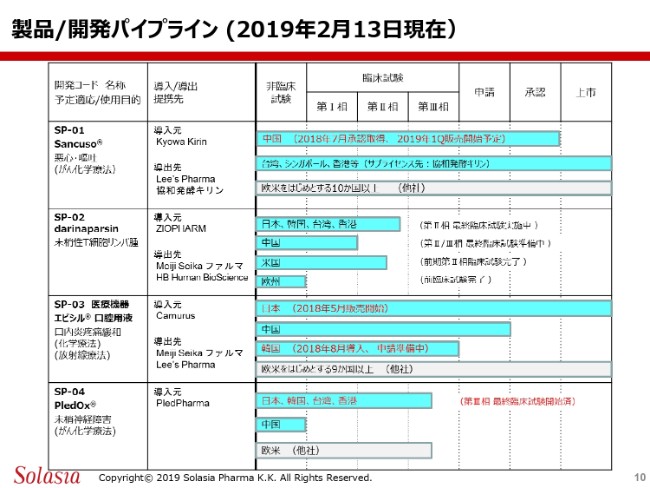
引き続きまして、製品・開発パイプラインの状況についてご報告申し上げます。こちらのガントチャートでございますけれども、2019年2月13日現在のステータスを示したものであります。この中で、2018年12月期に進行した内容は、赤字で示したております。
1つ目です。中国でのSP-01は、2018年7月に承認を取得して、今年度の第1四半期に発売を開始する予定であります。従って、この承認まで(スライドの)バーが伸びたということになります。
SP-02に関しましては、バーそのものは変わっておりませんけれども、引き続き症例の登録を継続している状況です。SP-03については、日本において2018年5月に販売を開始したということで、このバーは最後の上市のところまで伸びました。このあたりが、新しい状況であります。
また、昨年8月には韓国における権利を導入しており、現在その申請の準備中でございます。
第4号製品については、昨年12月にご報告させていただきましたように、臨床試験を開始したというのが新しいステータスになります。
SP-01 開発事業化:経皮吸収型制吐剤「Sancuso® (善可舒®)」

ではここから、もう少し細かくご報告したいと思います。SP-01でございますけれども、これまでみなさんにご報告しているように、効能・効果としては、がん化学療法による悪心・嘔吐で、世界で唯一の経皮吸収剤という特徴を持っております。
中国版のNCCNガイドラインにも標準治療の1つとして、すでに記載されているものです。ご報告しましたように、2018年7月に当局による承認を取得したあとで、市販用の製剤の輸入の許可も取得しております。
そして、今年度の第1四半期には発売を開始する予定であります。現在は、北京市、上海市、広州市がソレイジアのテリトリーですが、この3地域において、自社での販売開始の準備をしています。
またその他の地域については、Lee’s Pharma社が同じく販売の準備中ということになっております。
SP-02 開発事業化:新規化学療法剤「ダリナパルシン」

SP-02ですが、こちらも新規の化学療法剤「ダリナパルシン」というものがありまして、予定の適応症は、再発・難治性の末梢性T細胞リンパ腫であります。すでに第Ⅱ相臨床試験を日本各地で終了した後で、現在は日本、韓国、台湾、香港の4ヶ国で最終の第Ⅱ相臨床試験を実施中であります。
こちらの試験は、2019年内に終了を予定しているところであります。対象患者は、この末梢性T細胞リンパ腫の患者さんで、計画上は65名の評価症例数を集積する予定であります。
目的としては、末梢性T細胞リンパ腫に対するSP-02の有効性および安全性を検討するというところです。こちらの試験で我々の想定する効果が得られれば、その後に承認申請を行うということで、直前の最終試験として位置づけられているものであります。
SP-03 開発事業化:医療機器「エピシル® 口腔用液」

SP-03ですが、こちらはご存知のように医療機器であります。化学療法や放射線療法をともなう、口内炎で生じる口腔内疼痛の管理および緩和を行うための物理的作用を持っている医療機器であります。
日本においては、2018年4月に保険収載されました。ボトル1本あたりが7,520円という価格であります。その後、2018年5月にMeiji Seikaファルマ社から発売が開始されています。中国については、2019年中の承認取得を想定し、その後も2019年中の販売開始を想定しているものであります。
また、新しく韓国のテリトリーについて昨年8月に権利を導入し、現在はその承認申請の準備をしているところであります。
SP-04 開発事業化:細胞内スーパーオキシド除去剤「PledOx®」①

SP-04ですが、こちらは細胞内のスーパーオキシド除去剤でございます。予定の適応症、また将来の効能・効果は、がん化学療法にともなう末梢神経障害であります。
現在、がん化学療法にともなう末梢神経障害を効能・効果とする薬剤は、日本および世界の中でも、まだ承認されていない状況であります。
一昨年11月から昨年2月にかけて、導入元でありますPledPharma社が第Ⅰ相試験を実施して完了しております。そこでの安全性とそれから忍容性、そして薬物動態が確認されたのちに、日本、韓国、台湾、香港において、昨年12月から第Ⅲ相の国際共同臨床試験……これも承認前の最終試験になりますけれども、開始したところであります。
SP-04 開発事業化:細胞内スーパーオキシド除去剤「PledOx®」②

このスライドは、SP-04の第Ⅲ相臨床試験の要約でございます。試験のデザインとしては、第Ⅲ相、国際多施設共同、二重盲検、プラセボ対称試験ということで、いわゆる第Ⅲ相試験の標準的なものになると思いますけれども、こちらのデザインで実施されています。
このSP-04の目的は、がん化学療法誘発性の末梢神経障害の発現抑制効果、および安全性について、プラセボと比較するというものであります。
試験自体は2つで構成されておりまして、1つが「POLAR-M試験」、もう1つが「POLAR-A試験」と名付けております。
「POLAR-M試験」は、mFOLFOX6療法という、いわゆる大腸がんに対しての標準療法を行ったときに出てくる、末梢神経障害の発現抑制に対する効果と安全性を見ることです。
「POLAR-A試験」は、いわゆる手術した後の化学療法として、今度はmFOLFOX療法を行う大腸がんの患者さんに対して、SP-04の効果、発現性、安全性をプラセボと比較するというものです。
対象となる患者さんは、大腸がんの患者さんですけれども、mFOLFOX6の使い方が若干違うということで、この2つのデザインの試験を実施しております。
主要評価項目については、たくさんありますけれども、スライドに書いてあるような評価項目があります。目標の症例数は「POLAR-M試験」が420例で、アジア・欧州・米国を含みます。
「POLAR-A試験」は280例で、アジアと欧州のみになります。これら420例のうち、当社の領域でありますアジアからは120例。「POLAR-A試験」については、280例のうち、当社の領域からは80例を登録する目的で実施しております。
新着ログ
「医薬品」のログ





