第131回 個人投資家向けIRセミナー 第5部
ジェイファーマ、創薬ベンチャー初となる日本発自社創製化合物のグローバル承認を目指し、治験フェーズ3まで進捗
はじめに
𠮷武益広氏(以下、𠮷武):ジェイファーマ代表取締役社長の𠮷武です。本日は、当社の概要と事業についてご紹介します。
私たちの体は、約37兆個の細胞から構成されているといわれています。外部からの侵害を防ぐために、細胞はスライドのような細胞膜という層に覆われていますが、一方で、この層を通じて栄養を取り込まなければ細胞が生き延びることができません。
生体には約400種類の「SLCトランスポーター」が存在するといわれており、私どもはこのSLCトランスポーターに対する新しい医薬品を開発しています。
これにより、アンメット・メディカル・ニーズに応え、ニッチではありますが医療の要望に特化し、患者のみなさまの困難を解消することを目指しています。
この新薬をグローバルに展開し、1日でも早く世界の人々の健康に貢献するため、革新的で模倣ではない新薬を届けるために日々努力しています。
L型アミノ酸トランスポーター1(LAT1)と、当社開発品ナンブランラト
𠮷武:私どもが最初に取り上げたトランスポーターが「L型アミノ酸トランスポーター1(LAT1)」です。
細胞ががん化するとLAT1が細胞表面に現れます。LAT1はイソギンチャクのように動きながら、活発に細胞外からアミノ酸を細胞内に取り込み、がんの増殖を促進する非常にユニークな栄養の入口となるトランスポーターです。
動画をご用意していますのでご覧ください。
(動画流れる)
LAT1阻害剤:開発パイプライン:2026年3月現在

𠮷武:私どものLAT1阻害剤についてご説明します。動画でもご覧いただいたように、LAT1には、細胞ががん化すると増加し、がんの成長を促進する特徴があります。
当社では、2つの薬剤「ナンブランラト」と「JPH034」を臨床ステージとして開発中です。これらの薬剤は、アメリカの政府機関であるFDA(米国食品医薬品局:United States Food and Drug Administration)の審査・レビューを受け、現在はアメリカで臨床試験が進められています。
特に「ナンブランラト」は、この試験を終えれば全世界の患者さまに届けられる可能性が見えてくる、フェーズ3と呼ばれる段階に進んでいます。
LAT1に関して私どもがこれほど多くの研究を行うことができた理由について説明します。
まず、創業者である遠藤が1998年にLAT1を発見したことがあります。当時の特許法は現在と異なっており、遺伝子特許では、あるタンパク質を発見し、さらにそれを読み込んでいる遺伝子を見つけると、その周辺を網羅的に特許として押さえることが可能でした。そのため、私どもは独占的に研究開発を進めることができ、その期間は20年間にも及びました。
また、遠藤は非常に優れた研究者であり、自分でその領域を押さえながらも、できる限りオープンイノベーションを進めようと、LAT1に関するさまざまな研究材料や資料を世界中の研究者に提供しました。
その結果、多くの研究者が積極的に研究を進め、約25年以上の間でLAT1の特性や治療への活用方法が次第に明らかになってきました。
医薬品のグローバル開発、承認に至る確率と、必要とされる開発費
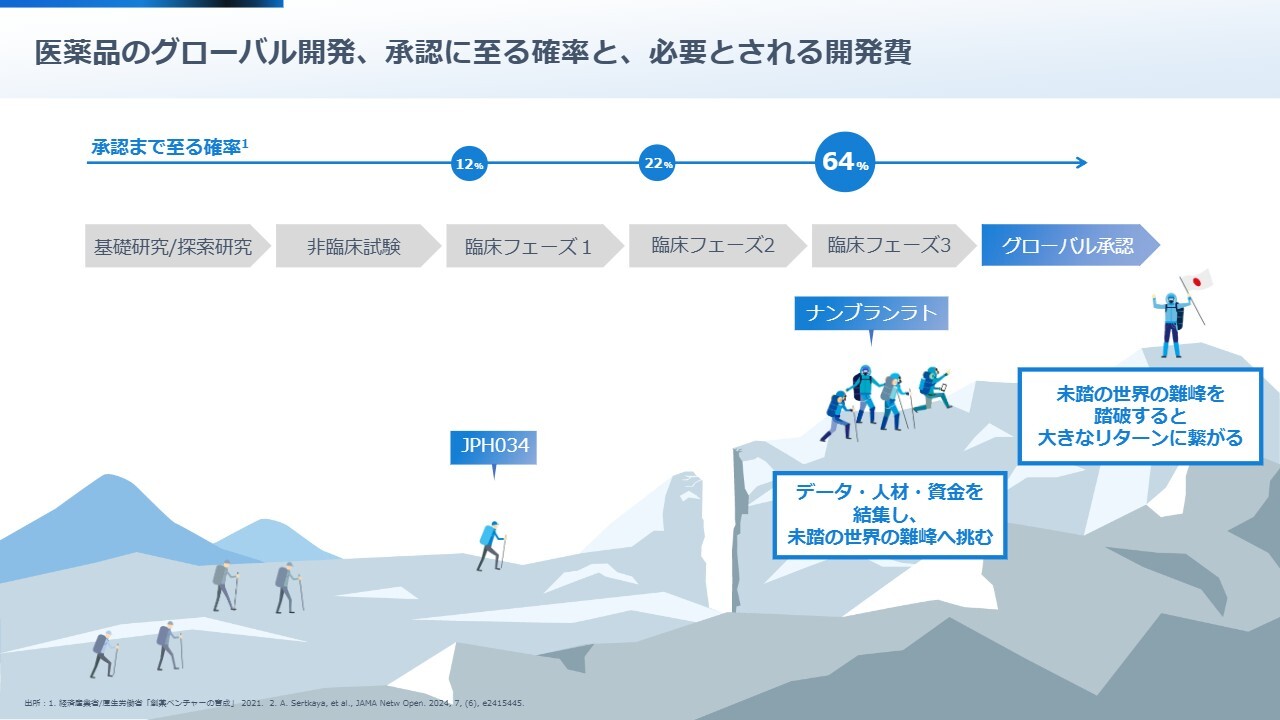
𠮷武:「医薬品の開発って、難しくてよくわからない」と言われます。そこで私は、よく山登りに例えてお話ししています。
まず、基礎研究として遠藤がLAT1を発見し、それを最適な標的として定めました。続いて、それに基づき「薬の卵」を開発します。次に動物に長期間投与して、本当に安全であるかを確認します。
このプロセスはスライドに示している「基礎研究」「探索研究」「非臨床研究」に該当します。この一連の流れは、山登りのために兵站部隊を整え、ザイルや食料、シェルパなど、さまざまな準備を整える段階だと考えていただければと思います。
準備を終えると、どの山に登るのかを決める段階に入ります。例えば、高尾山に登る場合でも一定の準備が必要ですし、富士山に登るには十分な準備を整えなければなりません。準備不足で登り始めてしまえばトラブルが生じることは明らかですので、しっかりとした準備が重要なのです。
エベレストやK2といった世界の頂を目指すような挑戦として、私どもは新しく優れた薬を世界中の人々に届けることを目指しています。必要な兵站を整え、臨床フェーズにおける最初の段階である「臨床フェーズ1」に進んでいきます。
私どもはフェーズ1で、5種類の異なるがん患者さまにご協力いただきました。その中で、今日お話しする胆道がんにおいて、本当にキラリと光るダイヤモンドの原石のようなものを1つ見つけることになりましたので、遠藤には非常に運があったと思います。
その原石を私自身も確認し、約7年半前に当社に入社しました。そして、その原石が本当に確かなものなのかを確かめるべく、次の「臨床フェーズ2」に進んだのです。
フェーズ2では日本の先生方や100人以上の日本人患者さまにご協力いただく中で、この原石が真に光り輝くものであり、人体に投与しても非常に安全だという可能性を示す糸口を見つけました。
医薬品の開発は、上位フェーズに進むほど成功確率が高まります。フェーズ1では成功確率が約12パーセント、フェーズ2では約22パーセントに上昇し、フェーズ3まで進むと約64パーセントとなります。すなわち、フェーズ2において、約40パーセントの薬剤が脱落していきます。
フェーズ2は「死の谷」のようなものだと言われています。私どもは、その途中でコロナ禍にも直面し、大変な苦労を味わいながら4年間奮闘した末に、この「死の谷」を乗り越えました。
現在は頂上を目指す「臨床フェーズ3」へと進んでいます。フェーズ3を山登りに例えるなら、7合目付近まで到達していることになりますが、私どもが7合目に到達したと確信を得たのが昨年12月でした。
それを機に私どもはグロース市場に上場し、必要な資材や資金を集めました。さらに、海外の多くの方々にも協力を依頼し、現在最後の山に挑んでいます。
医薬品に関しては、日米欧でほぼ同じレギュレーションとなっています。30年かけて進められたハーモナイゼーションの成果として、各国ごとに試験をやり直す必要がなくなっています。1つの試験が認められれば、それをもとに日本、アメリカ、ヨーロッパで承認を得ることが可能なシステムが整っています。
私どももそのシステムを活用しながらグローバルフェーズ3を進めており、承認を得られれば、日米欧における販売が可能となります。グローバルに承認されれば、1,000億円以上の売上と高い利益率が期待されますので、この最後の山登りに全力を注いでいます。
ナンブランラトの開発状況と、累積調達金額・累積赤字(投資)金額
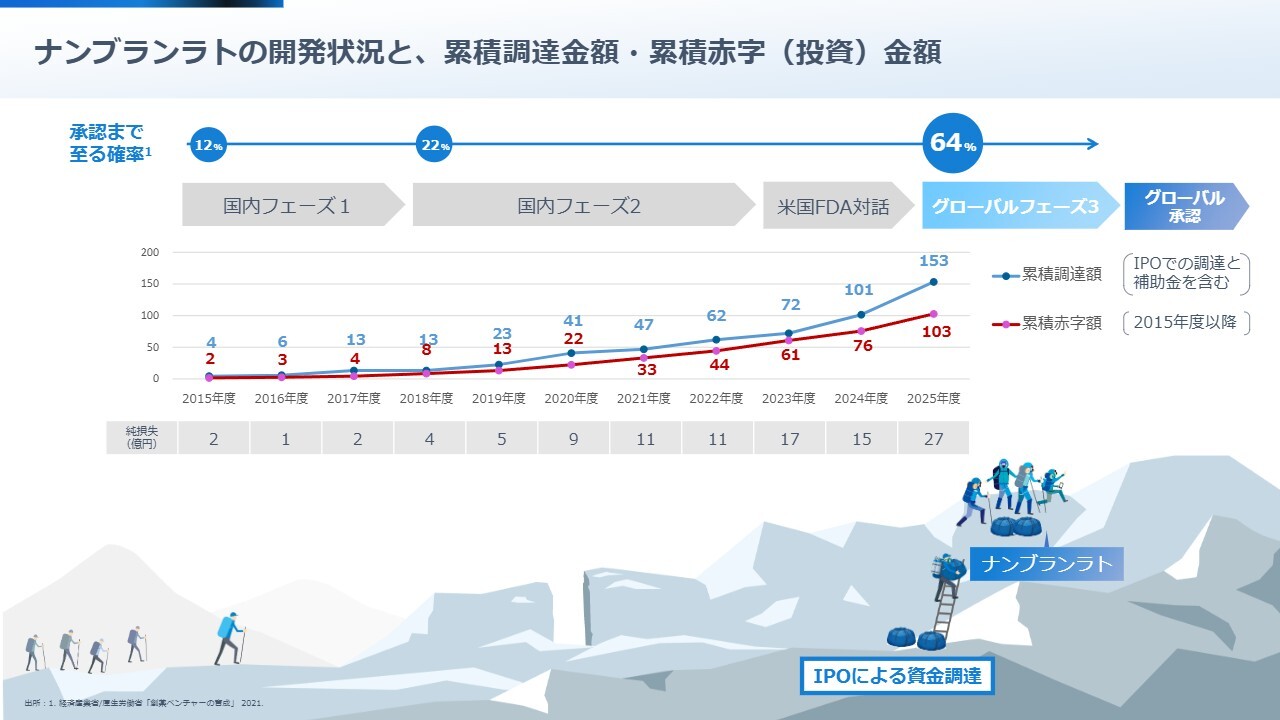
𠮷武:私どもは、何も蓄えがなくこの山を登り始めたわけではありません。フェーズ1の13億円は、遠藤が一人で投資家のもとを回って資金を集めました。
フェーズ2からは私も参加し、生まれて初めて資金調達を行いました。私どもの国内パートナーである大原薬品工業の社長にご理解いただいたことや、アメリカやヨーロッパの投資家のみなさまから「このプロジェクトは価値がある、おもしろい」とご支援いただくことで、フェーズ2を乗り越えることができました。
そこまでは順調でしたが、日本国内だけでフェーズ1とフェーズ2を実施した結果、アメリカのFDAから「これは日本のためにやっている臨床試験ですよね? アメリカの国民のためになるよう、ちゃんと考えてください」と指摘を受けました。
つまり、アメリカの患者さまにとって適切であり、アメリカの患者さまが飲んでも安全で効果がある手法を検討するように言われたのです。
この課題を解決するのに2年以上を要しましたが、最終的にはFDAにも納得していただける臨床試験計画を作り上げました。さらにIPOによる資金調達も無事完了し、現在はその最終段階に到達しています。
私どもはこれまで累積でこの薬剤に100億円近い投資を行っています。さらなる資金は必要ですが、この大規模な投資が将来大きなリターンとして戻ってくると信じて進めています。
関本圭吾氏(以下、関本):先ほどの動画の中で、LAT1は御社の創業者である遠藤さまが発見されたと説明されていました。
グローバルで見た場合に、LAT1を研究している他企業は存在するのでしょうか? また、それらの企業よりも御社が進んでいるのか、遅れているのかなど、競合比で見た状況について教えていただけますか?
𠮷武:2019年まで遠藤が特許を保有していたことにより、2019年まで他社は商業的な開発を行うことができませんでした。
現在、LAT1を医薬品で直接阻害して治療に結びつけようとして、臨床開発を進めているのは、全世界で私どものみです。グローバルのベンチャー企業で動物実験などに取り組んでいる例はありますが、臨床試験のステージまで進んでいるのは当社のみです。
このLAT1が非常にがんに多く発現していることは周知の事実です。例えば、LAT1がアミノ酸を取り込む性質を利用し、アミノ酸にホウ素を付加してがん細胞内に運び込み、その後、中性子を照射してがん細胞内で核分裂を誘発する治療方法は、日本でもすでに開始されています。このホウ素の投与の入口としてLAT1が利用されています。
また、別の放射性物質や細胞を殺す物質を付加し、LAT1を介することでより選択的にがんを攻撃するトライアルは他社でも行われています。しかし、LAT1そのものに直接作用し、これを医薬品として治療につなげようとしているのは、私どもが最も先行していると考えています。
太陽のように患者に寄り添う抗がん剤の開発

𠮷武:フェーズ2のデータから見えてきたこととして、LAT1阻害剤「ナンブランラト」は、「太陽のように患者さまに寄り添う抗がん剤」になり得るのではないかと考えています。
日本では、死亡する方の3分の1ががんで亡くなっています。しかし、昔と比べて圧倒的に治療の選択肢が増えてきたことから、がんを完全に叩こうとして自身の体を弱らせるのではなく、共存しながらともに長く生きていくことも1つの戦略となる時代になっています。
みなさまも、抗がん剤や化学療法という言葉を耳にしたことがあると思います。例えば、化学療法には、特につらい副作用として、髪の毛が抜けてしまう、せっかくきれいにしたネイルがボロボロになってしまう、あるいは手足の感覚がしびれてしまうといったものがあります。その結果、自分の生活がどうしても犠牲になってしまいます。
がんを叩くために自分の体も蝕まれていくことが化学療法であり、イソップの童話に例えるなら「北風のように副作用の強い抗がん剤」ではないかと考えています。
一方で、フェーズ2で100名以上の患者さまに「ナンブランラト」を投与した結果、従来の化学療法に比べ、副作用が非常に少ないことが確認されています。
「ほとんどない」と言ってしまうと語弊があるかもしれませんが、副作用に関しては、我慢できるぐらいの範囲に収まるのではないかと思います。私自身が投与を受けたわけではないので確かなことは言えませんが、データを見る限りではそのように言えると考えています。
また、FDAの指摘にもあったように「どのようにすれば、この薬がより患者さまに貢献できるのか?」とさまざまな解析を進めていきました。その中で、この薬を長期的に服用することで、より長く生きられる可能性があることが見えてきました。
実際に胆道がん患者さまの90パーセント以上が65歳以上であり、強い抗がん剤治療には耐えきれない状況にあるのが現状です。例えば、完治には6回の服用が必要な薬剤であっても、4回で投与が終わってしまい、効果が不十分なためにより悪化してしまうことがあります。
しかし、私どもの薬剤は副作用のプロファイルがあまり悪くなく、適切に反応すれば、長期間服用を続けることが可能です。その結果、この薬剤を服用した方々は非常に長生きできる可能性があることがわかっています。
「太陽のように副作用が少なく患者さまに寄り添う」という新しいコンセプトを持つ抗がん剤を、グローバルのフェーズ3において立証していきたいと考えています。
胆道がん - 患者数は少ないが、極めてアンメットニーズが高いがん種
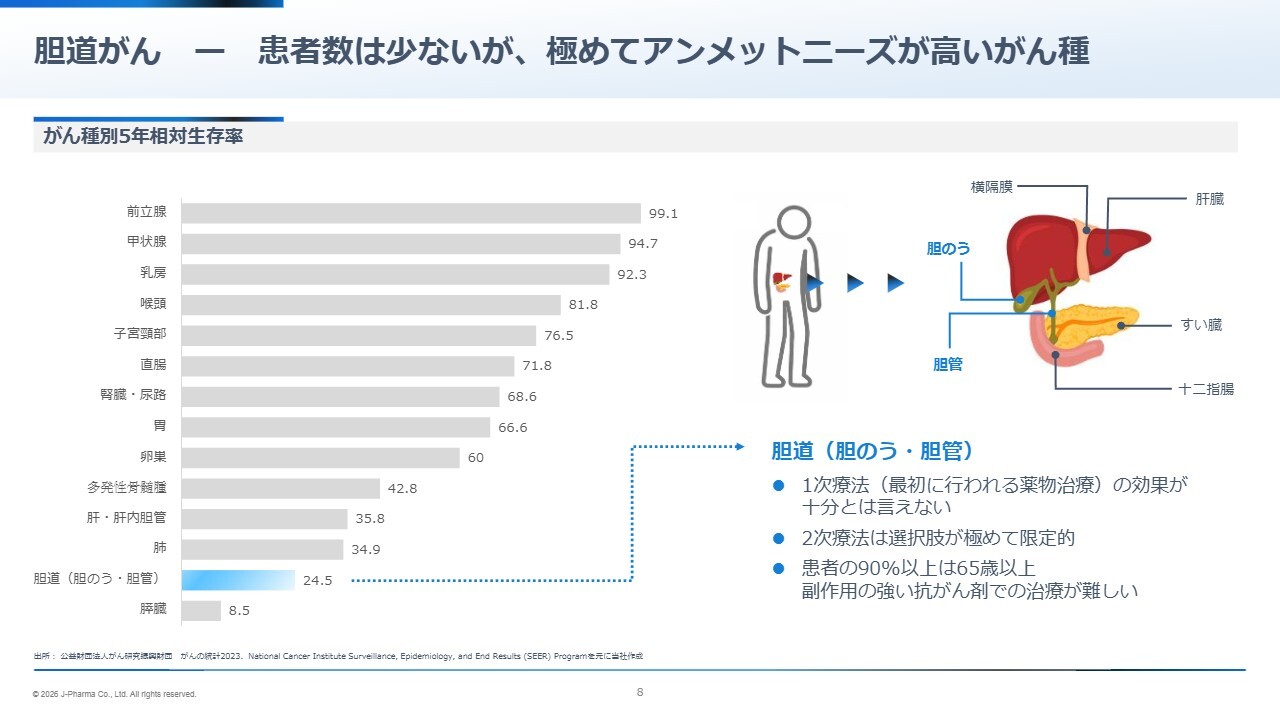
𠮷武:胆道がんについて少しご説明します。スライド右側にあるイラストでは、赤茶色の部分が肝臓、緑色の部分が胆管です。
肝臓で作られる非常に酸性度の高い胆汁を、胆のうで濃縮し、十二指腸に吐き出します。この過程で膵臓から分泌される膵液と合流し、胆汁と膵液が協力して摂取した食べ物の消化を助けるという、重要な役割を果たしています。
スライド左側のグラフには、がんの発生部位ごとの5年生存率を示しています。「5年生存率」とは、がんが見つかった後、5年間生存できる確率です。これは、現在のがん治療の成否を測る重要な指標の1つとなっています。
例えば、男性に多い前立腺がんや女性に多い乳がんでは、診断技術と治療法が進歩した結果、90パーセント以上の患者が5年以上生存できる時代になっています。
一方、グラフの下方にある胆道がんと膵臓がんでは予後が悪く、5年生存率が1桁パーセント台や20パーセント台にとどまっています。
この理由の1つに、胆管や膵管といった細い管にがんが発生することがあります。これらの管は非常に細く、基底膜などによる支えが弱いため、がんができると早い段階で外に突き抜けてしまう性質があります。その結果、転移もしやすくなります。
例えば、肺や肝臓のような臓器であれば、がんが進行しにくい構造になっていますが、管の場合にはそのような守りがないため、進行が早いのです。
さらに、これらのがんは「サイレントキラー」とも呼ばれるように、症状がほとんど現れません。そのため、ある日突然、激しい腹痛や、目が黄色くなるなどの症状が現れます。
そこで精密検査を受けて初めてがんが見つかることが多く、発見された時にはすでにステージⅢBやステージⅣまで達しており、余命が1年を切るとされる非常に重篤な病気です。
私どもは、極めてアンメットニーズが高い胆道がんの治療において、状況を改善していきたいと考えています。
欧米における、胆道がん治療の現状と課題
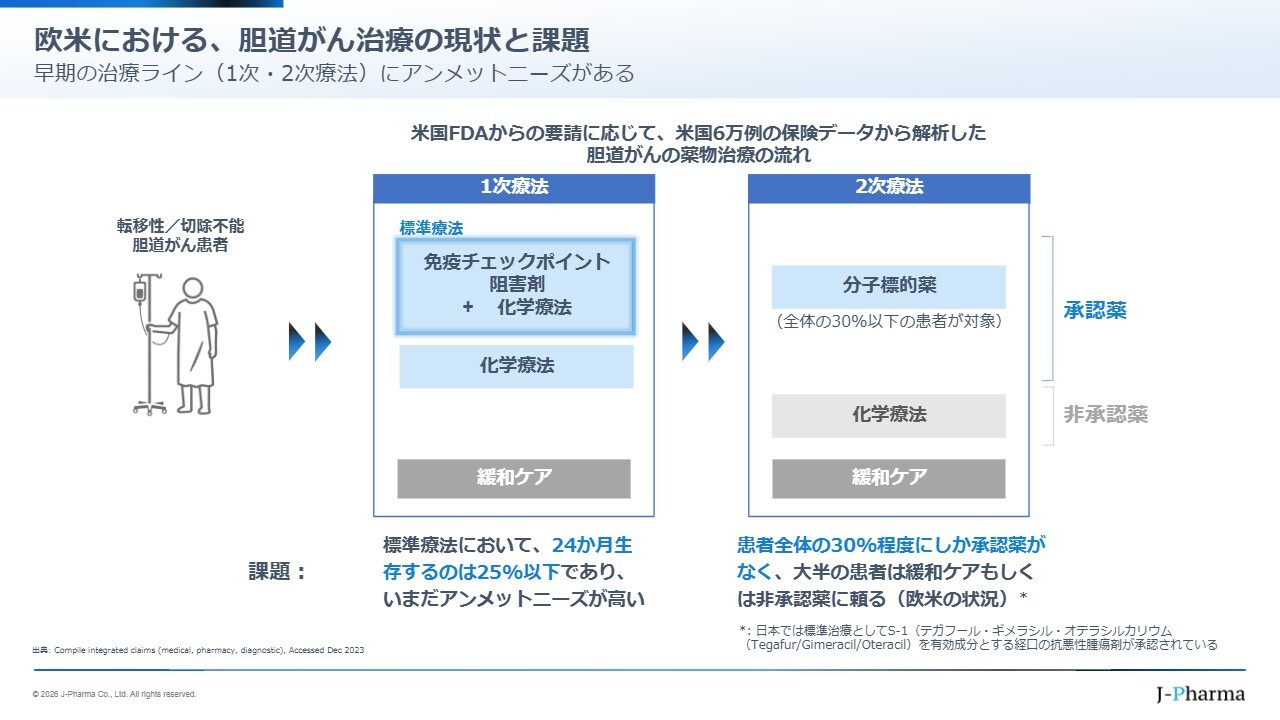
𠮷武:実際の胆道がん治療でどのように使用されるのかについてご説明します。まず手術が考えられますが、手術ができない場合や再発した場合に、最初に受ける治療が「1次療法」と呼ばれるものです。
京都大学の本庶佑先生が開発した免疫チェックポイント阻害剤(ICI)による治療は、現在では世界中でがん治療の基盤的な治療法となっています。
胆道がん治療では、免疫チェックポイント阻害剤と化学療法を組み合わせた治療法や、化学療法を用いた治療法が「1次療法」として実施されます。
ただし、先ほども述べたように、他のがんに比べて生存率が低いことが課題です。2年間治療を行っても、4人に1人しか生存していない状況だといわれています。この状況をさらに改善する努力が必要であり、私どももその取り組みを推進したいと考えています。
1次療法の効果がなくなった場合、もしくは患者が治療に耐えられなくなった場合には「2次療法」に移ります。
現在ではがんの遺伝子解析が非常に進歩しており、どのがんにどのような遺伝子変異が関係しているのかが解析されてきています。胆道がんでは3つの遺伝子に変異があり、それらに対して非常に選択的に働く分子標的薬が開発されています。
同様の薬剤はこの5年ほどで次々と登場してきていますが、これらの画期的な分子標的薬は、患者全体の約30パーセントしかカバーできません。残りの約70パーセントの患者さまは、特に欧米においては2次療法となり得る承認薬が存在せず、非常に副作用が多い化学療法を受けるか、治療自体を諦めざるを得ない状況にあります。
胆道がん治療においてアンメット・メディカル・ニーズが最も高いのは、2次療法で使用できる薬剤が存在しない、約70パーセントの患者さまだと考えています。私どもは、そのような患者さまに福音を届けるべく、現在グローバルフェーズ3試験を展開しています。
2026年3月時点で東証グロースに上場している創薬ベンチャーのうち、日本で自ら創製した化合物のデータを積み重ねてグローバルフェーズ3まで進めている唯一の事例(当社調べ)

𠮷武:フェーズ1では遠藤が胆道がんでのキラリと光る原石を見つけ、そしてフェーズ2では100名以上の患者さまを対象に、日本国内で行われた同種の試験としてはかなり大規模な試験で効果を実証しました。さらに、プラセボ(偽薬)と同程度の安全性であると評価も受け、国際的にも認められる結果となりました。
がん領域で最も権威ある学会の1つであるASCO(米国臨床腫瘍学会:American Society of Clinical Oncology)では、年に2回の口頭発表を行いました。口頭発表には上位2パーセントから3パーセントの演題しか選ばれず、非常に狭き門となっています。さらにアメリカの『Clinical Cancer Research』にも掲載いただいています。
また、先ほどもお話しした2年間にわたるFDAとの討議についても、ESMO(ヨーロッパ臨床腫瘍学会:European Society For Medical Oncology)でポスター発表を行いました。
現在進めているフェーズ3は、何百人もの規模での臨床試験を実施しており、アメリカのスタッフも100人を超えて活動しています。
誰もが覚えやすいよう、プロジェクトには「Beacon-BTC」というニックネームを付けています。
「BTC」は「Biliary Tract Cancer」の略で、胆道がんを指します。「ともしび」「灯台」を意味する「Beacon」と組み合わせ、「胆道がんへのともしびをあてましょう」というキャッチフレーズのもとで臨床試験を進めています。
副作用が少なく、太陽のように患者さまに寄り添う抗がん剤として、安全で長く治療でき、最終的には延命にもつながる可能性を立証する試験です。
関本:プロジェクトのスケジュールについてうかがいます。自力でグローバルフェーズ3まで進められていますが、これは非常に珍しいことだと思います。そのような決断に至った背景や理由は何かあるのでしょうか?
𠮷武:さまざまな要因が重なっていますが、1つには、私が前職で大手製薬会社に勤務していた頃の経験があります。
欧米企業へ自社の化合物を導出(ライセンスアウト)したのですが、この経験はあまり喜ばしいものではなく、当初は非常に苦く辛い思いをしました。
最初に導出した2つの薬は日本でも承認されたものの、アメリカやヨーロッパでは日の目を見ず、棚上げされてしまいました。また、3つ目の薬は日本でもヨーロッパでも承認されましたが、ライセンス先が突然市場から取り下げてしまいました。
そのような経験が背景にあり、前職の経営陣は「最終的に薬をグローバルに広げていくのは大きな製薬会社でなければできないが、薬そのものは自分たちである程度まで育て上げるんだ」という方針を採用しました。
いわば赤ちゃんのような新薬が独り立ちしていくためには、自分たちの手で育て上げるほうがよいという結論に至ったのです。新薬の独り立ちは将来的に患者さまにとっての福音にもなります。ビジネスとしての成功にもつながる道筋が明確に示される段階まで、自分たちで育て上げるべきだという考えです。
また、人のまねをしない独自性のある取り組みには、既存の教科書がありません。私たちが現在掲げている新しいコンセプトも、模倣できる教科書がなくすべてが試行錯誤の連続です。
仮に導出した場合、そのような面倒なことに取り組んでくれる会社はほぼ存在しません。多くの企業は教科書どおりに進めてしまい、迅速にお金に結びつけることを優先します。
新しいものを育てていくためには、自ら汗をかき、それが役立つものであることを立証してからライセンスアウトすることが重要です。
私どももフェーズ3をすべて行おうとは考えていません。フェーズ3の前半部分をしっかり自分たちでこなし、日本で100人、アメリカで120人に投与し、「同じような結果が出ましたね」と言える段階までは自分たちで確実に実施します。
その後、ヨーロッパやアジアなどの複数の地域に広げる段階では、私ども1社では対応できませんので、協力していただける企業を探していきたいと考えています。
関本:過去の経験に基づいてここまで進められてきたのですね。
免疫チェックポイント阻害剤(ICI)との併用療法への展開
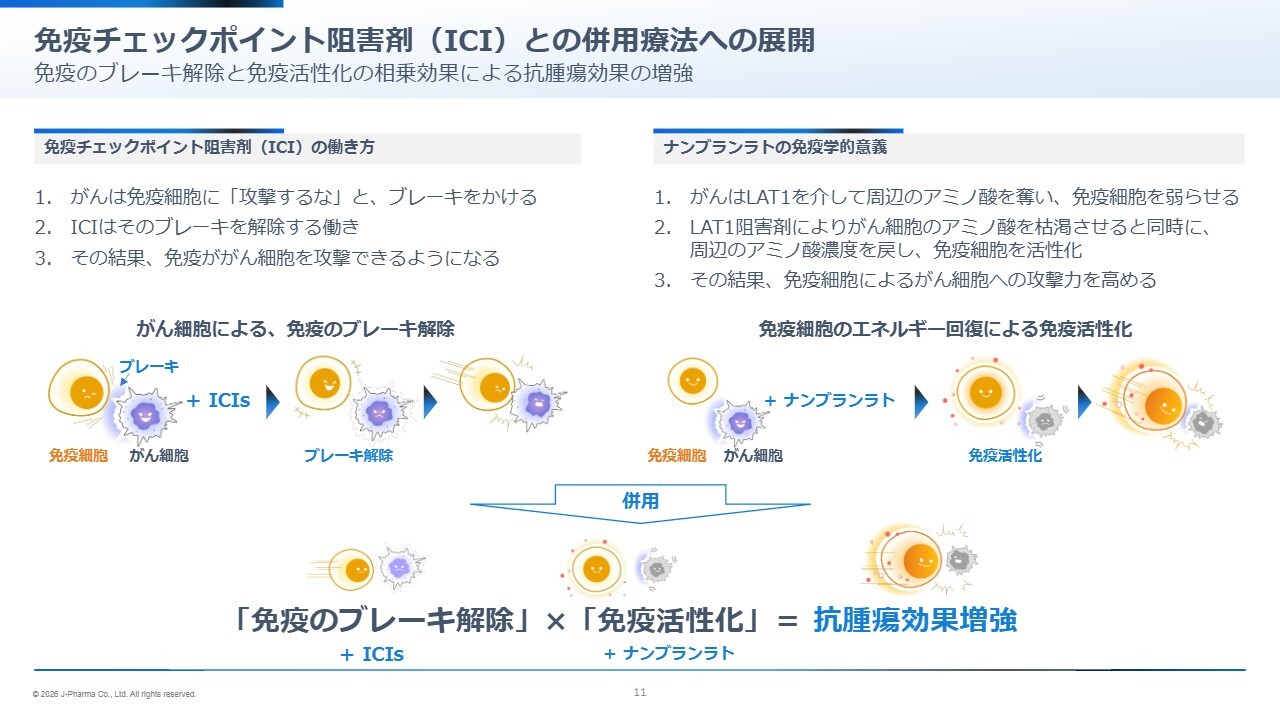
𠮷武:先ほど、1次療法において免疫チェックポイント阻害剤(ICI)が使用され始めているとお話ししました。この治療法はノーベル賞の対象にもなっており、非常に画期的です。
スライド左側に示されているように、がんは異物であるため、本来は体の免疫が攻撃するはずです。しかし、がんはその攻撃を回避するためのブレーキを持っています。免疫チェックポイント阻害剤は、そのブレーキを解除することで作用します。
この治療法により、これまでまったく治療ができなかったがんに対して、まるで奇跡のような効果が得られるとされています。ただし、この奇跡も永続的ではなく、ブレーキを外して「攻撃せよ」と指示しても、免疫細胞は徐々に疲弊していきます。
私どもの研究により解明されたのは、がん細胞の増殖と免疫細胞の活性化にはいずれもアミノ酸が必要であることです。しかし、そのアミノ酸がすべてがん細胞に取り込まれてしまうと、免疫細胞に必要なアミノ酸が不足します。
そこで、がん細胞によるアミノ酸の取り込みを抑えることで、そのアミノ酸が免疫細胞に届き、免疫細胞をより強化します。この結果、ブレーキを外した後の加速がさらに強まり、抗腫瘍効果が向上するのではないかという仮説を立てています。この仮説は、動物実験ですでに立証されています。
この研究については今年4月に、すでにPMDAに治験届を提出しています。5月からは、日本国内における胆道がん患者を対象に、この仮説が実証できるかを日本の4つの主要ながんセンターで検証を開始予定です。この取り組みは私どもにとって次なる大きなチャレンジの1つとなっています。
胆道がんにおける事業計画

𠮷武:私どもは今回、IPOにより資金調達を実現しました。「ナンブランラト」のグローバルフェーズ3試験、および免疫チェックポイント阻害剤の併用について、自分たちで見通しが立つところまで進めていこうと考えています。
その上で見通しが立った際には、大手または中堅規模でも、ヨーロッパやアメリカで積極的に取り組んでくれる会社にライセンスアウトしたいと考えています。
ここまで育て上げることで導出後に返還されるリスクが減少し、価値が明確になるため、大型契約の交渉も可能になると考えています。
最終的には長期的に承認を取得し、販売に至ることを目指しています。この新しい抗がん剤は新しい作用機序を持つ抗がん剤であり、日米欧での承認を得られれば、ブロックバスターとして年間売上が1,300億円から1,500億円以上に達する商品になり得るといわれています。
医薬品は非常に利益率が高く、特許によって独占権が維持されるため、長期的には研究開発費をすべて回収し、投資家のみなさまに対し、なんらかのかたちで貢献できるよう努めていきたいと考えています。
世界トップレベルの研究者から、研究成果をグローバルに送り出す医薬品開発専門家にバトンタッチ

𠮷武:私どもがなぜうまくいったのかを振り返ると、やはり遠藤仁という世界に通用する研究者が大きな役割を果たしたと思います。
日本の基礎研究は本当にすばらしく、ノーベル化学賞やノーベル生理学賞など、さまざまな先生方が受賞されてきました。このことからも、日本の医学分野におけるサイエンスは世界トップクラスであることがわかります。
しかしながら、その成果がトランスレーショナルリサーチとして医薬品に橋渡しされていない現状があります。私どもはそれを1つ成功させたと考えています。
遠藤という世界的レベルの科学者が、NEDOやAMEDなどの日本の公的資金によってキラリと光るダイヤモンドの原石を見つけ出しました。その後、私がそのプロジェクトに参画し、医薬品のグローバル開発に携わるさまざまな専門家を集め、ダイヤモンドとなり得ることを確認しました。
当社のグローバル開発を支える世界最先端の大学・研究機関の医師・科学者
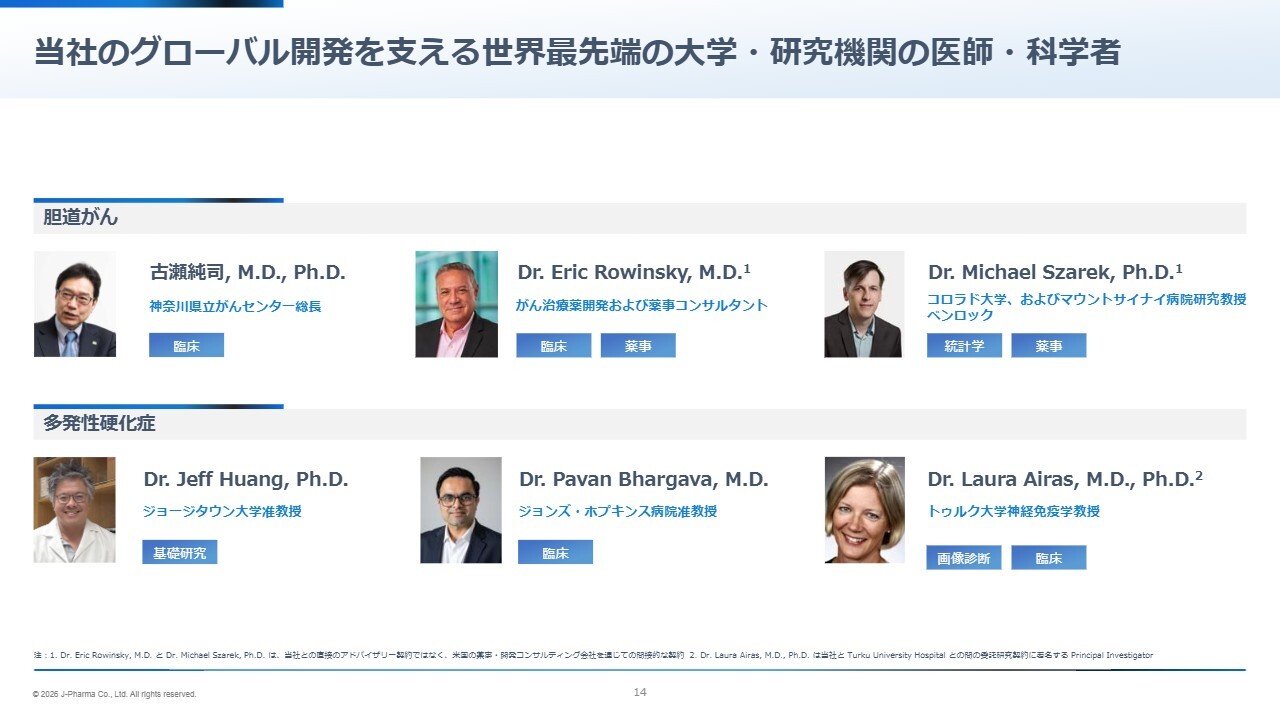
𠮷武:新しい取り組みを進めていく中では、世界最先端の方々が興味を持ち、一緒に働いてくれています。
例えば、日本では神奈川県立がんセンターの古瀬総長がこの領域でトップの先生の一人です。アメリカではEric Rowinsky先生は、これまでに5つ以上の抗がん剤を開発された実績をお持ちです。
また、コロラド大学やマウントサイナイ病院のMichael Szarek先生は、FDAとの長期にわたる交渉が可能な生物統計学の専門家です。そのような方々の支援を受けて、私どもはここまで進んでくることができました。
今後のビジネス展開 - ニッチでアンメットニーズが高い疾患領域を狙う
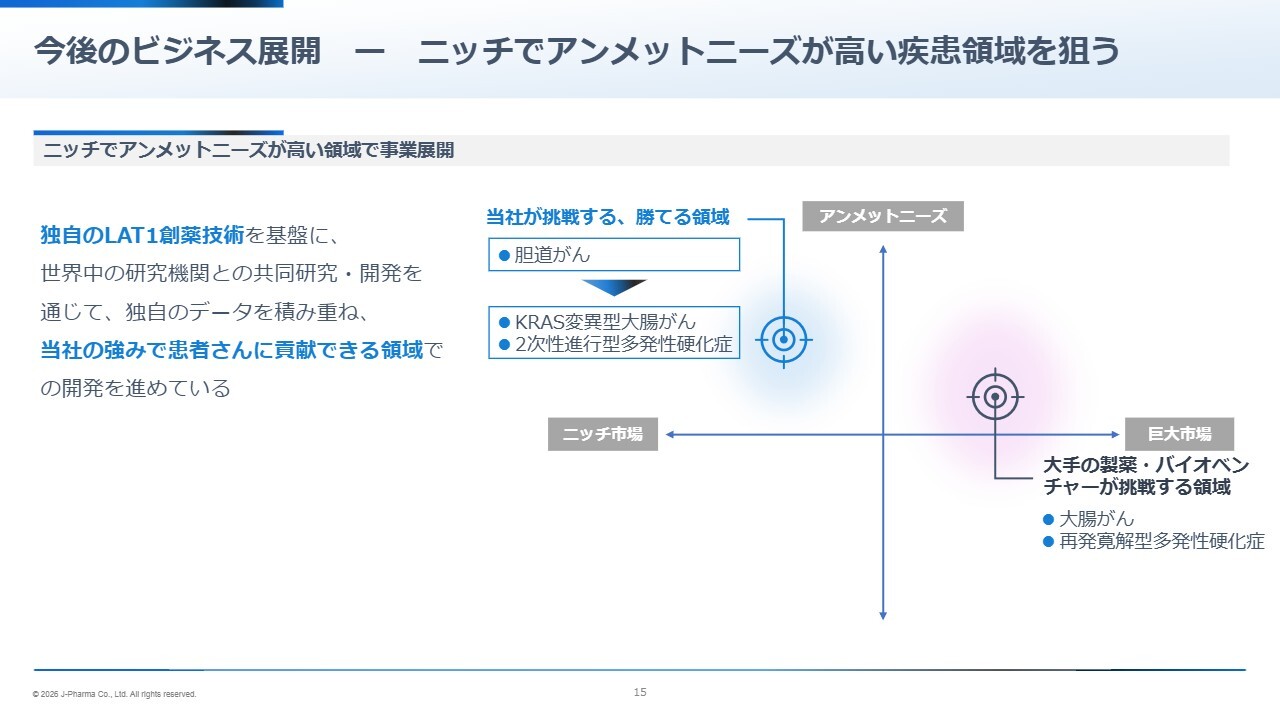
𠮷武:今後のビジネス展開です。私どもは、誰の模倣もしない、自分たちの独特な技術をさまざまなかたちで研究し、自分たちのデータと向き合いながら、専門家の意見に耳を傾けています。
それによって最も効果を発揮できるニッチ市場に注力していますが、ニッチだからといって、市場が小さいわけではありません。さまざまなセグメントの中で、この薬剤の効果が最も発揮できる分野を絞り込み、それを基にグローバルな市場で戦っていくべくモデルを構築しています。
現在、非常に治療が難しい遺伝子変異による大腸がんであるKRAS変異型大腸がんや、自己免疫疾患である多発性硬化症の中でも特に難しい2次性進行型多発性硬化症などについて、アメリカの先生方から一緒に進めたいと要望が寄せられています。
胆道がんでのモデルが成功すれば、これらのお話にもつなげていくことができます。
多発性硬化症の進行とくすぶり炎症
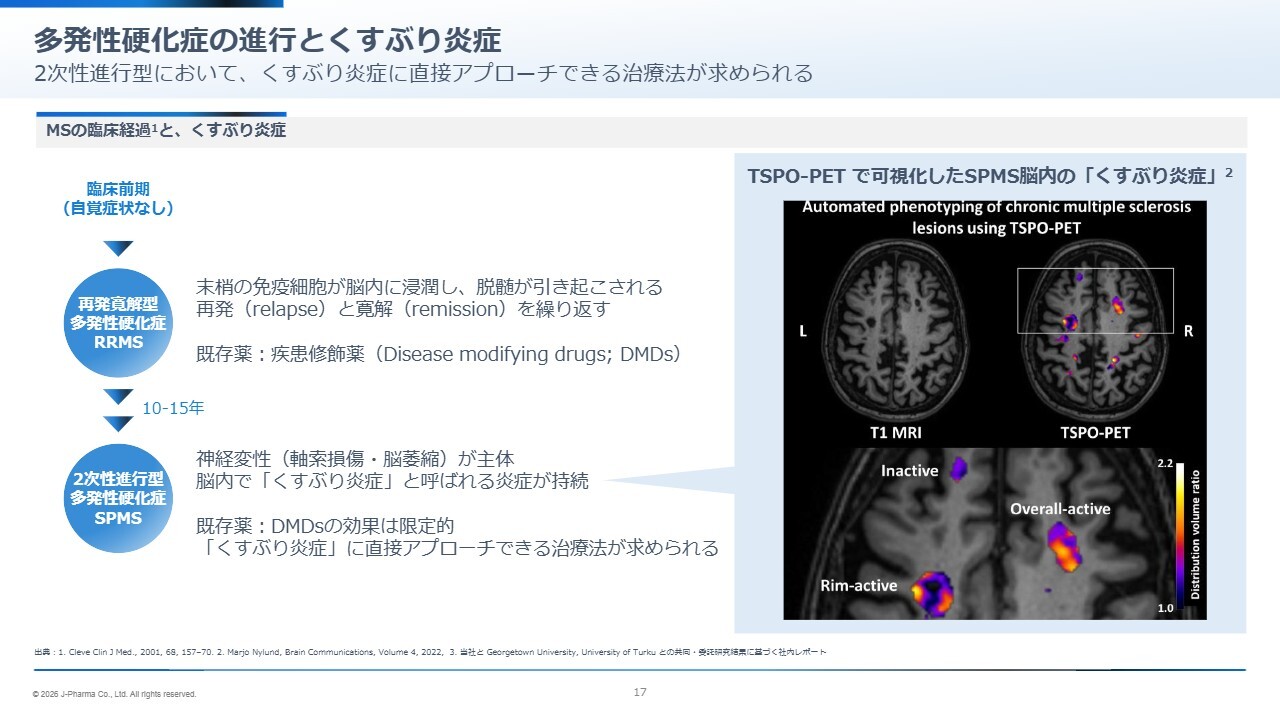
𠮷武:多発性硬化症の2次型である進行型がなぜこれほどまでに悪化してしまうのかについて、すでにジョージタウン大学と7年間にわたり研究を行い、ここ1年半はフィンランドのトゥルク大学の先生方と協力して取り組んできました。
右側に示したMRIの図をご覧ください。多発性硬化症患者さまのMRI画像に、TSPO-PETによって発光する部分を重ねたものです。
悪化していく患者さまの場合、この発光部分が非常に多く見受けられます。これを抑制することで新しい治療法につながるのではないかというコンセプトに至りました。
この分野は誰も取り組んでいない未開拓の分野であり、さらに深く掘り下げて研究を進めたいと考えています。
2次性進行型多発性硬化症に対し、独自の技術で切り込む
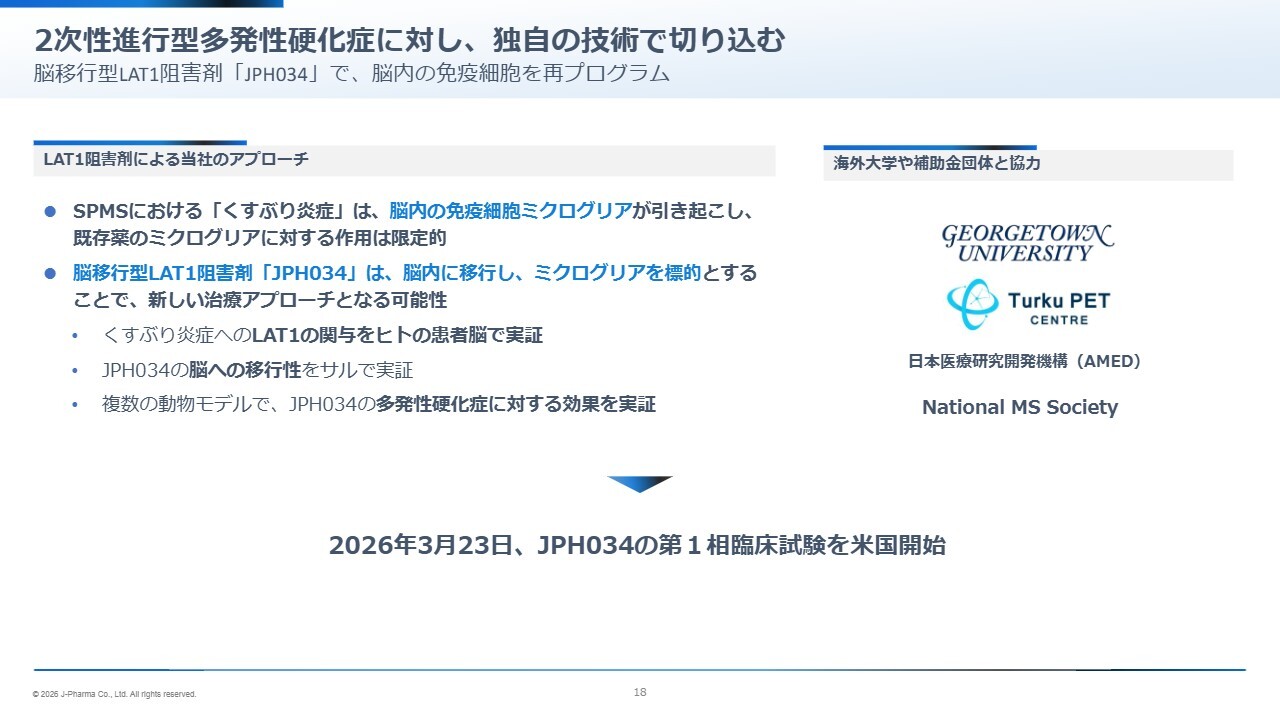
𠮷武:今ご説明した薬剤にあたるのが脳移行型LAT1阻害剤「JPH034」であり、今年3月にアメリカで第1相臨床試験が開始されました。
ジェイファーマの強み - 日本発の革新的創薬をグローバル市場へ

𠮷武:私どもは、独自の技術が確実に役立つと評価されるニッチな領域に絞り込み、グローバルでの承認を目指す企業です。
先ほど「珍しい」とおっしゃっていただいたように、東証グロース市場に上場する企業の中で、自社で創製した医薬品をグローバルフェーズ3まで進めているのは私どもだけです。
私が40年前にこの業界に入った頃は、医薬品は大手企業が開発するものでした。しかし現在では、承認される医薬品の85パーセント以上を、アメリカ、ヨーロッパ、中国の新興バイオベンチャーが開発し、それを最終的に製薬会社が世の中に広めるビジネスモデルに変わってきています。
日本のバイオエコシステムも将来的にはこの方向を目指していくと聞いています。その中で、私どもは日本のバイオエコシステムがさらに活躍し、より活発化することで優れた研究者が誕生し、優れた投資家の方々からのサポートを受けて進んでいけるような企業を目指していきたいと考えています。
以上となります。ありがとうございました。
質疑応答:非専門家に向けて伝えたい自社の評価ポイントについて

関本:丁寧にご説明いただきありがとうございました。バイオベンチャーという難しい領域のため、基本的なところからうかがいたいと思います。
投資家には、医学の専門家はあまり多くないと感じています。そのため「海外のメガファーマに導出した」といった事実ベースの定性的評価によって、「ここは技術的に確からしいぞ」「そうではないのかもしれない」と反応することが多くなります。
そのような意味で、御社のパイプラインについても「自社でやっているからこそ難しいよね」「投資家からは見えにくいよね」と感じられる部分もあると思います。ここが見やすい実績だというポイントな
新着ログ
「医薬品」のログ





