提供:Heartseed株式会社 2025年12月期第2四半期決算説明
Heartseed、売上高の増加で経常利益は初の黒字化を達成 パイプラインも順調に進捗、「HS-001」は治験の患者投与が完了し経過観察へ
免責事項

福田惠一氏:みなさま、こんにちは。Heartseed株式会社代表取締役社長の福田惠一です。本日は、2025年12月期第2四半期(中間期)の決算説明会にご参加いただき誠にありがとうございます。6月12日に適時開示した決算短信をもとにご説明します。
こちらは免責事項です。
本日の目次

本日のアジェンダです。決算の概要、またトピックをお話しした後、質疑応答の時間を取ります。
2025年12月期第2四半期(中間期)決算:P/L
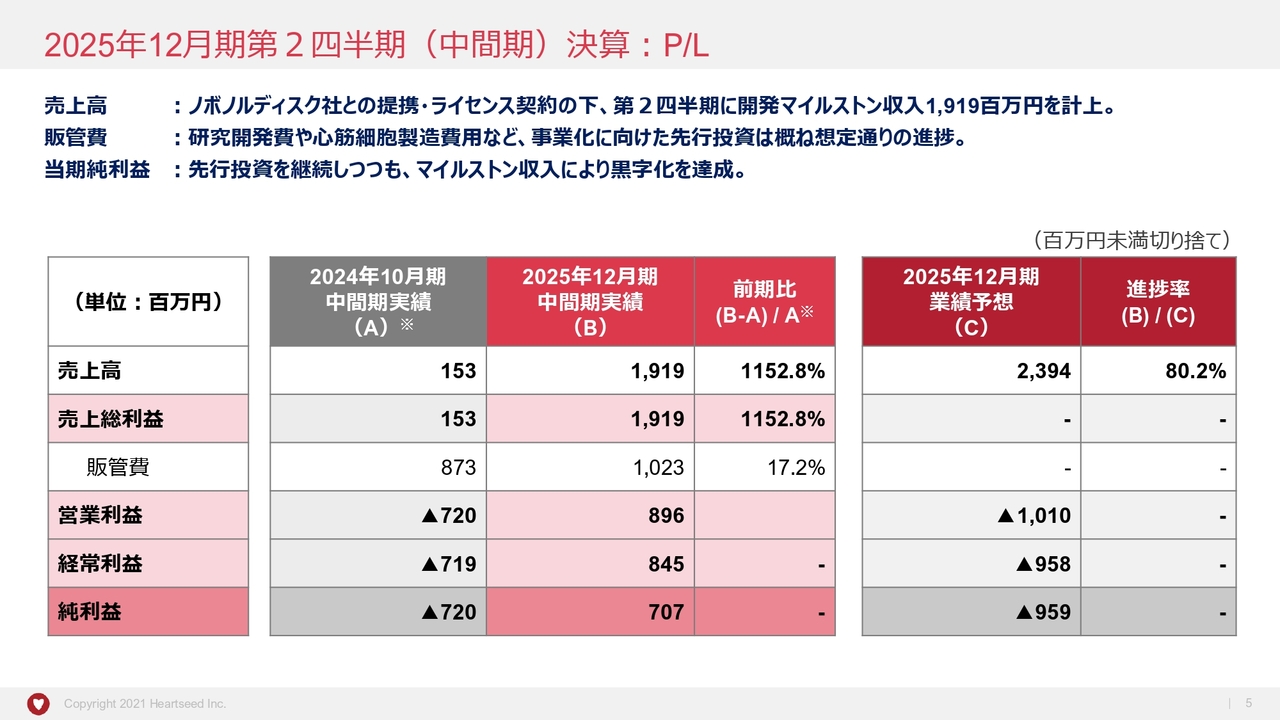
2025年12月期第2四半期(中間期)のP/Lです。
売上高に関して、第1四半期の決算短信における後発事象で、グローバルパートナーのNovo Nordisk社からの開発マイルストン収入を第2四半期に15億5,000万円を計上する予定であるとお伝えしましたが、予定したマイルストン収入にくわえ、もうひとつ別の開発マイルストン収入も発生し、19億1,900万円となりました。今年度の業績予想に対し順調な進捗となっています。
売上総利益は、現状、売上原価がありませんので、売上と同様となります。
販管費は、大半を占める研究開発において、「HS-001」の最終治験「LAPiS試験」の患者投与が1月末に完了したものの、フォローアップにかかる費用にくわえ、心筋細胞製造費用など、事業化に向けた投資も進み、昨年度比17パーセント増の10億2,000万円と概ね想定どおりの進捗となりました。
営業利益は、19億円強の売上高の計上に伴い、8億9,600万円となりました。
経常利益は、第1四半期から第2四半期にかけて円高ドル安が進んだことによる約5,000万円の為替差損の影響を僅かに受け、8億4,500万円、純利益は7億700万円となり、四半期・中間期ベースではありますが、創設以来初の黒字となりました。
一方、今年度末である12月末までに予定している残りのマイルストン収入や、加速する事業化に向けた投資などを鑑み、現時点においては、今年度の純利益の予想のマイナス9億5,900万円は据え置きました。今後の進捗を見ながら、修正が必要となる場合には、適宜適切に開示を図っていきます。
2025年12月期第2四半期(中間期)決算:B/S
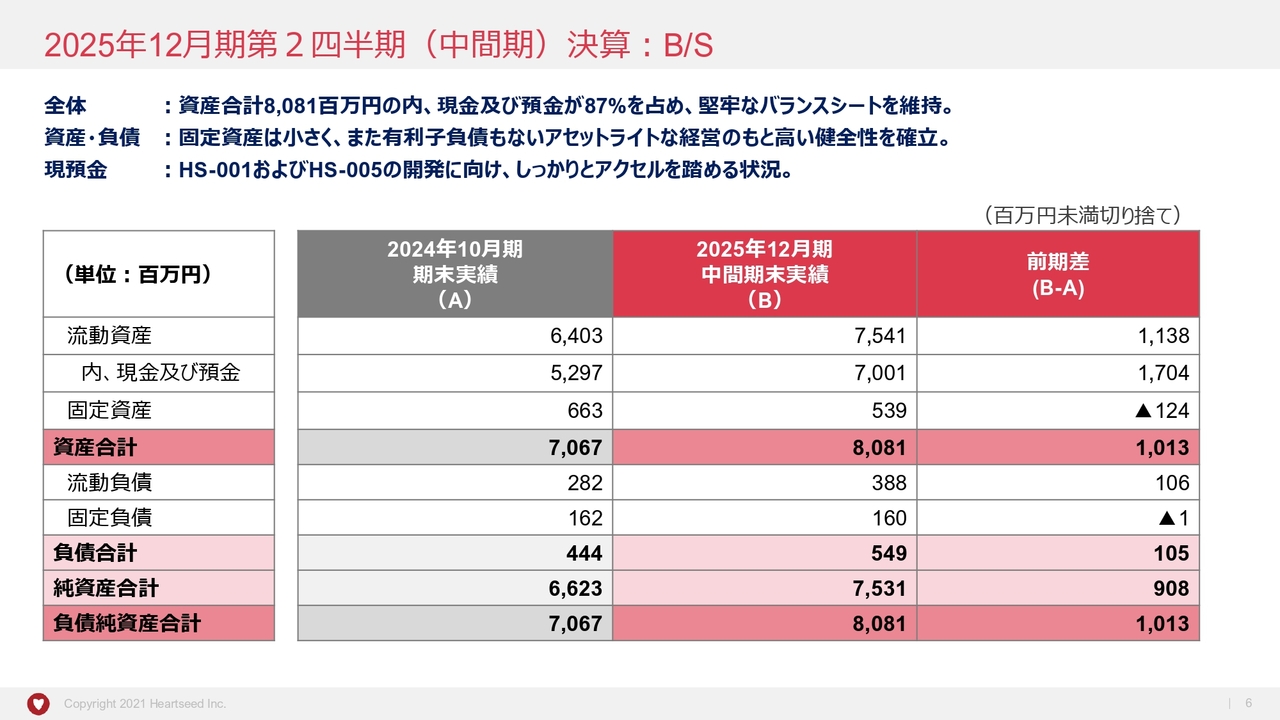
B/Sです。P/Lでお話ししたように、Novo Nordisk社からのマイルストン収入があったことにより現預金が増え、資産の大半を占める中、堅牢なバランスシートを維持しています。
また、アセットライトな経営のもと、有利子負債もなく、高い健全性を維持しています。今後加速します、「HS-001」の承認や上市に向けた準備、また「HS-005」の開発に向けて、しっかりとアクセルを踏める財務状況であると考えています。
2025年12月期第2四半期(中間期)開発目標に対する進捗

主な事業進捗について説明します。
冠動脈バイパス手術との併用で行われる「HS-001」は、国内最終治験の「LAPiS試験」において、1月末に全10例の患者投与が完了し、現在経過観察中です。データの取りまとめや承認申請に向けた準備が粛々と進んでいます。
弊社にとって重要である学会が9月以降に複数予定されていますが、高用量群を含めた最新データについて、治験施設の先生方にご発表いただけるのではないかと期待しています。
カテーテルによる投与の「HS-005」については、詳細を申し上げることはできませんが、治験届の提出に向けて、当局との相談が進んでいます。また、カテーテルの共同開発について、新規パートナーとの開発が順調に進捗しており、国内での治験に向けて、2025年内での治験届の提出を、変わらず目標としています。
自家iPS細胞から作製する心筋細胞の「HS-040」は、国からの補助金をもとに、開発を進めています。治験の実施に向けて、細胞製造に関する基礎的な技術開発の積み上げや、前臨床試験などを進めています。
高用量群を含めたLAPiS試験の最新データの発表機会
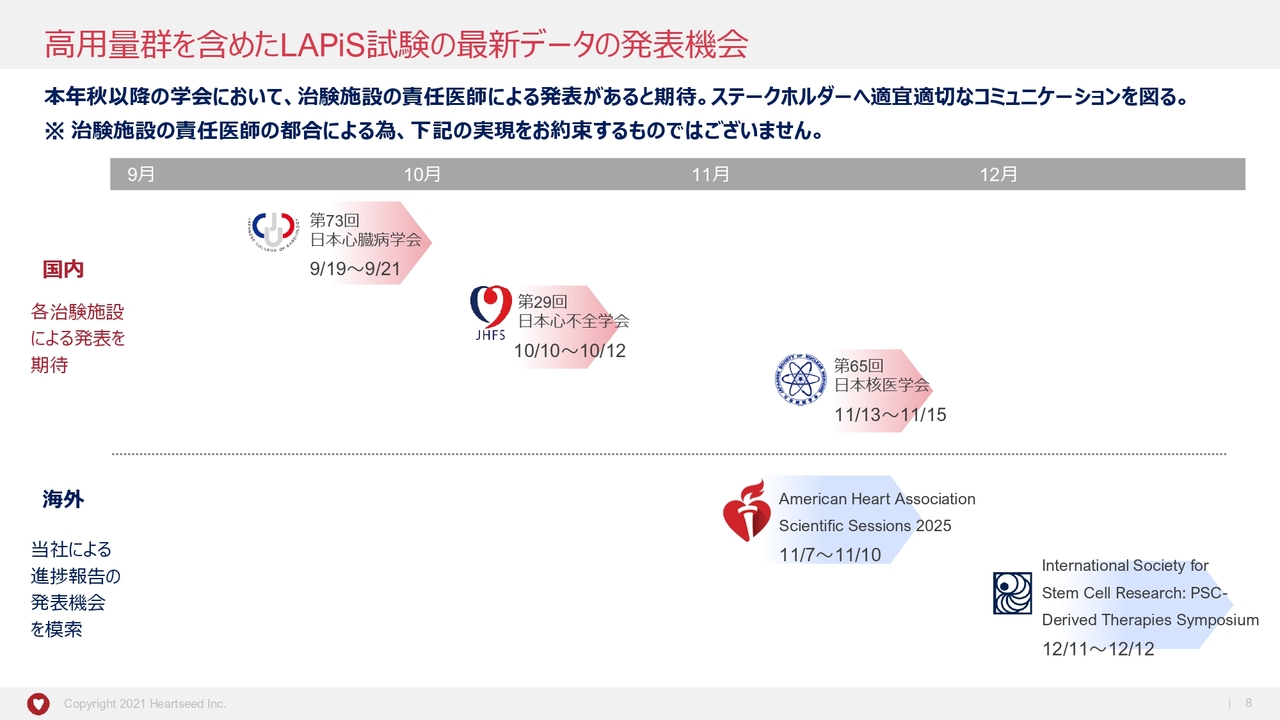
「HS-001」における国内最終治験「LAPiS試験」について、高用量群を含めた最新データがどのタイミングで学会発表されると考えているのか、ご説明します。
はじめに、学会発表は、治験施設の責任医師のご都合によるところが大きいので、弊社としてお約束できるものではなく、あくまで現時点における可能性であることをご理解いただければと思います。
独立安全性評価委員会の承認のもと、2024年8月以降に高用量群の投与が開始され、2025年1月末に最終となる10例目の投与が完了しています。
そうした中、国内においては、9月以降の主要学会において、一部の治験施設の先生方から、高用量群における、移植後6ヶ月のデータを含めた学会発表をしていただける可能性があると考えています。
一方、海外においては、国内において治験施設からの発表があることが前提とはなりますが、それらのデータをもとに、国際学会やシンポジウムにおいて、弊社から複数施設のデータを包括したかたちで、進捗報告することを目指しています。
世界初となる心筋補填療法の治験であるため、治験施設の先生方の発表意欲も高く、また学会側も、発表のエントリーを受け入れていただける可能性は十分にあるものと考えています。
製品パイプライン
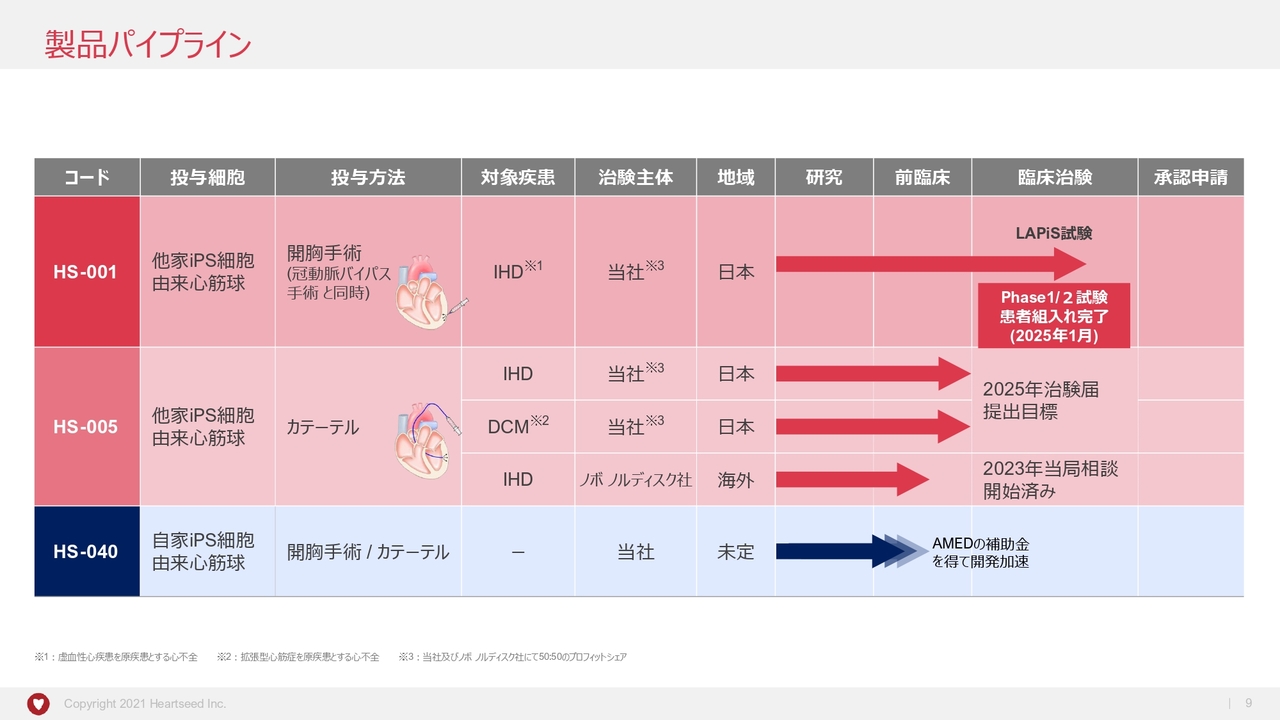
製品パイプラインのおさらいです。国内で治験中の「HS-001」と、開発が進むカテーテル投与の「HS-005」は、Novo Nordisk社との提携の対象製品です。
一方、自家iPS細胞由来心筋球、「HS-040」は、当社がグローバルでの権利を有しています。
メインパイプラインの中長期目標マイルストン(2025年6月12日現在)
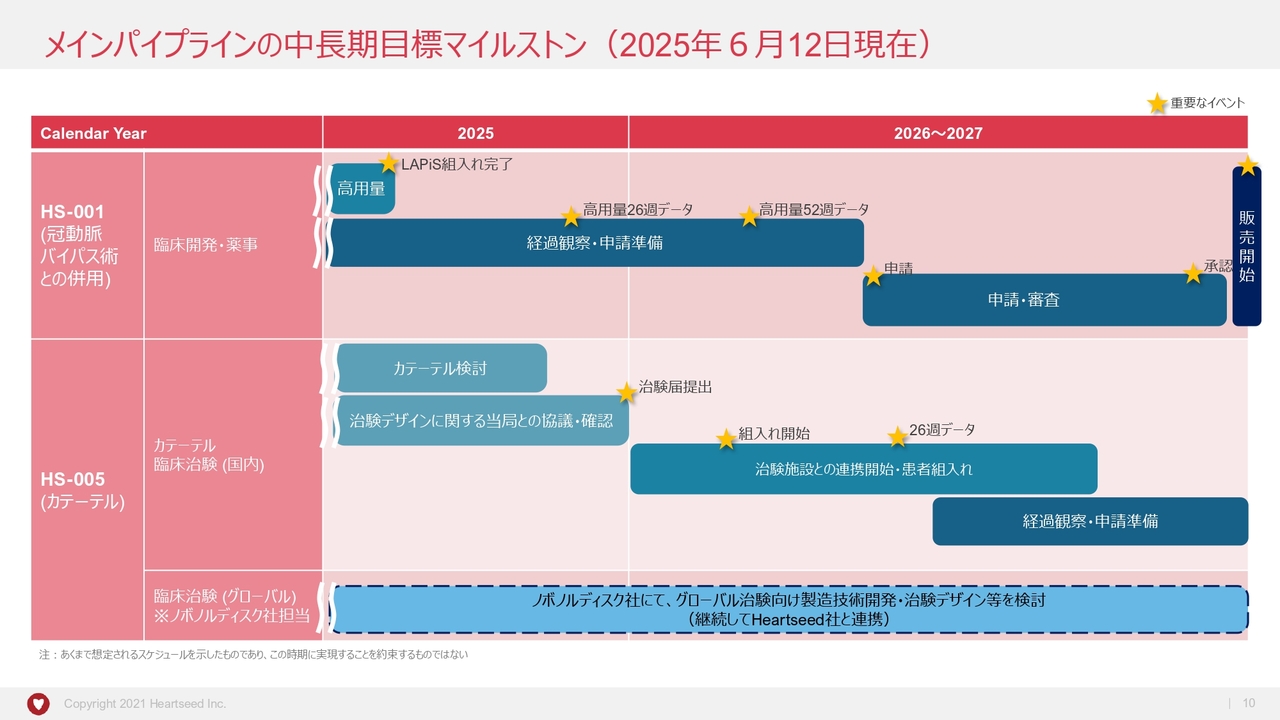
従前よりお示ししているスケジュールから変更はありませんが、「HS-001」と「HS-005」の詳しいスケジュールについてご説明します。
「HS-001」は、全10例の患者投与が1月末に完了し、現在、経過観察にくわえ申請に向けた準備を進めています。あくまで目標ではありますが、2026年内の承認申請、2027年内の承認および販売開始をめざしています。
「HS-005」については、新規パートナーとのカテーテル開発が進む中、当局との相談も進捗しており、2025年内での治験届の提出、また2026年内の患者組入れ開始を目指しています。
「HS-005」のグローバル展開に向けては、Novo Nordisk社において引き続き細胞製造技術開発にくわえ、治験デザインの検討等が進んでいます。
知財戦略や実用化への進展を高くご評価いただきました。

2025年12月期中間期における主なトピックについてお話しします。
2025年1月に、「第7回日本医療研究開発大賞 スタートアップ賞」を受賞しました。石破総理のご臨席のもと、表彰状を頂戴しました。「スタートアップ賞」は、将来性の高い技術を開発するスタートアップ企業を対象とする賞部門で、弊社事業の社会的意義と実用化に向けた進展をご評価いただいたものと理解しています。
また、4月には、「知財功労賞 経済産業大臣表彰」を受賞しました。知的財産関連において大変名誉高い賞です。研究初期から上市後まで各段階に応じた網羅的な特許網を構築した知財戦略を高くご評価いただきました。
世界のアカデミア界における当社のリーディング・ポジションを確認

この半期においては、国際的な学会やシンポジウムから、心筋補填療法の企業としては唯一招聘を受け、技術や治験の初期データを世界のアカデミアに共有する機会が多くありました。
日米欧を中心とした世界トップのサイエンティストより期待の言葉をいただいたとともに、競争環境下における弊社のリーディング・ポジションを改めて確認することができました。着実かつ迅速に事業化を進めていきたいと思います。
小職は、僭越ながら「社長メッセージ」たる所感を、不定期ではありますが、弊社Webサイト・IRページに掲載し始めたところです。2025年3月が第1回の連載です。年数回程度を目標として今後も掲載していきますので、当社の事業活動における方向性の理解の一助としていただければと考えています。
再生医療で心臓病治療の扉を開く

ご多忙の中、ご清聴誠にありがとうございました。
新着ログ
「医薬品」のログ





