エーザイ株式会社 2021年3月期第3四半期決算説明会
エーザイ、長期化するCOVID-19の影響下でも増収を達成 将来の企業価値のための先行投資を断行
2020年度第3四半期 連結業績(IFRS)
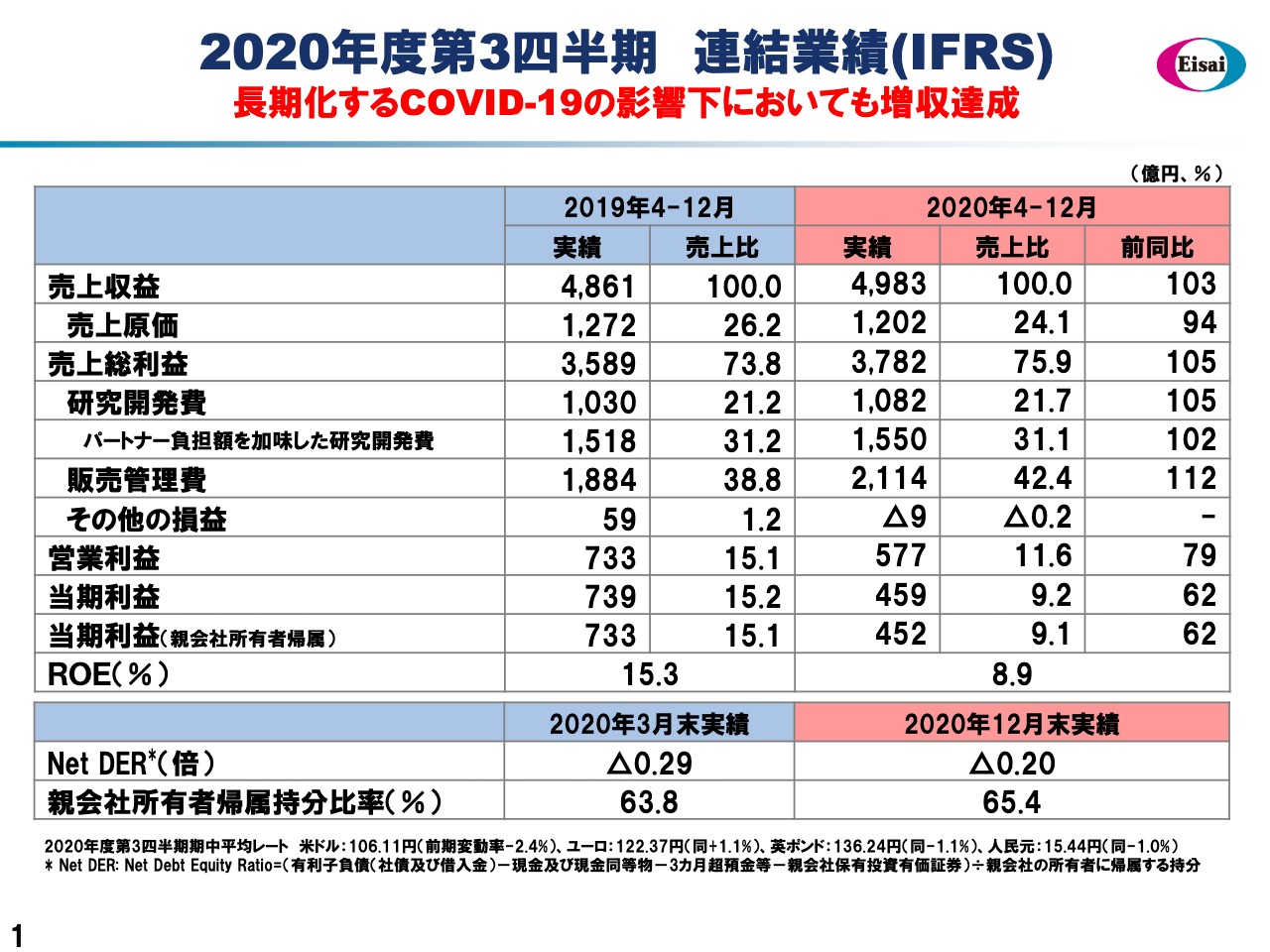
柳良平氏(以下、柳):それではCFOの柳より、財務セクションにつきご報告申し上げます。初めに1ページのスライドをご覧ください。こちらでは、2020年度第3四半期9ヶ月間の連結のP/Lの概況をお示ししています。COVID-19の影響を受けながらも、増収を達成することができました。そのトップライン、売上収益ですが、4,983億円と、前年から103パーセントの成長・増収を果たすことができました。
日本国内における薬価改定の影響、為替の影響等がございましたが、事業開発案件に加えて、「レンビマ」を中心としたグローバル品で折り返して、増収を達成しています。
特に「レンビマ」は、前年から232億円の増分を獲得しています。さらに特記事項といたしまして、「レンビマ」のカレンダーイヤー(1月から12月までの暦年)の通算セールスが、1.2ビリオンドルのスレッシュホールドを達成したことから、メルク社からのマイルストンペイメント、200ミリオンドルを売上収益として認識しています。
そして、原価率の低い「レンビマ」の躍進により、プロダクトミックスが改善したことから、原価率は24.1パーセントにまで改善してきています。それらをもちまして、コアの収益としての売上総利益(粗利)は3,782億円。前年から105パーセントの増益を獲得することができました。このように増収、コアの収益の増益を獲得していますが、ここから経営の意思をもって、将来の企業価値のために先行的な費用投入を断行しています。
まず、研究開発費は1,082億円。前年から105パーセント増加。売上高に対する比率は21.7パーセントとなっていますが、主な増分は「レンビマ」、さらに「次世代アルツハイマープロジェクト」に大きな資源を投入しています。なお、パートナーからの負担金を468億円入手していますので、真水では1,550億円の研究開発費投入。研究開発費率は31.1パーセントと、グローバルな製薬産業の中でも、最もR&Dに資源投入をしている会社の1社という位置付けであります。
一方、販管費の投入につきましては2,114億円。前年から112パーセントの2桁増。販管費率はやや異常値になってきていますが、42.4パーセントと高まってまいりました。しかしながら、この販管費には「レンビマ」の前向きな費用とも言うべき、メルク社へのプロフィットシェアリング、利益折半費用の支払い470億円を含んでいますので、それを除きますと販管費率は実質33パーセントと、グローバル・ピアのアベレージに近付いてまいります。
販管費投入は2桁増ではございますが、申し上げましたプロフィットシェアリングで100億円以上、約半分程度の増分は説明がつきますし、残りも前向きな「デエビゴ」の費用や、次世代アルツハイマー品の将来の患者さま貢献への準備の費用など、積極的な先行投資を行っています。昨年度はその他の損益で、エルメッドエーザイの譲渡益44億円を計上していますが、今年度は大きな特殊要因はございません。
それらをもちまして、営業利益は577億円。前年から約80パーセントではございますが、引き続きOPマージンは2桁の12パーセント弱を確保しています。なお、この営業利益の577億円は、事業計画を大幅にアウトパフォームしています。また、純利益(当期利益)に目を向けてみますと、ボトムラインは昨年度、特殊要因がございました。
日米間の資金の偏在を解消するために行った米国減資の結果として、約151億円のタックスベネフィットを享受したことから純利益が高くなっていますが、特殊要因のなくなった今期は452億円の純利益。前年からは62パーセントではございますが、こちらの当期利益も営業利益同様に、事業計画を大幅にアウトパフォームするかたちとなっています。
また、9ヶ月間の参考値ですが、この期間の平均ROEは8.9パーセントと、株主資本コストの前提8パーセントを上回って、正のエクイティスプレッドを創出。企業価値を創造しているという理論値になります。一方で、バランスシートアイテムに目を向けてみますと、Net DERはマイナス0.20倍と、引き続きネットキャッシュポジション、実質、無借金会社のステータスでございます。
しかしながら、費用投入と同様に投資の年と位置付けて、通常の資本的支出の2倍に近いレベルの積極的な資本的支出を、設備投資やIT、DX、事業開発等に資源投入していますので、キャッシュバランス自体は減少しています。それでもなお、ネットキャッシュが1,300億円超、自己資本比率は65パーセントと、財務の健全性、ストロングバランスシートは万全でございます。
ご参考までに、今年度は信用格付機関R&I社から、「AA-」へ格上げをいただいています。このようなファイナンシャルインテグリティに依拠して先行投資を支えている、第3四半期の決算でございました。
売上収益の増減要因分析
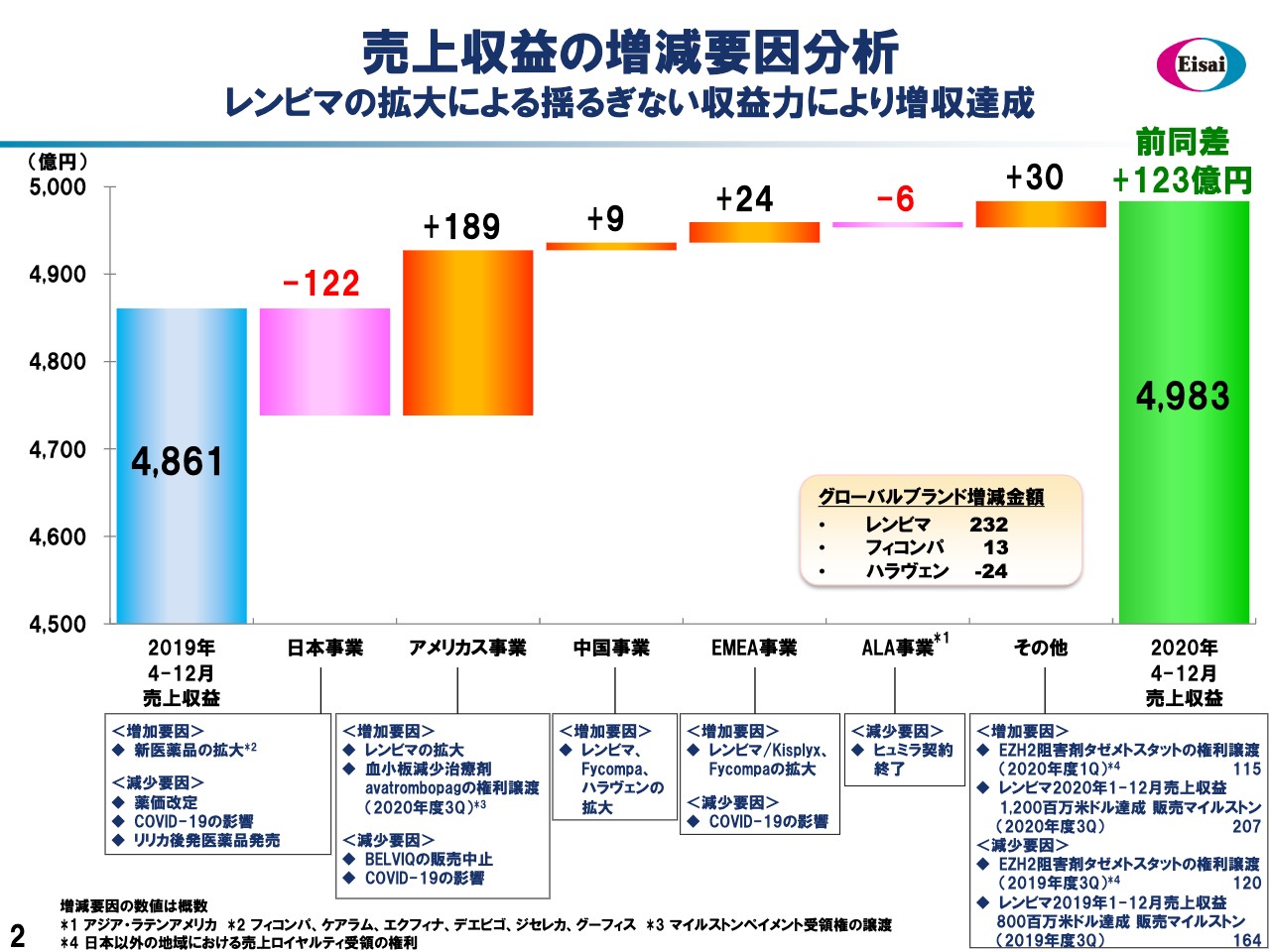
次のスライドをお願いします。2ページの滝グラフでは、売上収益の増減要因をお示ししています。昨年度9ヶ月間の売上は4,861億円。日本事業につきましては、COVID-19に加えて薬価改定の影響、「リリカ」の後発品の影響などがございました。また、アジアでは「ヒュミラ」の契約終了の影響がございました。しかしながら、それ以外の海外、すなわち欧米・中国におきましては、グロースドライバーの「レンビマ」を中心として、しっかりと増収を獲得しています。
事業開発案件の出入りはございましたが、特記事項として申し上げましたとおり、「レンビマ」がカレンダーイヤーの節目、1.2ビリオンドルの売上を計上し、メルク社から200ミリオンドルのマイルストンを収益認識していますので、プラス30億円にネットではなっています。これらをもちまして、前同差プラス123億円の増収、4,983億円の売上の着地となっています。
営業利益の増減要因分析
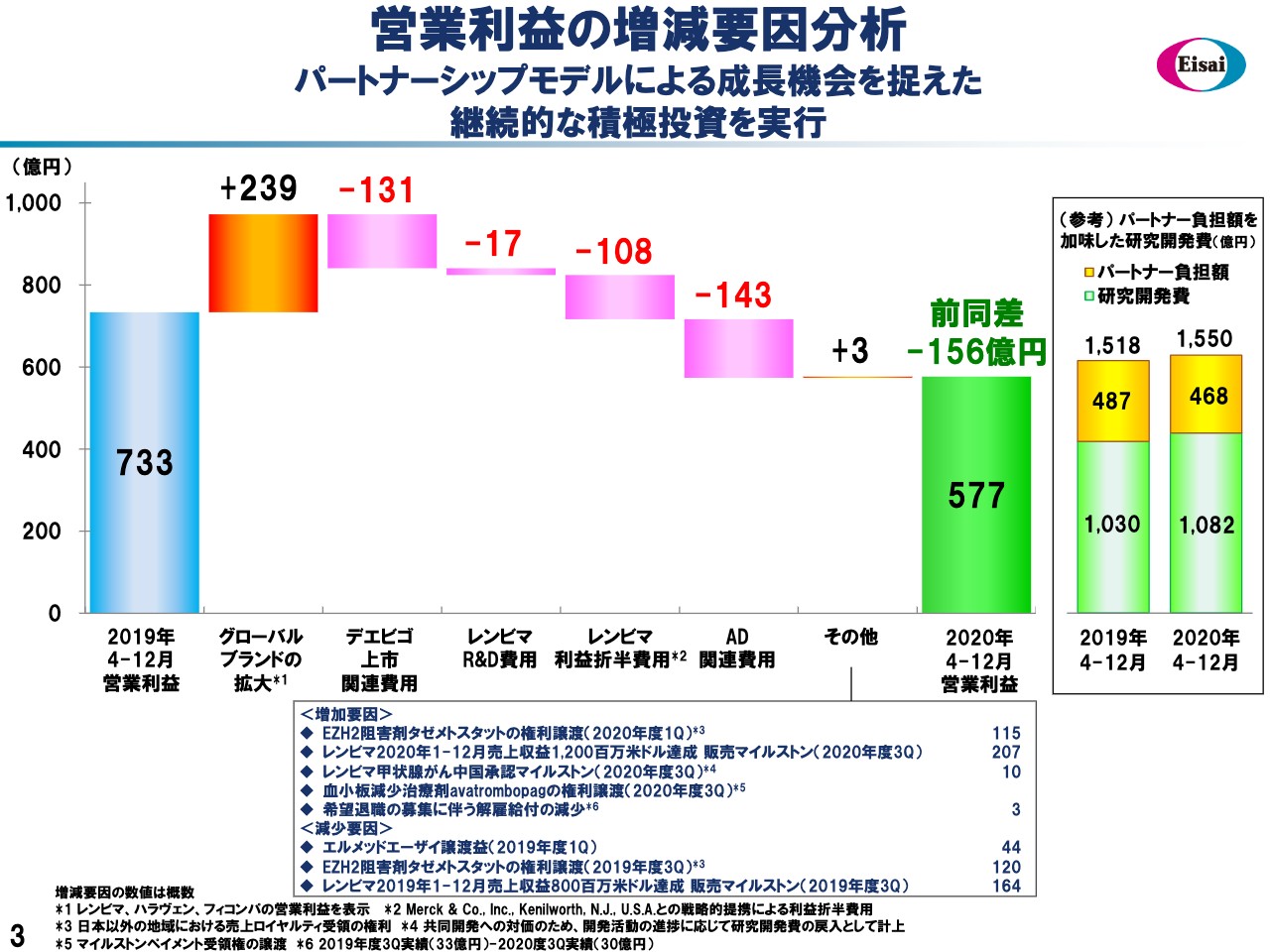
次に、3ページの滝グラフでは、営業利益の増減要因をお示ししています。昨年度9ヶ月間の営業利益は733億円でございました。それに対しまして、「レンビマ」を中心としたグローバルブランドの増収によりまして、しっかりと増益。239億円の利益を獲得しています。さらにそこから経営の意思をもって、前向きな先行投資を行っています。
「デエビゴ」の上市関連費用131億円。「レンビマ」のR&Dが17億円の純増。「レンビマ」のプロフィットシェアリングが108億円の増加。そして、次世代AD品の関連費用が143億円となります。このような前向きな先行投資がございましたので、営業利益は577億円の着地となっていますが、申し上げたように、事業計画は大幅に過達という状況でございます。
右のボックスで、ご参考までにR&D費の内訳をお示ししています。申し上げたように、会計上のネットの研究開発費は1,082億円の計上ですが、パートナーからの負担金で468億円を得ていますので、真水では、引き続き1,500億円を超える大幅なR&D費の投入を、将来の企業価値創出に向けて行っています。
2020年度 連結業績見通し(IFRS)
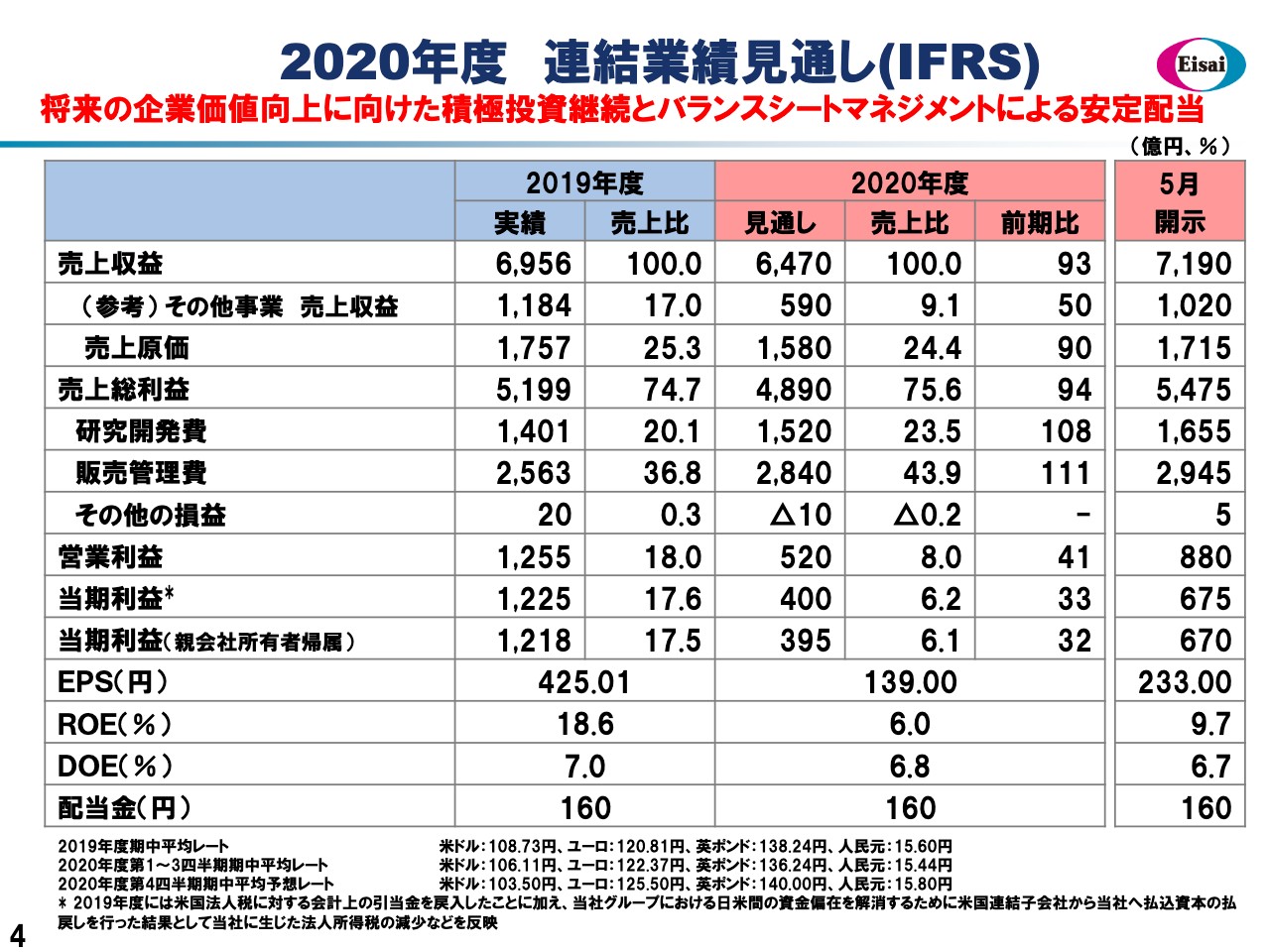
次に、4ページのスライドでは、2020年度通期連結業績見通しをお示ししています。5月の決算短信から修正を行わせていただいています。残念ながら下方修正となっていますが、サマリーといたしましては、将来の企業価値のために積極的な先行投資を断行し、一方で、バランスシートマネジメントでそれを支えながら、安定配当も両立するという絵が浮かび上がってきます。
初めにトップライン、売上収益ですが、6,470億円に修正させていただきました。これにつきましては、COVID-19の影響が当初企図した以上に長期化し、深刻化した。それらの売上収益に対する影響。さらには、競合関係やマーケットの需給の関係などもございますが、単一かつ最大の特殊要因としては、「レンビマ」関連がございます。「レンビマ」の通期グローバル売上の予想は、5月には1,580億円と開示させていただきましたが、決算短信・参考資料で今回お示ししているように、1,415億円に修正させていただきました。
この変更の狭間に、最後のもう1つの販売マイルストンのスレッシュホールドがございまして、そのもう1つの販売マイルストンの基準を満たさなくなったことから、メルク社からの、最後の予定していた販売マイルストンが今期、獲得することができない見通しとなりました。したがいまして、それは翌期以降に持ち越されることになります。
メルク社からの販売マイルストンは、セグメント情報では、参考でお示ししています「その他事業」に含まれています。参考資料にあるとおり、590億円の予定になっていますが、もちろんマイルストンだけではなく事業開発関連や輸出入等、さまざまな要素がありますが、セグメントとしては、マイルストンは「その他事業」になります。
そして、このメルク社からの販売マイルストンは権利を失ったわけではなく、来期以降に一定の基準を満たせば同額を獲得することができますし、もともとのメルク社との戦略的提携の契約時においては、当初、2021年度に達成するかたちで予定していたものでございますので、相対の「レンビマ」フランチャイズにかかるNet Present Valueには大きな変動はない、企業価値には大きな変動はないと考えています。
原価率は24.4パーセントに改善し、粗利4,890億円。研開費・販管費は申し上げてきましたように、引き続き、将来の企業価値最大化に向けて先行投資を断行する。その結果として、営業利益は通期520億円を見込んでいます。こちらにつきましては、トップラインとパラレルで影響がございますが、もちろん単一で最大の理由は、先ほどの販売マイルストンの翌期以降への期ズレになります。
いわゆるボトムライン、親会社所有者帰属の当期利益は395億円を見込みます。そこから価値創造のKPI、EPS・ROE・DOE等はこのように算出されます。ROE、6パーセントレベルと修正させていただいていますが、企業価値創造につきましては複数年でこのKPIを見ていく。すなわち、これも含めまして、5年平均のROEは10パーセント以上を望んでいますので、十分なエクイティスプレッドを確保できる。
あるいは足元のボラティリティから、株主資本コストが足元では上昇しているというアサンプションも吸収できるレベルに、5年平均でショートターミズムに陥らずに、ロングターミズムで企業価値創造を果たしてまいります。
なお、配当金160円は、EPSとの比較で配当性向115パーセントとなりますが、こちらもロングターミズムで、5年平均の配当性向は70パーセント未満に抑えられますし、1,300億円以上のネットキャッシュ、自己資本比率65パーセント以上のストロングバランスシートを有していますので、バランスシートマネジメントに基づく配当政策を施行し、安定配当を成長投資と両立してまいります。
以上、財務セクションにつき、私から申し上げました。ありがとうございました。
認知症がもたらす社会への影響 課題解決への使命

アイヴァン・チャン氏:ニューロロジービジネスグループのアイヴァン・チャンと申します。本日はニューロロジーフランチャイズの重要な進展について、最新の情報を提供したいと思います。アルツハイマー病に特に強調しながら、お話をしたいと思います。
次のスライド、5ページ目。アルツハイマー病は「見えないパンデミック」と呼ばれてきました。新型コロナよりも、より重篤で、長期にわたるコストもかかる恐れがあると考えられます。非常に重要なこととして、アルツハイマー病が、コロナに次いで優先度の高い医療の領域であり続け、そして現在のパンデミックの間、およびそれ以降も、患者さまを見過ごすことをしてはならないということです。
スライドの左側にご覧になれるように、2050年までに、世界の人口の6人に1人が65歳以上になります。認知症当事者が1億5,200万人に達する。そして、現在の3倍になると予測されています。全世界で、認知症当事者の約60パーセントが現在、低中所得国に住んでいます。この数字は2050年までに71パーセントに伸びる予測です。世界の認知症にかかるコストは、2015年には90兆円でありました。これが国だとしたら、世界で第18位の経済規模になります。
1月25日に、スライドの右側にご覧になれるように、弊社CEOの内藤は、アルツハイマー病に取り組む世界経済フォーラム「The Davos Agenda」、2021年会合におけるパネルに参加しました。そこでアルツハイマー病の課題と戦うための、グローバルな連携の必要性について話し合い、また、世界中の患者さまとご家族に、効果的な解決策をお届けするためのエーザイのビジョンを共有しました。
内藤は、特に「患者さまの参画、ならびに一般生活者の参画が重要である」ということを強調していました。それは健康な睡眠・食事・運動など、また、脳の健康のための予防行動の推進や、ブレインパフォーマンスのチェックのために必要です。このため、デジタル技術はスマートでアクセス可能なソリューションを提供することができ、低中所得国においても使うことができます。
アルツハイマー病の危機がもたらす甚大な社会経済的な影響に鑑みますと、官民パートナーシップが必要で、ソリューションを見つけ出すためには、力を合わせることが必要です。特に今後来たる、初の疾患修飾薬の準備を整える中で必要になるでしょう。
同じ日、1月25日に、「Davos Alzheimer’s Collaborative(DAC)」が正式に立ち上げられました。これは、これまで世界経済フォーラムが促進してきた、ヘルスケア・医療分野の取り組みをモデルにしたものです。例えば、GAVIアライアンス、ワクチンと予防接種のための世界同盟、また、CEPI(感染症流行対策イノベーション連合)などです。
このDACにおいては、官、学、NGO、そしてさまざまな業界のパートナーが集結する、官民パートナーシップになります。エーザイにおいては、このような、この種で初めてのグローバルな取り組みに参画できていることを、誇りに思っています。
aducanumab

次のスライド、6ページ目になります。先週の、パートナー社のバイオジェンとともに行った共同プレスリリースでご覧になったように、アメリカのFDAにおいては、「aducanumab」BLA申請のPDUFAアクションデートを3ヶ月延長し、今年の6月7日としました。私どもは、FDAとバイオジェンとの間で行われている継続中の協議を、力強く思っています。
継続中の審査の一環として、バイオジェンはFDAによる追加情報の要請への回答を提出しました。その中には、追加の解析や臨床データが含まれています。これらをFDAにおいては、審査により時間がかかる申請の主要な改定とみなしたようです。FDAがこの協議を継続していることをありがたく思っています。今後もFDAと協議を継続することに期待し、「aducanumab」の審査の完了につながるように期待しています。
「aducanumab」の申請については、EUにおけるEMAが審査中であり、また、ここ日本においてはPMDAによる審査が行われています。バイオジェンは日本において、厚生労働省に昨年12月10日に新薬承認申請を提出しました。それに加えまして、他の地域におきましても順次、当局相談を実施しています。また、「EMBARK」の再投与試験における適格患者さまの登録を続けていきます。
バイオジェン社とともに、おそらく世界初のAD疾患修飾薬として上市を目指している、その中で、アメリカでの上市準備は整っています。また、主要マーケット、日本やヨーロッパなどでの上市に向けての準備を強化してまいります。
抗Aβプロトフィブリル抗体 lecanemab①

次のスライド、7ページ目です。それでは、「lecanemab(BAN2401)」に話を変えたいと思います。まず、最初にClarity AD試験についてですが、第Ⅲ相のプログラムです。早期AD患者さまをターゲットとしています。先月、スクリーニング登録を締め切りました。間もなく患者さまの割り付けも完了予定です。Data readoutは予定どおり、2022年度第2四半期を目指しています。
本試験における在宅での治験薬の投与や、遠隔医療のインフラを整える前に、昨年のコロナ感染の第一波の際に、投与機会が一時的に失われた症例の影響に関し、積極的にFDAと協議を続けてまいりました。進行中の治験における新型コロナ関連の課題対応のための、FDAガイドラインの吟味を行いました。また最近、「昨年、投与機会が失われた症例の影響を緩和できるよう、約200症例を追加する」というFDAからの貴重な助言を得ることができました。
これによりまして、単一の承認申請用の試験である本試験の主要解析のため、最高の質のデータの確保を目指してまいります。目標登録症例数は1,566例から1,766例まで増加されました。この変更は、Clarity AD試験の何らの臨床結果の情報もない状態で実施されました。また、我々は、この1年間の本試験の大きな進展を積極的に管理できてきたと思っています。患者さまの割り付けも間もなく完了予定です。これまでどおり、Data readoutは2022年度の第2四半期末までに完了する予定です。
抗Aβプロトフィブリル抗体 lecanemab②
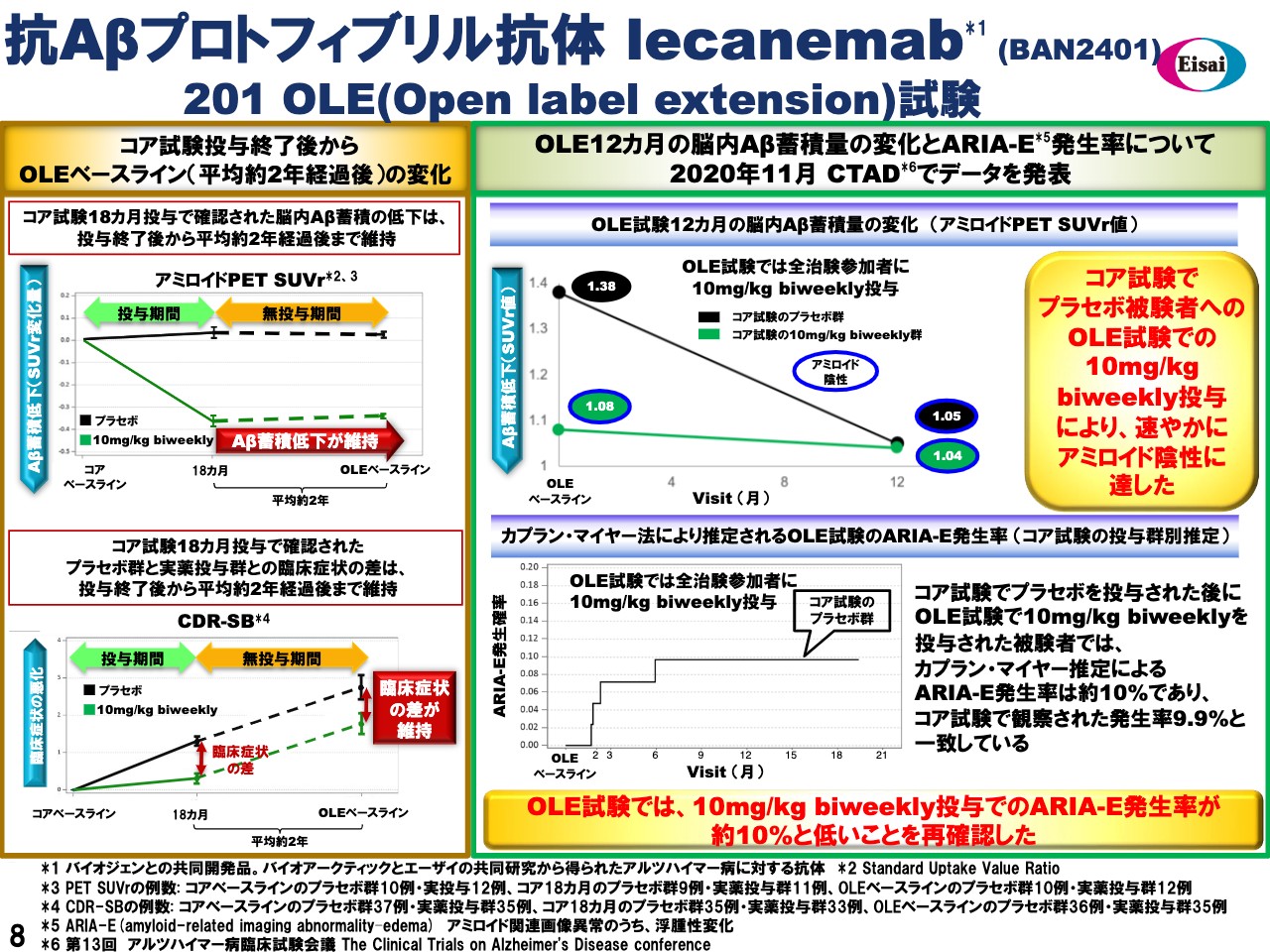
次、8ページ目をお願いします。もう1つ、「lecanemab」のstudyが行われており、201 OLE(Open label extension)studyです。コア試験(201試験)の終了後、無投与期間が平均で約2年間ありました。その後に180人のコア試験の治験参加者に対して、OLE studyにおいて最高用量、10ミリグラム/キログラム biweeklyの投与を行いました。これはコア試験中の投与用量、何を投与を受けたのかとは関係なくです。
そして1年ほど前に、この201 OLE試験のベースラインデータを発表しました。左側にお示しのように、脳内Aβの蓄積の低下が維持されている。投与終了後もそれが持続している。それからCDR-Sum of Boxesの差についても、「lecanemab」群とプラセボ群との間での差が、投与終了後も持続をしているという結果です。
また、昨年11月のCTADでは、アミロイドPETの結果、それからARIA-E発生率を、最高用量10ミリグラム/キログラム biweeklyでOLE試験で投与した、12ヶ月投与期間後の発生率と、アミロイドPETの結果について発表しています。右側でお示しのように、コア試験中にプラセボ投与を受けていた治験参加者は、OLE試験では最高用量、10ミリグラム/キログラム biweeklyとなり、速やかに多数の治験参加者がアミロイド陰性を達成しています。
このデータは、「lecanemab」10ミリグラム/キログラム biweeklyで、タイトレーションがないという用量のポテンシーを確認する結果となっています。コア試験で示されたことが確認されています。また、同じ治験参加者の、カプラン・マイヤー推定によるARIA-E発生率は約10パーセントで、コア試験のARIA-E発生率9.9パーセントと、一貫性のある数字となっています。
「lecanemab」10ミリグラム/キログラム biweeklyのARIA-Eの発生率が低い、10パーセントほどであるということが確認されました。この201 OLE試験のベースラインの結果、そして12ヶ月の投与期間の後の結果について、大変意を強くしています。「lecanemab」の有効性・安全性について、良好なプロファイルをサポートする結果となっています。
抗Aβプロトフィブリル抗体 lecanemab③

「lecanemab」の3つ目の試験が、AHEAD 3-45第Ⅲ相試験です。最初はPreclinical、アルツハイマー病治験参加者です。ACTCとの協力によるものです。登録がアメリカ、そして日本で継続中です。また、他の多くの国で施設の立ち上げの準備が順調に進んでいます。スライドでお示しのとおりです。昨年11月、CTADでReisa Sperling医師、ACTCのリーダーの一人ですが、AHEAD 3-45の臨床試験のデザイン、そして初期の被験者のスクリーニング結果を発表しています。
AHEAD 3-45試験はプラットフォーム試験で、共通のプロトコルで姉妹試験2つ、A3試験・A45試験に参加者を無作為割り付けしていきます。Preclinical AD、EarlyからLate stageをカバーしています。A3では、境界域アミロイド蓄積の患者さんが組み入れられます。そして、脳内アミロイド蓄積を遅らせるという目的で試験が行われます。A45試験では、脳内アミロイドβ蓄積が陽性の被験者に対して、認知機能低下のリスクリダクションを目的として試験を行います。
投与レジメンですが、A3・A45試験それぞれに用量を設定します。ベースラインのアミロイド負荷に基づいたものです。また、全被験者に対し、アミロイドPET・タウPETの検査を行いますし、広範なバイオマーカーパネルを用い、CSFや血液中のバイオマーカーの変化の測定を行います。
先ほど申し上げましたように、Dr. Sperlingが初期のスクリーニング結果を発表しています。その結果、無作為割り付けとして、A3試験とA45試験への割り付けの比率は、ほぼ当社の予想どおりとなっています。ACTCと密に協力を続け、AHEAD 3-45試験への登録をグローバルに加速していきたいと考えています。「lecanemab」は、こういった早期段階のオペレーションに対し、ベネフィットのある最適な有効性・安全性プロファイルを有していると、私たちは信じているからです。
AD Continuumを基軸とするプロジェクトが進行中

「aducanumab」「lecanumab」は、脳内アミロイドβ凝集体をターゲットとするものですが、それに加えて2つ、追加で疾患修飾治療薬が臨床開発中です。アルツハイマー病のContinuumをターゲットとするためです。E2814は、新規の抗MTBRタウ抗体です。そして、抗タウ治療薬としては、特にアルツハイマー病におけるものとしては、ベスト・イン・クラスになるポテンシャルがあると考えています。
アルツハイマー病ではタウ病変の拡散は、MTBRを含むフラグメントがタウ伝播種となり、拡散すると考えられています。そして、細胞外のMTBRタウフラグメントを捕捉するように、E2814はユニークにデザインされています。そして、タウ伝播種の蓄積の拡散を予防することを狙っています。
CTADで11月に、フェーズⅠ単回投与試験の結果を発表しています。健常被験者において、単回静注投与でE2814は忍容され、血中およびCSFの薬物動態は一般的抗体薬と同等でした。また、CSF中のMTBRタウにE2814が直接作用していること、MTBRタウに結合していることが示されました。反復投与漸増試験を行い、来年度には第Ⅱ相試験に進めていきたいと計画しています。ユニークなE2814については、大変エキサイティングだと感じています。
E2511は新規のシナプス再生剤です。選択的にTrkAに結合します。しかも、望ましくない経路をNGFが誘発し、活性化することがありません。E2511は、ユニークなファースト・イン・クラスの化合物で、アルツハイマー病の根本の病態生理をターゲットとします。それは2つのメカニズムによります。まず、ダメージを受けたコリン作動性神経を、機能性神経に回復すること。2つ目が、コリン作動性神経の変性を予防することによってです。
E2511は現在、フェーズⅠ単回投与試験を行っており、このユニークな化合物についても、その可能性について、とてもエキサイティングだと感じています。
AD診断環境が着実に進展中

次に、スライド11です。よりシンプルにアルツハイマー病を診断するという環境も、迅速に展開が見られています。社会のキャズムに対応し、初の疾患修飾薬の到来に備えて診断ができる、という環境が整うことは重要です。Cogstateと協力し、世界的に認知機能診断デジタルツールを導入しようと努力しています。
アミロイドβの血液検査については、日本では島津製作所の最近の進展、そして米国のC2Nのスクリーンテストの進展を見て、エキサイティングであると感じています。どちらも質量分析に基づくものです。また、エーザイはパートナー、シスメックスの「HISCL」システムを使ったアミロイドβ血液テストについて、共同開発を進めています。低コスト・高スループットのテストを実現する、大きなポテンシャルがあると考えています。
先ほど申し上げましたように、認知症患者さまの60パーセントが低中所得国に暮らしています。単純な血液検査ができるようになれば、こういったコミュニティにとって非常に有益なものになるでしょう。次世代のさまざまな診断法について、力強くサポートを続けていきたいと考えています。アミロイドβだけではなくp-タウ、その他、病態生理学的なバイオマーカーを使ったものもサポートしていきます。
そして300万人ものアルツハイマー病の患者さまに、本当の意味のベネフィットを提供できる、疾患修飾薬が提供できるようにしていきたいと考えています。
神経変性疾患の診断と治療概念変革への長期的コミットメント
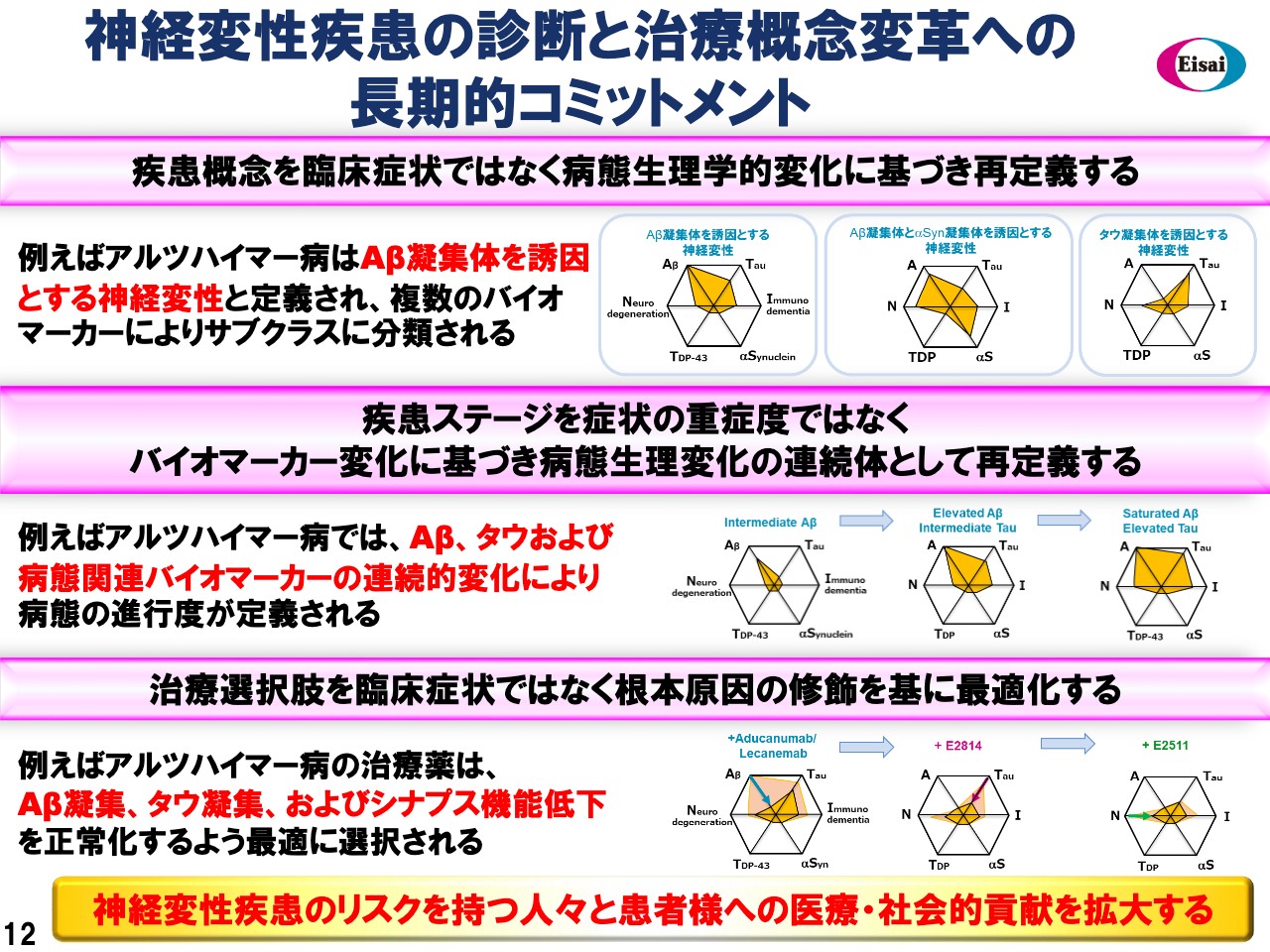
私の最後のスライドでは、12枚目ですけれども、エーザイが、神経変性疾患の診断治療を変革する長期のコミットメントを示していることを、再度強調して申し上げたいと思います。根本原因、臨床症状ではなく病態生理に基づいて、疾患を診断するべきであると考えています。そして、Aβ凝集体を誘因とする神経変性という再定義。そして、タウのようなバイオマーカーのフットプリントを使い、さらに再分類をすることが、アルツハイマー病について可能だと考えています。
また、AD Continuumについては、病態生理学のバイオマーカーの変化によって再定義ができる。臨床症状に基づくのではなく、と考えています。AD Continuumについては、例えばアミロイドβやタウ、その他、重要なバイオマーカーの変化によって再定義ができると考えています。認知機能パフォーマンスの変化を見るのではなく、です。
3つ目に、治療オプションについても再定義が可能であると考えています。疾患の根本原因を修飾することによってです。臨床症状を対象とするのではなく、です。例えば治療選択肢についても、アミロイドβ凝集、タウ凝集、シナプス機能低下を正常化するというかたちで、治療選択肢を選択するように再定義されていくのではないかと考えています。
エーザイはリーディングカンパニーとして、神経変性疾患のリスクを持つ方々、そして、患者さまへの医療・社会的貢献を拡大する貢献を続けてまいる所存であります。次は井池からです。
柳:ビジネスについて、井池より説明いたします。
レンビマ①

井池輝繁氏:スライドは13ページでございます。「レンビマ」の状況、そしがん領域のパイプラインについてご説明をいたします。左の図にお示ししていますように「レンビマ」売上、累計1,038億円、前年比129パーセントと伸びました。ただCOVID-19の影響、そして、今期計画をしていました肝細胞がん、「キイトルーダ」併用の米国迅速承認が得られなかったことによる、計画からのディレイが見えてしまいました。
米国は、子宮内膜がん・腎細胞がんが伸びています。そして中国、昨年12月に国家償還リストの収載が決まっています。今後の飛躍的な患者さまアクセスの拡大を見込んでいまして、MRの大幅な増員を行っています。欧州、Virtualプロモーションの活用によりまして131パーセントの伸び。日本は、肝細胞がんでTACE不適の患者さまへの貢献を進めています。
レンビマ②

次のスライドの14ページでございますけれども、こちらは「レンビマ」の新しい適応症をお示ししています。このスライドの左の上にございますように、「レンビマ」単剤といたしまして、中国で甲状腺がんの承認を、現地のフェーズⅢ試験をもとに、昨年11月に取得いたしました。そして、その下にありますように、日本では胸腺がんの適応で目下申請中でございます。
その右の箱にございますが、「キイトルーダ」併用で腎細胞がん。これは3つの重要な有効性の連続ポイントをすべてヒットいたしまして、申請の準備中でございます。このフェーズⅢ試験の結果の詳細は、今月、2月13日の「ASCO-GU」で口頭発表の予定でございます。
そして、子宮内膜がん。これは、米国ですでに迅速承認を受けています適応の検証試験に当たります。このフェーズⅢ試験も成功いたしました。この結果は3月19日、「SGO」、米国の婦人科がん学会で、プレナリーセッションでの口頭発表が決定いたしました。こちらもグローバル申請の準備中でございます。
その下の箱にお示ししていますけれども、胃がんは、「ケモセラピー」併用での1LのフェーズⅢ試験を新たに開始することを、メルクさんと合意いたしています。そしてバスケット試験では、迅速承認の申請目的も視野に入れまして、症例数を拡大いたしています。また、膵臓がんを新たに開始いたしました。小児での臨床試験も順調に進行中でございます。
レンビマ+キイトルーダ

次のスライドの15ページに移らせていただきます。「レンビマ」「キイトルーダ」併用、いわゆるLEAP studiesの状況でございます。スライド中ほど左寄りに、子宮内膜がん・腎細胞がんを示していますけれども、「レンビマ」「キイトルーダ」併用のフェーズⅢとして、結果がポジティブに出ました。第1、第2のフェーズⅢ試験でございましたけれども、2つともポジティブでございました。
その右側の大きい枠の中にお示ししていますように、10以上の承認申請用の試験が進行いたしています。肝細胞がんは先ほど申しましたように、シングルアームのフェーズⅡ試験による米国の迅速承認はなりませんでしたけれども、フェーズⅢ試験(LEAP-002試験)は、すでに昨年の春に患者さまの登録を完了いたしています。
そして肺がん。非小細胞肺がん、1LのLEAP-007試験は患者さまの組み入れを完了いたしました。もう1つの肺がん1Lでございます、オールカマーの006試験も、間もなくラストペイシェントの予定でございます。間、3つ目のLEAP-008試験も順調に進行中でございます。全体的にCOVID-19による治験の遅れは最小限にとどめられていまして、2025年度の5,000億円に向けて、順調に進行中でございます。
ポスト レンビマを担うファーストインクラスのNMEパイプラインの乳がんでの進展

次のスライドの16ページ目に移らせていただきます。こちらはパイプラインより、乳がん関係の2つのテーマをお示ししています。
上側、「H3B-6545」、クラス名を「SERCA」と呼んでいます。エストロゲンの受容体に共有結合して阻害するという、新規メカニズム経口剤でございます。このH3B-6545、これまで約130名の乳がんの患者さまで臨床評価をされています。ホルモン受容体の変異が、治療抵抗性と関係していることが報告されていますけれども、変異の中でも頻度が高く、予後が悪いと言われています変異を持つ患者さまに、特に期待が持たれています。
スライドの下には「E7090」をお示ししています。これは国内ですでに先駆け指定を受けていまして、胆管がんで開発を進めていますけれども、並行して、当社では乳がんでも前臨床研究を進めてまいりました。乳がんのCDK4/6抵抗例で、FGFとその受容体が発現量が上がる、という臨床のエビデンスが報告されていますけれども、このたび乳がんで、この「E7090」、ホルモン療法併用の臨床試験を開始いたしました。
がん領域のパイプライン

続きまして、スライドの17ページ目。細かくて恐縮ですが、がん領域のパイプラインをお示ししています。一番上の行、赤枠で囲んでいます、「レンビマ」「キイトルーダ」併用の子宮内膜がん。そして中ほど、同じく赤枠で囲っています腎細胞がん。こちらは、ともにグローバルの申請の準備中でございます。
そしてスライド中ほど、「E7438(タゼメトスタット)」でございますが、こちらは当社初のプレシジョン・メディシンとなることを期待いたしていまして、日本で申請中でございます。その下の「E7777」でございますけれども、こちらは申請中ですけれども、このたび医薬品の第2部会で承認が了承されています。
Cancer Continuumに基く患者様価値創造
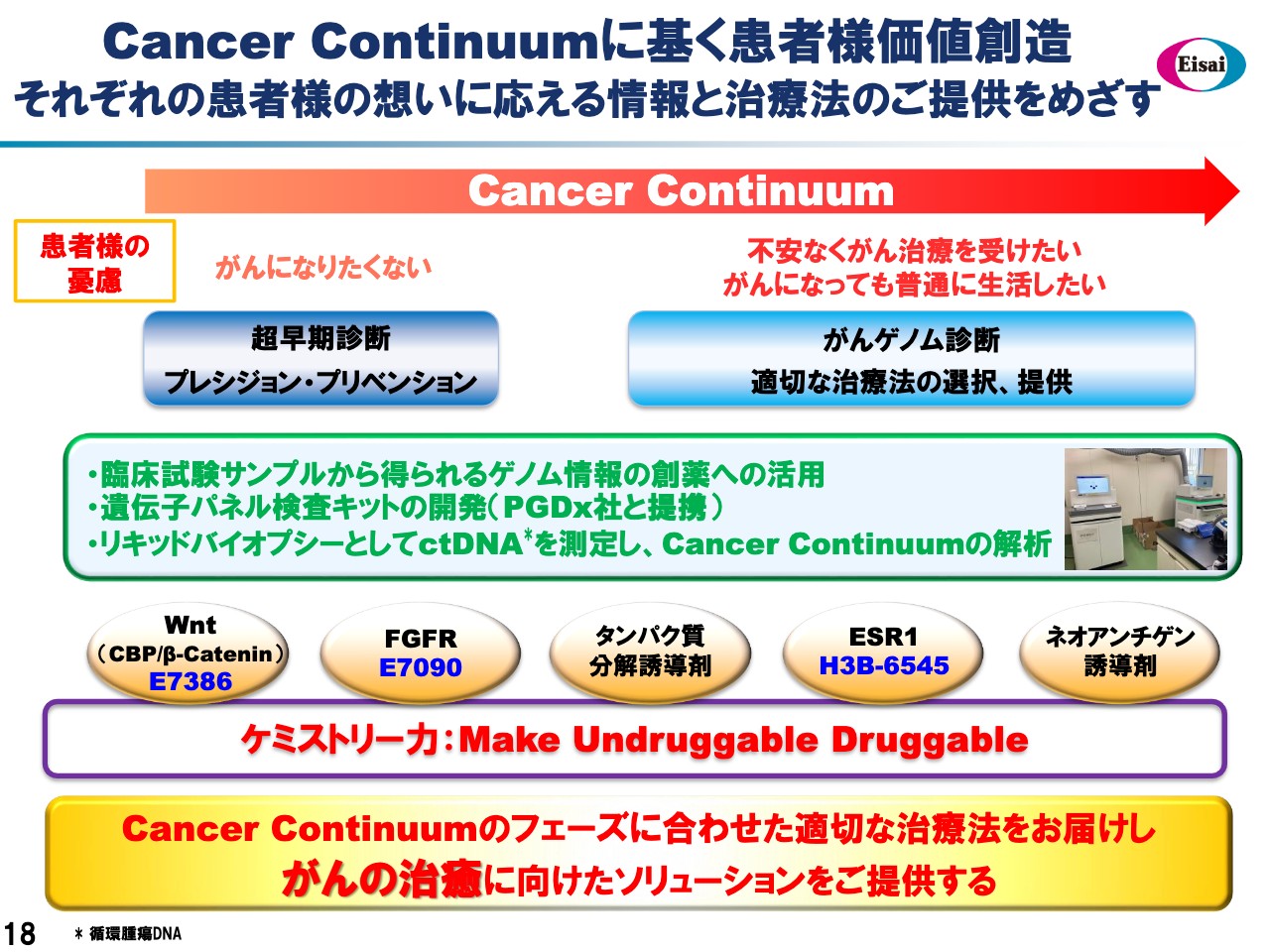
続きまして、次のスライド18枚目で、次世代のパイプラインについて若干触れさせていただきます。患者さま個々のがんの性質が、ゲノムレベルで解明されていく時代になっています。患者さまのご不安・憂慮を解決するために、ゲノム情報に基づく早期の的確な診断、そして、患者さまに合った治療法の選択が鍵になると考えています。
血液のサンプルから、がん由来のDNAゲノム解析を行うために、当社の筑波研究所でリキッドバイオプシーのラボを立ち上げています。そしてスライド中段、緑色の箱の下に、我々の注力プログラムの一部を挙げさせていただきました。がんのシグナルパスウェイといたしまして、VEGFに加えましてWnt、FGFがトップティアとして重要と考えています。
「レンビマ」の豊富な臨床データによりまして、これらのパスウェイに関わる、豊富なバイオジーのデータが蓄積いたしています。「レンビマ」、あるいは免疫療法への抵抗に関わるWnt、そしてFGF。これらは、Beyond「レンビマ」として必須であると考えています。
また、タンパク質分解誘導剤も重要な柱と考えています。そして、Bristol-Myers Squibb社と提携して共同研究開発を行っています、ネオアンチゲンの誘導剤。こちらは、スプライシングに作用いたします当社の化合物群を用いて、共同研究が進んでいます。我々のケミストリー力によりまして、UndruggableであったターゲットをDruggableにする。そしてプレシジョン・プリベンションと、がんの治癒に貢献をしてまいりたいと思います。
引き続き、ご理解・ご支援をよろしくお願い申し上げます。以上、がん領域の説明をさせていただきました。
企業価値向上に向けた機会への積極的資源投入を継続

柳:それでは再びCFOの柳より、最後にオーバーオールなステートメントを述べさせていただきます。最後のスライド、19ページをご覧ください。ここまでご説明してまいりましたように、エーザイは今、非常に重要な時期にさしかかっています。将来の企業価値向上に向けた、大きなポテンシャルへのオポチュニティが眼前にある。そして、それに向けて中長期的な視野で先行投資を断行している、という時期にあります。
そして、その将来投資の3本柱は、次世代ADによる患者さま貢献のAD-DMT。「レンビマ」フランチャイズの価値の最大化を図る、LEAP study。そして、COVID-19以後の世界も睨みながら、DXを基軸としたBusiness Transformationを行う、ということになります。こうした大きなプロジェクトを支えていくためにも、Strongバランスシートが重要になってきます。
その財務の健全性、ファイナンシャルインテグリティに依拠して、適切なキャピタルアロケーションやキャッシュアロケーションを図っていき、積極的な投資、安定配当を両立して、将来の患者さま貢献、企業価値を最大化してまいりたいと思います。それは取りも直さず、パーパス・企業理念に沿った経営であって、使命としての患者さま貢献のために、先行的な投資を今実行する。
そして、結果として中長期的、事後的に経済的価値を創出する。すなわち、ショートターミズムに陥らずにロングターミズムで。例えば、平均ROE10パーセント以上を持って企業価値を作っていくような、サステナブル経営を指向してまいりますので、引き続きご支援のほどをよろしくお願いします。以上をもちまして、プレゼンテーションのセッションを終了いたします。ここまでご清聴ありがとうございました。
新着ログ
「医薬品」のログ