株式会社カイオム・バイオサイエンス 2019年12月期第2四半期決算説明会
カイオム・バイオサイエンス、創薬支援事業が増収するも開発委託費用増加等で減益幅は拡大
損益計算書
小林茂氏:代表取締役社長の小林茂でございます。本日はお暑いなか、弊社の第2四半期決算説明会にご出席いただきまして、誠にありがとうございます。
さっそくですが、2019年12月期第2四半期の決算説明を始めさせていただきたいと思います。最初に第2四半期の業績でございます。
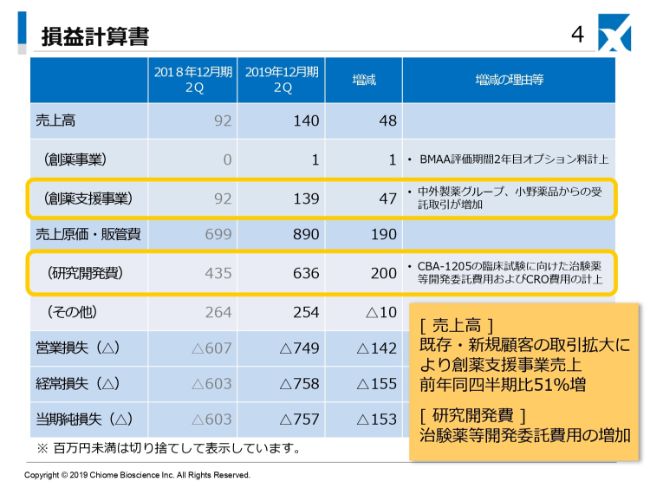
まず損益計算書ですが、2019年12月期第2四半期の売上高は1億4,000万円で、そのうち創薬支援事業が1億3,900万円と、ほとんどの売上が創薬支援事業から来ております。
研究開発費が6億3,600万円となっていて、営業損失、経常損失、当期純損失がそれぞれ7億4,900万円、7億5,800万円、7億5,700万円となっております。
前年同期と比較しますと、売上高が4,800万円、創薬支援事業が4,700万円のプラスで、約51パーセント増となっております。また、研究開発費は2億円ほど増えておりますが、これはのちほど説明する開発パイプライン「CBA-1205」の臨床開発に向けて準備が進んでいるための外注費用等でございます。
先ほどの創薬支援事業の売上については、中外製薬さまおよび小野薬品工業さまからの受託事業が順調に増加しているためであり、50パーセント強の増加となっております。
貸借対照表
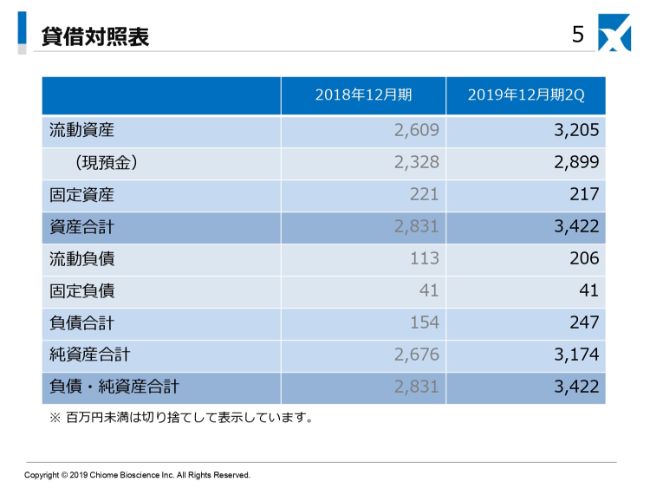
2019年12月期第2四半期末の貸借対照表は、流動資産が32億500万円、資産合計が34億2,200万円となっております。前年同期は流動資産が26億900万円、資産合計が28億3,100万円となっております。
キャッシュフロー計算書
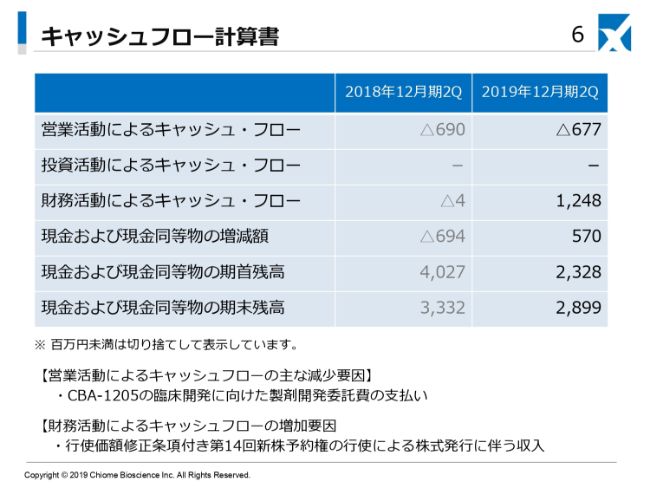
キャッシュ・フローについては、営業活動によるキャッシュ・フローがマイナス6億7,700万円、財務活動によるキャッシュ・フローが12億4,800万円となっております。
営業活動によるキャッシュ・フローのおもな減少要因としては、先ほど触れたとおり「CBA-1205」の臨床開発に向けた製剤開発や治験薬の開発、製造などに、CMOのコストがかかっているとご理解いただければと思います。
また、財務活動によるキャッシュ・フローの増加要因としては、行使価額修正条項付き第14回新株予約権の行使による株式発行に伴う収入ということになります。
当社の事業セグメント

それでは次に、2019年12月期の事業進捗についてご説明いたします。当社の事業セグメントは創薬事業と創薬支援事業に分かれています。
創薬事業は、アンメットニーズに対する抗体医薬をキーワードとして、自社開発や共同開発も含め初期の臨床開発まで進め、その結果を(製薬企業等に)導出することによって契約金、アップフロント、マイルストーン、ロイヤルティ等を収入としていく事業でございます。
もう1つの創薬支援事業は、当社が培ってきたタンパク質を扱う技術、ノウハウなどを活用し、高品質のサービスをある程度限定された顧客に提供させていただくといった受託ビジネスでございます。
具体的には、お客さまがお持ちの抗原、あるいは抗体といったタンパク質の発現、培養、生成等を受託として行っております。
創薬事業(パイプライン)①
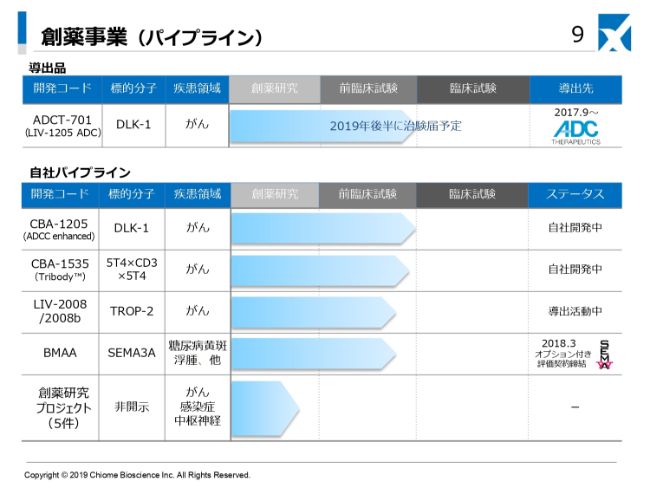
創薬事業の進捗状況、としてパイプラインのご紹介でございます。すでにスイスのADC Therapeutics社に導出している「ADCT-701」は、当社が先方とのコミュニケーションで得ている情報としては、固形がんを対象に、GLP試験という臨床試験に入る最後の非臨床的な試験がほぼ終了している段階でございます。
創薬事業(パイプライン)②

当社のパイプラインについてでございます。とくに肝細胞がんを中心とした固形がんを対象としたDLK-1抗体である「CBA-1205」も、当社がこれまでに計画したスケジュールどおりに進んでおり、2020年以降に国内での治験申請を行う準備が順調に進んでいる段階でございます。
具体的に申し上げますと、GLP試験が現在進行中でございます。また、先ほどキャッシュ・フローのところでもご紹介申し上げたように、治験薬の製造に向けたGMP原薬の製造、およびそれに続く治験薬の製造にこれから入っていくことになります。
続きまして「CBA-1535」でございます。これは当社が2018年12月にイギリスのバイオベンチャーから譲渡を受けた多重特異性抗体「Tribody™」というフォーマットに乗った、固形がんを対象とした抗体です。悪性中皮腫、肺がん、乳がんといった固形がんが対象となります。
現在、当社では「CBA-1205」の次のパイプラインとしてこの抗体の開発を進めていて、これから実際のGMP製造に向けたプロセスの確立を進めていく段階でございます。
「LIV-2008」はTROP-2抗体です。これは自社で開発を進めてきましたが、すでにADCのTROP-2抗体が他社さまで承認されつつあるもの、さらにそこからフェーズ1に入っているものがあるため、このまま当社が開発続けるのはなかなか難しいと思い、他社さまにこの抗体をさらにうまく活用していただくために他社さまの技術と合わせて臨床開発を進めていくべく、現在は海外の製薬企業さんを含め3社ほどが評価をしている状況でございます。
「BMAA」という抗セマフォリン3A抗体はがんではなく、糖尿病黄斑浮腫という網膜の病気(の抗体)です。(糖尿病黄斑浮腫は)成人の失明のおもな原因であり、これに対する治療薬ということで、カナダのSemaThera社が評価を進めている状況でございます。
このほかに創薬研究のプロジェクトは5つほど進めており、今後はリード抗体の選定ができたものから上のステージに上げていく状況でございます。
ここで1つ説明させていただければと思います。我々はよく臨床開発、あるいは臨床試験という言葉を使いますが、「CBA-1205」を例にとって説明させていただくと、当社は現在GLP試験を行っておりますが、このあとに治験申請というプロセスがございます。
そのあと、申請に対して当局から照会事項がきて、その照会事項に対応し終わった段階で臨床試験の施設と契約を結び、その後に患者さまを登録して、ようやく最初の患者さまに投与が始まります。
従って、治験申請を行ってからおよそ9ヶ月後に患者さんの登録が終わって投与が始まるといったようなタイムラインをイメージしていただくとよろしいかと思います。もちろん、当社はできるだけ短い期間で進めていくために努力いたします。
創薬支援事業 トピックス①

次に創薬支援事業でございます。今期のトピックスとしては、1つは富士レビオさまが当社の「ADLib®システム」という抗体作成のプラットフォームを使って作成した抗体を用いた診断薬キットをこの秋に販売開始いたします。それにともないまして当社と契約を締結いたしました。販売によって得られた収入の一部を当社がロイヤルティとして頂戴するという契約でございます。
富士レビオさまが販売しておりますビタミンDに対する抗体がすでにヨーロッパ、日本で販売されておりますが、この度の製品化はこれに次いで2つ目の「ADLib®システム」で作成した抗体の製品化ということになります。
当社は以前、富士レビオさまとの共同研究契約を期間満了で終了したと開示しておりますが、本件においては富士レビオさまが、当社と契約がなされている間に作成した抗体の開発を進めて製品化したということでございます。
創薬支援事業 トピックス②

2つ目のトピックスといたしましては、協和キリンさまとの委受託基本契約締結というものがございます。
基本契約について申し上げますと、協和キリンさまからは以前から個別の案件を単発ベースで受託し、サービスを提供させていただいていたのですが、ある程度実績が積み重なってきたところで、当社の技術、サービスの品質などを評価していただき、包括契約を締結させていただくことになったという話でございます。
包括契約を結ぶことによって、個々の案件について一つ一つ契約を結ばずに済むため省力化が進むということで、さらに受託をしやすい環境になってまいります。
創薬支援事業
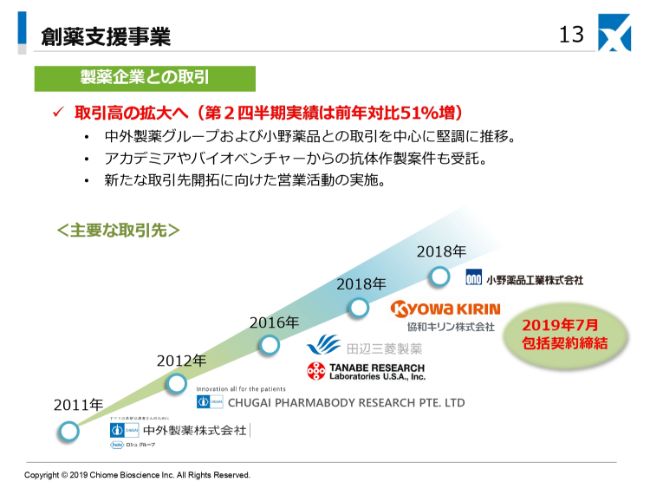
創薬支援事業全体を見ますと、2011年初期に当社の事業を始めてしばらく経った頃から、中外製薬さまとの受託事業が始まり、現在ももちろん続いております。
さらにそこから田辺三菱製薬さま、協和キリンさま、小野薬品工業さまといった新しいクライアントを開拓して、この第2四半期は前年同期に比べて50パーセント増の事業となりました。
社員や我々役員も含め、個人で保持するネットワークを活用し、さらに新たな製薬企業さま、バイオテック企業さま数社を新たな顧客として取り込んでいきたいと考えております。
一方、当社の訴求ポイントは、お客さまの立場に立って、サテライトラボのような感覚で使っていただける高品質のサービスを提供することであり、顧客の数だけを増やせばいいとは考えておらず、安定的にお付き合いいただける重要な顧客を大事にしていきたいと考えております。
その他
創薬事業と創薬支援事業につきましては、ご説明したとおりでございます。以下は資金調達の状況でございます。
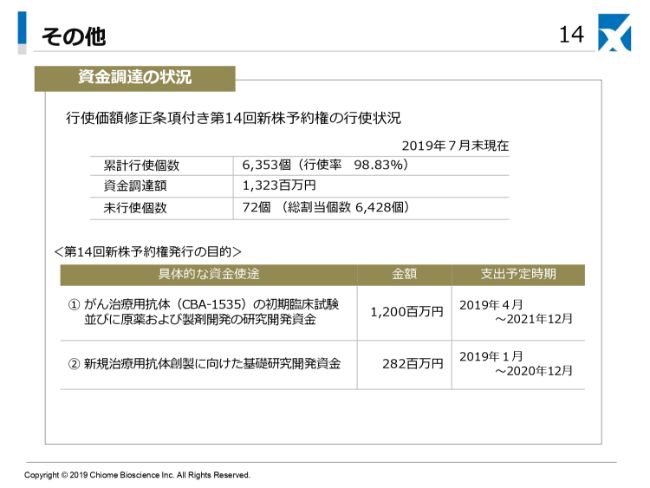
行使価額修正条項付き第14回新株予約権の行使状況としては、累計行使数が6,353個で、行使率としては98.83パーセントでございます。資金調達額は13億2,300万円となっております。未行使数は72個でございます。
本調達の目的としては、1つ目ががん治療抗体「CBA-1535」の初期臨床試験、原薬および治験薬開発の研究開発資金という目的で12億円、新規治療用抗体創製に向けた基礎研究という目的で約2.8億円の調達を行っております。
以上、簡単ではございますが、第2四半期のトピックスと事業の状況についてご説明申し上げました。ありがとうございました。
新着ログ
「医薬品」のログ





